翻訳|liquid
精選版 日本国語大辞典 「液体」の意味・読み・例文・類語
えき‐たい【液体】
改訂新版 世界大百科事典 「液体」の意味・わかりやすい解説
液体 (えきたい)
liquid
物質の状態は形と体積のありようから三つに区別される。直観的には,形が一定なら固体,形は一定しないが体積が一定なら液体,そして形も体積も一定しないのが気体である。液体は形が一定しない点で気体と同じであり,また体積が一定している点では固体と同じである。このため,液体は気体に通じる性質と固体に由来する性質の両面をもっている。前者は流動性として古くから知られていたが,後者はようやく1930年代以降の研究によって明らかとなったミクロの構造に関するものである。液体のこの二面性は今日の液体像の根幹である。
液体の分類
液体が化学的に単一な物質よりなっているとき,これを純液体または単に液体と呼び,2種類以上の物質からなる場合を溶液と呼んでいる。また,中性の分子からできている液体は分子液体と呼ばれ,希ガス,酸素,窒素,二酸化炭素などを液化すると分子液体となる。多くの有機化合物の液体も分子性液体である。金属の液体は金属液体と呼ばれ,電子ガスの中に正の金属イオンが閉じ込められている。ケイ素の結晶は共有結合でできた半導体であるが,融解すると金属液体となる。塩化ナトリウムなどのイオン性化合物がとけると,正負のイオンからなる液体となり,これを溶融塩という。このほか,液体を構成している分子が,電気的双極子をもつか否かにより,有極性液体と無極性液体に分けることもある。
固体と気体のはざま
液体研究の歴史における最初の画期的なできごとは,19世紀後半にファン・デル・ワールスによって発表された状態方程式の研究である。彼が半ば実験的に提出したこの方程式は,ファン・デル・ワールスの状態方程式と呼ばれているが,これによって気体と液体との間の連続と不連続が統一的に扱われ,当時,永久ガスといわれていた気体をことごとく液化する道が開かれた。20世紀に入ってヘリウムが最後に液化されて,固体,液体,気体の3状態を柱として物質観を築き上げる礎ができ上がった。
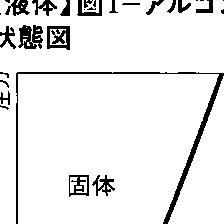
液体をつくっている分子やイオンの間に働く力をここでは単に分子間力と呼ぶことにしよう。多種多様な液体に対応して分子間力もまたいろいろであるが,その大筋は共通している。すなわち,分子間力は接近すれば強い反発力が働き,離れると弱い引力に変わる。この特徴のために,あらゆる物質は固体,液体,気体の三つの状態または相をとることができる。一つの平面上に温度と圧力を座標軸にとって,これらの状態が安定に存在する領域をかき分けた図を状態図という。図1はアルゴンの状態図である。おおづかみにいえば,曲線OTSは固体と気体,液体とを分ける境界線である。この境界線上では両側の相が共存し,一方から他方へ密度の不連続な飛びを伴って相転移する。曲線OT上では低い密度の気体と高い密度の固体とが平衡し(昇華曲線),曲線TS上では高密度の固体が同程度に高い密度の気体と平衡する(融解曲線)。点Tから短い境界線TCが分岐して,密度の異なる気体の間に切れめを入れて二つの相に分ける。液体または液相と呼ぶ状態は,Tを頂点としてTCを1辺とする扇形の領域である。扇の縁に相当する境界線は存在しないから,液体は高温,高圧の気体へ連続的につながっている。液相,気相の二つの相はTの近傍では明らかに異なっていて,TC上で相転移が起こる(蒸発,凝縮)。他方,Cを迂回すれば連続的につながった一つの相となっている。つまり,状態図はまずは固体と気体に二分されていて,液体はそのはざまに気体に寄生する形で存在している。Tは三重点,Cは臨界点と呼ばれ,純粋な物質に固有の定点である。
1対の分子の相互作用が球対称のポテンシャルで表されるとき,分子が丸いという。丸い分子からなる液体は単純液体と呼ばれ,現在もっともよく理解されている。液体アルゴンはその典型であり,多くの金属液体も単純液体と見てよい。
ミクロの構造
液体の統計力学は,単純液体について1930年代格子模型から始まった。やがてJ.G.カークウッドらにより,分布関数を中心とした本格的な理論が展開され,60年ごろには積分方程式を解いて具体的にミクロの構造を精度よく求めることもできるようになった。一方,同じころから計算機実験が行われるようになって,純粋な古典液体(量子力学的効果が本質的に重要となる液体ヘリウムを量子液体というのに対して,通常の液体を古典液体という)の研究は急速な発展を見るに至った。実験の側では,X線や中性子線を用いる回折実験の技術が開発されて,液体構造を直接探るもっとも普遍的手段となり,環状の回折像の解析から,液体の一つの分子を取り囲む分子群の分布密度の時間平均を求めることができるようになった。それは瞬間瞬間の分子配列を平均したもので,次のように定義される。まず,液体全体としての平均の分子密度は全分子数を全体積で割ったものである。これに対して一つの分子を取り囲む分子群の分子密度は,中心分子の影響のために必ずしも平均の密度と一致しない。すなわち,中心の分子のすぐ近くには,反発力のために他の分子は近寄れないから,密度は0となる。十分遠くではもはや中心分子の影響は及ばなくなり,平均の密度に落ち着く。一般の距離における密度を,平均の密度を単位として測ったものを動径分布関数という。単純液体では,エネルギーや圧力など主要な性質がこの関数と分子間力とから導かれるため,動径分布関数は液体構造論における主役というべき量である。図2はX線回折実験から求めた液体アルゴンの動径分布関数である。三重点の近くでは(曲線A)分子直径に相当する距離のあたりに鋭いピークが現れる。このピークの位置と形から一つの分子に寄り添っておよそ10個の分子がそのまわりを取り囲んでいることが明らかにされた。さらに,第2のピークが分子直径のおよそ2倍のところに現れ,第1と第2のピークの間には過疎の谷間ができている。このように,各分子のまわりには時間平均の意味で局所的な構造ができている。それは,結晶の場合の長距離にわたる周期的秩序には及ばないけれども,局所的にはそれに準じたもので,局所的秩序あるいは短距離の秩序と呼ばれる。たくさんの球を無造作に積み上げると,その中に同様な構造が見られるという。したがって,短距離の秩序は,分子どうしが互いに他を排除するために生じたといってよい。温度を上げると,局所的な秩序はしだいに失われ,臨界点を超えると高密度の気体となる(曲線B)。また,計算機実験により,剛体の球の集団が,一方では最密充てんの結晶構造をとり,他方ではそれよりやや小さい密度で短距離秩序をもった集合状態,つまり液体となって安定することが見いだされた。このことからも,高密度の状態で構造を決める主体は反発力であって,引力は高い密度の状態を低い圧力下で実現する役目を担っているということがわかった。反対に,気体と液体の間の相転移では,一般に密度の大きな変化を伴うから,ここでは引力も重要な役目を果たしている。
熱運動
ヘリウムを例外として,三重点より低い温度では安定な液体は存在しない。この事実は,液相を安定化するうえで分子の熱運動が本質的な役割を演じていることを物語っている。空間を規則的に分割して,分子はめいめい自分の小空間を占拠して永住するというのが結晶とすれば,液体では空間の分割は不規則,分子のすみわけは不完全,かつ時間的にも一定しない。分子は絶えずブラウン運動をしながら移動するので,わずかの外力によって流動が起こる。図3は液体アルゴンについて,計算機実験から求めた速度の相関関数〈v(t)・v(0)〉/〈v(0)2〉である。これは,任意の分子の時刻0における速度とt秒後における同じ分子の速度v(t)との間の相関を表す量である。三重点の近くでは(曲線A)相関関数の値は1から始まって急速に減少し,負となって停滞する。分子は10⁻13秒程度の周期で振動するが,振動の位相の記憶はたちまち失われる。実は位相のみならず,振動の方向も中心も無秩序に変動し,分子は拡散していく。その速さはおよそ10⁻12秒間に1Å移動する程度である。一方,臨界点近傍では(曲線B),分子の運動は振動的ではなく,多数回の衝突を経験しながらしばらくは行き足を維持している。これはもはや気体分子の熱運動である。
以上,アルゴンを例にして単純液体について述べてきたが,単純液体以外の液体についても,われわれの知識は現在急速に深まりつつある。なお,液体の水の構造と性質は,とくに三重点の近傍では単純液体と切り離して理解すべきものである。
→水
執筆者:山本 常信
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「液体」の意味・わかりやすい解説
液体
えきたい
物質の状態の一つ。圧力や容器の形によって容易に形を変え、流動性を示すものを一般に流体とよんでいる。流体には気体と液体がある。気体はいくら大きな容器に入れても容器全体を満たし、容器に孔(あな)があいていると外界に逃れてしまう。これに対し、液体は、容器の下方にたまり、開いた容器に入れて保つことができる。このような液体を、閉じた容器に入れて圧力を加えれば、すきまがなくなり、密度も大きくなる。
通常の物質には臨界温度というものがあって、この温度より上では、容器の下方にたまるという性質をもつ液体は存在しなくなる。なお水の臨界温度は374.1℃である。臨界温度より上では、圧力と密度がいくら高くても気体とよんでいるが、液体と気体の区別がなくなるということである。臨界温度より低い温度では、飽和蒸気の圧力より高ければ液体に、低ければ気体になり、この場合には同じ物質の気体と液体の密度にはかなりの違いがある。通常、われわれが気体というときには、このような低密度の気体をさすので、この場合には液体に比べると密度がかなり小さい。
気体と液体のほかのもう一つの状態は固体である。固体のなかでも、結晶になっているものでは、その中の分子が規則正しい結晶格子をつくって配列している。金属の場合には、外見は水晶のような単結晶とは違っているが、小さな結晶が集まっており、小さな結晶の中では、それぞれ分子は規則正しく並んでいる。固体というと、通常はこのような結晶性の固体をさすことが多い。結晶性固体と液体とのいちばん大きな相違は、X線回折写真がまったく異なることである。結晶性固体では、規則正しい格子によっておこる回折により、きれいな同心円の環状の像ができるが、液体の場合には幅広いぼやけた環ができるだけである。このことは、液体の中では、分子の配列は規則性がないことを示している。しかし、液体の分子は、気体の場合のように、ほとんど完全に無秩序になっているわけではなく、非常に小さい範囲に限れば、少数の分子は、ある程度の規則性をもって並んでいるが、広い範囲でみれば、まったく無秩序とみてよい。
中性子線の回折の実験によると、液体の分子は、振動をしながら、ゆっくり移動していることが明らかにされている。一般に、固体が融解して液体になると、すきまが多くなり、密度が減少する。氷の結晶のように、すきまの多い構造をもつものの場合には、融解するとかえって密度が大きくなるが、このような例は少ない。われわれが通常固体と考えているもののなかに、結晶性でないものがある。このようなものを非晶質(アモルファス)固体というが、分子が液体と同じように無秩序に配列している。ガラスもその一例であるが、これは過冷却された液体とみられている。
[小野 周]
液体の性質
結晶性固体の場合には、結晶格子が変形しにくいため、その形を保ち、ずれの応力に対しても抵抗をする。したがって、ずれの弾性(剛性)をもつ。これに対して、液体では、分子が相対的に位置を変えやすいので、容易に変形し、ずれの弾性率はゼロである。このため、液体の中では、固体と違って、横波は存在せず、縦波が伝播(でんぱ)するだけである。もちろん、液体の表面で、表面張力や重力によっておこる表面波は横波である。また、ずれの応力に対しては、抵抗なしに変形するので、静止した液内では、ずれの応力は存在せず、液体内にとった任意の面に対する力は、つねにこの面に垂直で、したがって、その力は面の向きによらない。このことは、静止している液体内の圧力は、どの面にも垂直で、また表面や器壁に対しても垂直になることを意味する。このような圧力を静水圧とよんでいる。また、液体内の圧力を大きくすれば、液体内の圧力は、すべての場所で同じ大きさだけ増加する。これをパスカルの原理という。
液体が運動しているときには、ずれの応力を生じる。これが液体の粘性である。このため、液体も、非常に急激な形の変化に対し剛性を示す。前に述べたガラスの場合には、粘性が極端に大きくなったものとみることができる。実際にガラスなどは、力をかけておくと、非常にゆっくりではあるが変形をするといわれている。液体内の分子は、振動しながら移動するが、異種の分子の拡散の場合にも事情は同じであって、液体内の拡散は、固体に比べると大きいが、気体に比べると小さい。
ここで述べたことの多くは、純粋な液体でなく2成分以上でできている溶液などにもそのまま当てはまる。また液体と結晶性固体の相違として、液体はいつも等方性をもつことがあげられる。
[小野 周]
百科事典マイペディア 「液体」の意味・わかりやすい解説
液体【えきたい】
→関連項目固体
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「液体」の意味・わかりやすい解説
液体
えきたい
liquid
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
化学辞典 第2版 「液体」の解説
液体
エキタイ
liquid
物質の集合状態の一つで,流動性をもち,一定の形はもたないが一定体積をもつ.温度,圧力の変化に関し,気体と固体の中間に位置する.固体と異なり分子の運動は自由であるが,分子間距離が接近しているため凝集力が大きく,一定体積を保つ.その物理的性質は,一般に気体と同様等方的であるが,まれに異方性液体も存在する.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
世界大百科事典(旧版)内の液体の言及
【音声学】より
…〈金〉[ki![]() ]。(4)流音liquid(図5参照) (a)歯茎側音lateral[l]は舌先を歯茎にあて舌の両側から息を流す。英語のlip[l
]。(4)流音liquid(図5参照) (a)歯茎側音lateral[l]は舌先を歯茎にあて舌の両側から息を流す。英語のlip[l![]() p]〈唇〉。…
p]〈唇〉。…
【子音】より
…また鼻音では有声の場合が多いので妨害の位置のみ指定し,両唇鼻音[m]のように呼ぶ。さらに閉鎖音と摩擦音を合わせて阻害音obstruentと称し,側音と顫動音,弾音をまとめて流音liquidという。以上の基本的調音に,ある変形を加えるものを副次的調音と呼ぶが,次のような副次的調音がある。…
※「液体」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
1 花の咲くのを知らせる風。初春から初夏にかけて吹く風をいう。2 ⇒二十四番花信風...