内科学 第10版 「代謝性肝疾患」の解説
代謝性肝疾患(肝・胆道の疾患)
脂肪肝(fatty liver)は,アルコール性肝障害と非アルコール性脂肪性肝疾患(non-alcoholic fatty liver disease:NAFLD)に大別される(図9-11-1).NAFLDのおもな病因はインスリン抵抗性で,肝のみでなく全身疾患としてとらえる必要がある.NAFLDは,病態が進行することのまれな単純脂肪肝と10~20%の肝硬変や肝細胞癌(hepatocellular carcinoma:HCC)へと進行する非アルコール性脂肪肝炎(non-alcoholic steatohepatitis:NASH)に分類される.NASHは肝組織所見から提唱された疾患概念で,いまだその診断には病理診断を要する(岡上ら,2010).
分類
NAFLDは,アルコール性肝障害をきたすほどの飲酒歴がないにもかかわらず肝に脂肪沈着をきたす病態の総称で,単一な疾患ではない.病理所見から,simple steatosis(単純脂肪肝)と壊死炎症性変化を伴うsteatohepatitis(NASH)に分類され,病因から肥満やインスリン抵抗性を基盤に発症する一次性と二次性に分類される.
原因・病因
NAFLDのおもな病因はインスリン抵抗性で,肥満やメタボリック症候群を基盤に発症する.二次性NAFLDとしては,内分泌疾患(下垂体機能低下症,Cushing症候群,甲状腺機能低下症,成長ホルモン欠損症,多囊胞性卵巣症候群,など),脂質代謝異常症,薬剤(ステロイド,タモキシフェンなど).高度の栄養障害(Crohn病,短腸症候群,神経性食思不振症)などが病因となる.
疫学
わが国では,飽食,運動不足により肥満人口は増加の一途をたどり,NAFLDは最も頻度の高い肝疾患となった.性・年齢別有病率は,日本人における肥満人口をそのまま反映する.男性は30歳代から60歳代まで30%前後のほぼ一定の高い有病率を示し,女性は20歳代では5~8%であるが年齢とともに徐々に増加し,閉経後では20~30%と上昇する.また,高度肥満例では約80%,糖尿病では30~50%がNAFLDを合併する.食生活や遺伝的要因(patatin-like phospholipase 3 geneなど)により家族集積をみる.人種による疾患感受性は,米国からの報告ではヒスパニック,白人,黒人の順である. わが国の全国調査によると,肝硬変の成因ではNASHは2.7%,また,HCCの基盤肝疾患では2.0%がNAFLDで,今後さらに上昇すると予測されている.
病理
病理学的には肝細胞の5%以上に脂肪滴を認めるものをsteatosis(脂肪肝)と定義し,simple steatosisと肝細胞の膨化(壊死性変化)と炎症性細胞浸潤を伴うsteatohepatitisに分類される.steatohepatitisでは,pericellular fibrosis,perivenular fibrosisから線維化が進行し肝硬変に至る(図9-11-2).
病理分類には,3つの代表的な分類がある.Matteoniの分類は,単純脂肪肝とNASHの分類で,単純脂肪肝は,type 1(脂肪沈着のみ)とtype 2(脂肪沈着+実質の炎症性細胞浸潤)で,NASHは,type 3(脂肪沈着+肝細胞の膨化)とtype 4(type 3に加えてMallory体や線維化を認めるもの)である.Bruntの分類は,NASHの重症度分類で,活動性(グレーディング)と線維化(ステージング)からなる.グレーディングは,脂肪沈着,肝細胞の膨化,炎症性細胞浸潤の重症度からmild,moderate,severeに分類され,ステージングは,ステージ1は中心静脈周囲の線維化,ステージ2は,さらに門脈域の線維化が加わり,ステージ3はbridging fibrosis,ステージ4は肝硬変である.そして,the NASH Clinical Research Network North America Pathologists Workingから,Bruntの分類を基に,NAFLDを活動性(NAS)と線維化の重症度で診断する病理分類が提唱された(Kleinerら,2005).NAFLDの予後を予測する上では線維化の重症度が最も重要な病理所見である.
病態生理
脂肪肝は,脂肪酸の流入,合成,燃焼,VLDLの肝からの分泌のアンバランスにより発症する.過食,高インスリン血症は,脂肪細胞から遊離脂肪酸を肝へ流入させる.脂肪酸合成では,sterolregulatory element binding protein-1c(SREBP-1c)が最も重要な転写因子で,インスリンやSREBP-1cそのものによる転写促進により合成が亢進する.また,肥満によるレプチン抵抗性も stearoyl-CoA desaturase-1を介して脂肪酸合成を促進する.脂肪酸の燃焼に関しては,インスリンは肝ミトコンドリアのβ酸化を低下させる.アディポネクチンは,peroxisome proliferator activated receptorα作用を活性化して脂肪酸を燃焼するが,肥満ではアディポネクチンは低下する.これらが脂肪肝のおもな病因である.
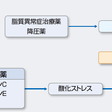
NAFLDの10~20%の症例が単純脂肪肝にとどまらずNASHへと病態が進行することに関しては,2ヒット理論が提唱されている.肝細胞への脂肪沈着をfirst hitとして,何らかのsecond hitが加わって壊死炎症性変化をきたしNASHとなる(図9-11-3).Second hitとしては,①酸化ストレス,②TNF-αなどのアディポサイトカイン,③インスリンの抵抗性,④チトクロームP450 2E1の異常,⑤鉄過剰などがあげられ,遺伝的要因も重要である.
肥満や糖尿病はHCCの危険因子である.これらを病因とするNASHでのHCCの発癌機序に関しては十分解明されていないが,酸化ストレスによるDNA障害,脂質過酸化,オーバル細胞の増加,高インスリン血症やサイトカインが成長因子として作用し腫瘍細胞の増殖を促すことなどがあげられている.
臨床症状
1)自覚症状:
NAFLDでは,肝硬変に進行するまで多くの症例で無症状である.診断の契機は,定期健康診断が多い.非代償性の肝硬変に進行すると黄疸,腹水,肝性昏睡などの肝不全症状を呈する.
2)他覚症状
:
多くの症例で肥満を合併する.脂肪肝では軽度の肝腫大を認める.
検査成績
1)血液・生化学検査
: NAFLDでは,ALT優位のトランスアミナーゼの上昇が特徴であるが,30~60%の症例では正常値を示す.線維化がbridging fibrosisまで進行すると,ヒアルロン酸などの肝線維化マーカーが上昇し,肝硬変に進行すると,ALTは低下し,AST優位となり,AST/ALT比は1以上となってくる.血小板・アルブミン・凝固因子が低下し,非代償期ではビリルビン・アンモニアが上昇する.
2)画像診断:
画像診断では,30%以上の肝細胞に脂肪沈着を認めた場合に,その重症度を含め脂肪肝と診断される.超音波検査では,エコーレベルの上昇,肝腎コントラストの上昇,深部エコーの減衰,血管の不明瞭化で脂肪肝が診断される.CT検査は,客観的評価が可能で,CT値は低下し,肝臓/脾臓のCT値比率(L/S比)が0.9未満であれば脂肪肝と診断できる.MRIやMRスペクトロスコピーも有用である.
3)肝組織診断
: 肝生検により肝組織標本を採取するが,リスクやコストの点からルーチンに行われる検査ではない.しかし,組織診断は肝疾患の診断,重症度判定をする上で最も正確である.NAFLDと診断され,さらにNASH診断のため肝生検の適応となる症例は,肥満や生活習慣の改善ができずトランスアミナーゼ高値が継続する症例,肝機能が低下傾向でNASHが疑われる症例,ほかの肝疾患との鑑別が必要な症例である.
4)その他:
NAFLDでは肝障害のほか,病因に起因する高血糖インスリン抵抗性,LDLコレステロールや中性脂肪の高値,HDLコレステロールの低下,フェリンチンや血清鉄の高値を示す.また,酸化ストレスの亢進による高感度CRP上昇や酸化LDLの上昇や頸動脈エコーでのプラークの形成などを高率に認める.
診断
NAFLDは,①非飲酒者②肝組織あるいは画像診断での脂肪肝の診断③ほかの原因による肝疾患の除外で診断される(岡上ら,2010).非飲酒者には,アルコール性肝障害をきたさない程度の少量飲酒者は含まれる.女性はアルコール代謝が男性に比較して弱いため,女性ではエタノール換算20 g/日以下,男性では30 g/日以下とされている.しかし,アルコール代謝能の低いALDH2遺伝子変異型の保有率の高い日本人では,その2/3が妥当である.NASHは,NAFLDで病理診断がsteatohepatitisを呈する症例である.
鑑別診断
NAFLD・NASHでは,血液診断マーカーがなく除外診断となる.Wilson病やC型肝炎では脂肪肝が特徴的病理所見の1つで,鑑別は重要である.また,自己免疫性肝炎・薬物性肝障害などでも脂肪肝を呈する症例があり,肝組織検査を含む鑑別診断が必要である.
合併症
NAFLDは,メタボリック症候群の肝病変である.95%以上の症例でインスリン抵抗性を示し,肥満,糖尿病,脂質異常症,高血圧などの生活習慣病を合併する.睡眠時無呼吸症候群合併例では無呼吸時の低酸素状態がNASHを増悪させる.
経過・予後
NAFLDは,心血管イベントと肝関連死亡が増加し,非合併例に比較して,生命予後が低下する.NASHでは,5年肝硬変進行率は10~25%,5年生存率は85~95%,肝関連死亡は10~30%と報告されている.一方,NASH肝硬変に進行すると,5年HCC発癌率は約10%,5年生存率は約75%で,死因はHCCや肝不全による肝関連死が約80%となる.
NASH肝硬変の末期では,脂肪沈着,炎症性細胞浸潤などのNASHの特徴が消失し,burned-out NASHとなる.NASHを基盤に発したHCCの特徴は,平均年齢65~75歳,男性に高頻度で(55~65%)で,肝硬変を基盤とする症例が多く多中心性発癌である.
治療・予防
NAFLDは,その病因にあわせた治療戦略をたてる(図9-11-4).病態の進行は,脂肪肝をfirst hitとして,何らかのsecond hitが加わって進行する.これを受けて,食事と運動療法を中心とした肥満と生活習慣病の治療と,second hitに対する治療としての抗酸化剤(ビタミンE,ビタミンC)や肝庇護薬(ウルソデオキシコール酸など)が行われる(岡上ら,2010;恩地ら,2010).高度肥満例では,数kgの減量でAST・ALTは正常化するが,肥満状態が続けば病態は進行するので,正常体重にまで戻すことが望ましい.NAFLDによる末期肝硬変は,移植適応疾患である.移植後NAFLDが再発する症例は約30%と報告されているが,重症例は少なく移植後の生存率は良好である.[橋本悦子]
■文献
Kleiner DE, Brunt EM, et al: Nonalcoholic Steatohepatitis Clinical Research Network. Related Articles: Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology, 41: 1313–1321, 2005.
岡上 武,田村信司,他:NASH・NAFDLの診療ガイド2010(肝臓学会編).文光堂,2010.
恩地森一,他:肥満と消化器疾患(日本消化器病学会編).金原出版,東京,2010.
出典 内科学 第10版内科学 第10版について 情報