化学辞典 第2版 「イオン交換平衡」の解説
イオン交換平衡
イオンコウカンヘイコウ
ion-exchange equilibrium
イオン交換樹脂が外部溶液と平衡にある状態をいう.樹脂相と外部溶液相との間にドナンの膜平衡が成り立つと考えると,同符号イオン間(たとえばA,B間)の交換平衡式が次式で得られる.
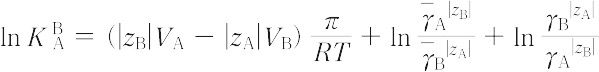
ここに,γは活量係数,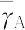 のバーは樹脂相,zはイオン価,Vは部分モル容積,πは膨潤圧である.KAB は次式で示され選択係数という.
のバーは樹脂相,zはイオン価,Vは部分モル容積,πは膨潤圧である.KAB は次式で示され選択係数という.
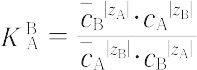
ここに,cは濃度である.また次式で示される SAB は分離係数という.
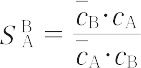
異価イオンの分離係数は濃度によっていちじるしく変化し,希薄溶液のとき,多価イオンの選択性が大(SAB が大)となる.液体クロマトグラフィーのように分離すべきイオンAが交換するイオンBに対して微量と考えると,次式で示す分配係数
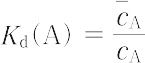
は,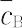 /cBが一定とみられるので,Kd(A)によって選択性を表しうる.最近の液体クロマトグラフィーでは,分配係数のかわりに次式で示す質量分配比(キャパシティーファクター)
/cBが一定とみられるので,Kd(A)によって選択性を表しうる.最近の液体クロマトグラフィーでは,分配係数のかわりに次式で示す質量分配比(キャパシティーファクター)
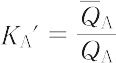
が用いられる.ここに,Qはイオンの量を示す.陽イオン交換における選択性は
Ba2+ > Ca2+ > Mg2+ > K+ > Na+,
陰イオン交換における選択性は
NO3- > Cl- > HCO3- > F-
である.H+ の選択性は強酸性樹脂ではきわめて小で,逆に弱酸性樹脂はもっとも大である.OH- の選択性も強塩基性樹脂ではきわめて小で,弱塩基性樹脂ではもっとも大である.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報


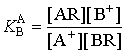 を定義すると,R-がB+に比してA+を選択的に捕捉する場合はKBAが大きい値となる。…
を定義すると,R-がB+に比してA+を選択的に捕捉する場合はKBAが大きい値となる。…