精選版 日本国語大辞典 「イオン交換樹脂」の意味・読み・例文・類語
イオンこうかん‐じゅしイオンカウクヮン‥【イオン交換樹脂】
- 〘 名詞 〙 イオン交換を行なう合成樹脂の総称。不溶性、多孔質の有機高分子化合物。一九三五年、イギリスのアダムズとホームズが発明。海水からの真水製造、硬水の軟化、糖類・医薬品の精製、化学分析などに広く用いる。有機ゼオライト。
日本大百科全書(ニッポニカ) 「イオン交換樹脂」の意味・わかりやすい解説
イオン交換樹脂
いおんこうかんじゅし
ion exchange resin
イオン交換作用を示す物質(イオン交換体)の一種。水に不溶性の合成樹脂で、陽イオン交換樹脂、陰イオン交換樹脂、両性イオン交換樹脂などがある。
[垣内 弘]
歴史
イオン交換現象は古くから知られていたが、化学的には19世紀の初めにイギリスの土壌学者トムソンH. S. ThomsonとウェイJ. Wayが明らかにした。ある種の土壌において、カルシウムイオンとアンモニウムイオンの間で陽イオン交換がおこることをみいだし、このときの交換は当量関係があり、あるイオンは他のイオンより容易に交換するという選択性を発見した。初めは粘土物質が交換剤として用いられてきたが、1935年にアダムスB. A. AdamsとホームズF. L. Holmesらが、多価フェノールとホルムアルデヒドとを縮合させた樹脂が塩類水溶液と陽イオンを交換し、さらにアニリンやメタフェニレンジアミンとホルムアルデヒドの縮合物の樹脂粒子が硫酸基を吸着する陰イオン交換性をみいだし、その後ドイツのIG(イーゲー)社によって系統的な研究と工業的なイオン交換樹脂の製造が始まった。また同じころにアメリカのレジナス社(現、ダウ・テュポン社)でも研究が行われ、1941年にイオン交換樹脂としてアンバーライトAmberliteの商品名で市販された。日本でもこのころから京都大学の小田良平(1906―1992)、三菱(みつびし)化成(現、三菱ケミカル)などがイオン交換樹脂の研究を開始した。第二次世界大戦中、アメリカ、ドイツなどで、イオン交換樹脂による水処理、人絹工場廃水からの銅の回収、キニーネの抽出精製、希土類元素の分離抽出など用途が急速に広がっていった。日本ではイオン交換樹脂を用いる海水の淡水化などが進んだ。戦後、スチレン系の強酸性陽イオン交換樹脂がローム・ハース社より発売されてスチレン系イオン交換樹脂の時代が始まり、核分裂生成物の分離、高純度純水の製造、各種の比較的高価な物質、たとえばアミノ酸や抗生物質の精製が工業的規模で行われ、またカンショ糖液の脱色、テンサイからソフトシュガーの直接製造、海水濃縮による食塩の製造などと多方面に工業的に応用されている。またイオン交換樹脂の利用技術として、膜状にしたイオン交換膜が開発されて幅広く用いられている。
[垣内 弘]
構造
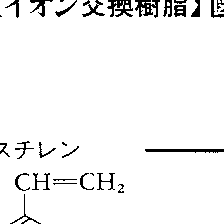
三次元の立体的な構造をもった高分子化合物(母体という)にイオン交換機能をもった交換基が共有結合で安定に結合し、その交換基が樹脂表面になるべく一様に分布していることが必要である。高分子母体は現在はスチレンとジビニルベンゼン(DVB)の共重合体で、DVBはスチレンの線状重合体に適当に架橋させるために用いる。
[垣内 弘]
種類
母体に導入される交換基の種類によって強酸性陽イオン交換樹脂(カチオン交換樹脂ともいう)、弱酸性陽イオン交換樹脂、強塩基性陰イオン交換樹脂(アニオン交換樹脂ともいう)、弱塩基性陰イオン交換樹脂がある。そのほか特殊なものとして、特定の金属とキレート結合のできる官能基を有するキレート樹脂や、両性のイオン交換樹脂などがある。母体であるスチレンとDVB共重合体の構造は、透明でほぼ均質なゲル形(ヘテロポーラス形ともいう)と、物理的に大きな孔径をもったマクロポーラス形とに大別でき、各種交換基とを組み合わせて多数の種類の商品が市販されている。
[垣内 弘]
性質
色は白、黄、橙(だいだい)、褐色、黒色など各種あり、一般に水を吸収した状態で市販されている。その粒子の大きさは大部分20~40メッシュ(粒子直径0.4~0.6ミリメートル)の不定形粒状または球状であり、前者は塊状または粒状のイオン交換樹脂を粉砕してつくったものである。含水状態での比重は1.2~1.4程度である。
[垣内 弘]
製法
母体の高分子物質としては、以前は多価フェノール類とホルムアルデヒドの縮重合物が用いられていたが、1960年ごろからはすでに述べたようにスチレンとDVBの架橋共重合体が用いられている。これに種々の官能基を導入していくが、架橋度の調節はDVBの量で行う。一般にDVB含有量6~16%程度であり、標準架橋はDVB含有量8%付近のものである。
陽イオン交換樹脂は交換基として酸性基を、陰イオン交換樹脂は交換基として塩基性基を導入したものであり、弱酸性基と弱塩基性基の両者をもったものが両性イオン交換樹脂である。
導入されるイオン交換基としてよく用いられるものは次のものである。
(1)強酸性基 スルホン酸基 -SO3H
(2)弱酸性基 カルボキシ基(カルボキシル基) -COOH、フェノール性ヒドロキシ基 -OH
(3)強塩基性基 第四アンモニウム塩基 -NH3⊕OH⊖
(4)弱塩基性基 第一、第二、第三アミン(-NH2、-NHR、-NR2)
などがある。
[垣内 弘]
用途
イオン交換がおもな用途である。陽イオン交換樹脂と陰イオン交換樹脂の作用を以下に示す。式中のRは母体。
●陽イオン交換樹脂
式(1)中和反応
R-SO3⊖H⊕+Na⊕OH⊖
⇄R-SO3⊖Na⊕+H2O
式(2)中性塩分解反応
R-SO3⊖H⊕+Na⊕Cl⊖
⇄R-SO3⊖Na⊕+H⊕Cl⊖
式(3)複分解反応
R-SO3⊖NA⊕+K⊕Cl⊖
⇄R-SO3⊖K⊕+Na⊕Cl⊖
●陰イオン交換樹脂
式(4)中和反応
R-NH3⊕OH⊖+H⊕Cl⊖
⇄R-NH3⊕Cl⊖+H2O
式(5)中性塩分解反応
R-NH3⊕OH⊖+Na⊕Cl⊖
⇄R-NH3⊕Cl⊖+Na⊕OH⊖
式(6)複分解反応
R-NH3⊕Cl⊖+Na⊕Bi⊖
⇄R-NH3⊕Bi⊖+Na⊕Cl⊖
これらの式からイオン交換反応は平衡反応であることが理解できるであろう。
[垣内 弘]
純水の製造と用水処理
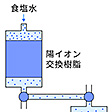
現在、蒸留水の製造はイオン交換法によっている。それぞれのイオン交換樹脂の粒状のものをカラム(ガラスや金属製の筒。管柱)に充填(じゅうてん)しておき上部から食塩水NaClを流下させると、式(2)の反応で粒状の陽イオン交換樹脂にナトリウムイオンが固定される。流出水中には塩酸HClが残る。次に陰イオン交換樹脂を充填したカラムに流下させると、式(4)の反応で塩素アニオンが固定され、流出した水は純水になる。この逆の反応が海水からの食塩の製造であるが、現在ではより能率的なイオン交換膜を用いて行われている。
用水処理とはエレクトロニクスや電力用の水処理である。天然水中ではカルシウム、マグネシウムなどの陽イオンや、炭酸水素イオンや硫酸イオンなどのほかにシリカやコロイド状有機酸が陰イオンとして考えられ、陰イオン交換樹脂で吸着または交換される。
[垣内 弘]
その他の用途
イオン交換樹脂は、イオン交換を主とする用途と、固体触媒としての使用法がある。前者はすでに述べた純水の製造のほかに硬水の軟化、ホルマリン中のギ酸の除去、各種イオンの分離抽出(希土類元素、超ウラン元素など)、ビタミン、アルカロイド、アミノ酸などの抽出精製、めっき廃液中からの重金属イオンやシアンイオンの回収などがある。触媒としての利用は、カチオン交換樹脂またはアニオン交換樹脂が、酸または塩基触媒反応の固体触媒となる。反応後の触媒の回収は濾過(ろか)ですむから反応生成物の精製が容易になる。
[垣内 弘]
『小田良平・清水博著『イオン交換樹脂』(1950・学術図書出版社)』▽『本田雅健他編『イオン交換樹脂』(1955・広川書店)』▽『山辺武郎・妹尾学著『イオン交換樹脂膜』(1964・技報堂)』▽『北条舒正編『機能性高分子シリーズ キレート樹脂・イオン交換樹脂』(1976・講談社)』▽『『テクニカルレポート イオン交換樹脂・膜の最新応用技術』(1982・シーエムシー出版)』▽『高分子学会編『入門 高分子材料――高度機能をめざす新しい材料展開』(1986・共立出版)』▽『中村泰治・中谷一泰著『生化学の理論――ポイントと解説』第2版(1993・三共出版)』▽『西山隆造・安楽豊満著『はじめての化学実験』(2000・オーム社)』
改訂新版 世界大百科事典 「イオン交換樹脂」の意味・わかりやすい解説
イオン交換樹脂 (イオンこうかんじゅし)
ion-exchange resin
不溶性の高分子の骨格にイオン交換能のある原子団を化学結合させた合成樹脂の総称。通常20~50メッシュの球状,あるいは無定形であり,骨格高分子は橋架けにより不溶化されている。交換基の種類によって,陽イオン交換樹脂cation-exchange resin(酸に相当する)と陰イオン交換樹脂anion-exchange resin(アルカリに相当する)に分類される。さらにその酸性度または塩基性度によって,強酸性陽イオン交換樹脂(スルホン酸基をもつもの),弱酸性陽イオン交換樹脂(カルボン酸基,ホスホン酸基,ホスフィン酸基をもつもの),強塩基性陰イオン交換樹脂(第四アンモニウム基をもつもの),弱塩基性陰イオン交換樹脂(第一,第二,第三アミン基をもつもの)に分けられる。また特殊なイオン交換樹脂として,キレート樹脂,両性イオン交換樹脂,酸化還元樹脂などがある。その母体構造からみると,均質な高分子相からなるゲル型のものと,細孔の発達した多孔質型のものとに大別され,これら母体構造と交換基の種類の組合せで多種類の商品が作られている。
イオン交換樹脂は酸やアルカリとしての化学的性質を備えているが,架橋高分子であるため,水その他の溶剤に溶けない。陽イオン交換樹脂R⁻H⁺の場合,苛性ソーダNaOHや食塩NaClを加えると次のような反応が起こる。
R⁻H⁺+Na⁺OH⁻─→R⁻Na⁺+H2O (中和反応)
R⁻H⁺+Na⁺Cl⁻⇄R⁻Na⁺+HCl (中性塩分解反応)
また他のイオンの塩(たとえば塩化カルシウムCaCl2)を加えると次の反応が起こる。
2(R⁻Na⁺)+Ca2⁺(Cl⁻)2⇄(R⁻)2Ca2⁺+2(Na⁺Cl⁻) (複分解反応)
陰イオン交換樹脂R⁺OH⁻の場合も同様に,塩酸HCl,食塩NaCl,さらに他のイオンの塩(たとえば硫酸ナトリウムNa2SO4)を加えると以下の反応を起こす。
R⁺OH⁻+H⁺Cl⁻─→R⁺Cl⁻+H2O (中和反応)
R⁺OH⁻+Na⁺Cl⁻⇄R⁺Cl⁻+NaOH (中性塩分解反応)
2(R⁺Cl⁻)+(Na⁺)2(SO4)2⁻⇄(R⁺)2(SO4)2⁻+2(Na⁺Cl⁻) (複分解反応)
イオン交換樹脂の特徴の一つは再生使用のできることであり,その場合次の反応を利用する。
R⁻H⁺+NaOH─→R⁻Na⁺+H2O
R⁻Na⁺+HCl⇄R⁻H⁺+NaCl
製法
モノマー(たとえばスチレンやアクリル酸エステル)と二官能性以上の架橋性モノマー(たとえばジビニルベンゼン)との共重合を行い不溶性高分子を作る。共重合は懸濁重合によって行われ,20~50メッシュの球状物を得る。重合開始剤には過酸化物やアゾ化合物が利用され,懸濁安定剤にはポリビニルアルコールや炭酸カルシウムなどが用いられる。こうして生成した粒状高分子を加水分解したり,イオン交換基を導入したりすることによってイオン交換樹脂を製造する(図1)。
応用
イオン交換樹脂は上記のように,(1)中和,中性塩分解,複分解の三つの反応を起こす,(2)生成する高分子塩が不溶である,(3)再生が可能で反復使用ができる,といった性質をもっており,これら三つの性質を利用して,硬水の軟化,海水の純水化,金属の分離・回収,糖液の脱色処理,アミノ酸や抗生物質の精製,高分子触媒,原子力発電関係の放射性物質の処理,電子産業用超純水の製造など,多方面に使用される。またクロマトグラフィーなど分析機器にも用いられている。イオン交換の方法にはバッチ法とカラム法がある。バッチ法は,樹脂と液を容器に入れてかくはんし,イオン交換を行う方法で,微粒子懸濁液の場合には有効であるが,イオン交換平衡が成り立ち,効率がよくないので一般に用いられることは少ない。カラム法は,樹脂をカラムにつめ,被処理液を流してイオン交換を行う方法で,広く用いられる。図2に示すように,イオンA⁻を吸着した樹脂R⁺A⁻にA⁻より選択性の強いイオンB⁻を含む溶液を流すと,樹脂層上部からB⁻の交換吸着が行われる。C-D部を交換帯と呼び,交換が進むにつれ交換帯は下に移動する。交換帯が底部に達すると,B⁻のリークが起こるので樹脂を再生,交換する必要が生ずる。
イオン交換樹脂を膜状にしたものは,とくにイオン交換膜と呼ばれる。本質的にはイオン交換樹脂と同じであり,陽イオン交換膜にはスルホン酸基が,陰イオン交換膜には第四アンモニウム基が用いられている。陽イオン交換膜はNa⁺,Ca2⁺などのカチオンは透過するがアニオンは透過せず,逆に陰イオン交換膜はCl⁻,SO42⁻などのアニオンは透過するがカチオンは透過しない。イオン交換膜のこういった選択透過性を利用して隔膜に用いられる。電気透析用隔膜としては,海水の濃縮による食塩の製造や淡水の製造に用いられるほか,電解隔膜として食塩溶液の電気分解による塩素と苛性ソーダの製造に用いられる。この場合,塩素ガスに強い膜が必要であり,フッ素樹脂を骨格としたものがよく用いられる。
歴史
イオン交換樹脂は1935年にイギリスのアダムズB.A.AdamsとホームズE.L.Holmesによって発見され,39年にドイツのイーゲー・ファルベン社により初めて工業的に製造されウォファチットWofatitの商品名で販売された。44年アメリカのダレリオG.F.D'Alelioがポリスチレンを母体とした現在の構造の樹脂を発明してから化学的に安定な高性能の製品が製造されるようになった。第2次大戦中ドイツでは,ウォファチットを用いて水の精製を行い,また人絹工場における銅アンモニアの回収や写真工業における銀の回収に利用した。50年にはバークリウムBk,カリホルニウムCfの2元素が陽イオン交換樹脂によって単離された。50年以降イオン交換膜の研究も行われ,電気化学的応用も開けた。
→イオン交換
執筆者:福谷 秀夫
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「イオン交換樹脂」の解説
イオン交換樹脂
イオンコウカンジュシ
ion-exchange resin
イオン交換能のある解離基をもつ不溶性多孔質の合成樹脂の総称.多価フェノール類とホルムアルデヒドの縮合反応による,いわゆる縮重合型イオン交換樹脂が用いられたが,現在ではスチレン-ジビニルベンゼン(DVB)系の付加重合型イオン交換樹脂が主として用いられている.前者は,縮重合前のフェノール類に官能基を導入したのち高分子化したもので,後者は,まず架橋高分子母体を製造し,これに官能基を導入したものである.陽イオン交換樹脂(cation-exchange resin)は母体樹脂に酸性ヒドロキシ基,カルボキシル基,スルホ基などが結合している高分子酸で,陽イオン交換反応は正確迅速に行われ,また一般に安定であるから,高能率を保ちながら反復使用できる.陰イオン交換樹脂(anion-exchange resin)は,母体樹脂にアミノ基や第四級アンモニウム基のような塩基性基が結合している高分子塩基である.一般に,陽イオン交換樹脂よりやや性能が劣るが,再生可能で反復使用できる.これらイオン交換樹脂は,硬水の軟化,海水の純水化(塩水淡水化),アミノ酸や医薬品の精製分析,金属イオンの分離抽出,高分子触媒など多方面に利用されている.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「イオン交換樹脂」の意味・わかりやすい解説
イオン交換樹脂【イオンこうかんじゅし】
→関連項目イオン交換|機能性高分子|徐放薬|脱色剤
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「イオン交換樹脂」の意味・わかりやすい解説
イオン交換樹脂
イオンこうかんじゅし
ion-exchange resin
R-SO3-H++Na+Cl-→R-SO3-Na++HCl
イオン交換樹脂は水処理に最も広く使われ,硬水の軟化のほか,完全脱塩による非常に高純度の水の製造を可能にした。 F. H.スペディングらによる希土類元素の相互分離 (1947) は,交換樹脂の特筆すべき応用例。そのほか,廃液処理,有機物質の精製・分離,有機反応の触媒など利用面は広い。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「イオン交換樹脂」の解説
イオン交換樹脂
世界大百科事典(旧版)内のイオン交換樹脂の言及
【機能性高分子】より
…したがって,その機能については特定の定義があるわけではなく,多様なものを含んでいる。歴史も古く最も代表的なものとしてイオン交換樹脂があげられる。そのおもな機能はもとよりイオンの交換であるが,これが高分子の構造形成機能(この場合,水に不溶の小粒子)と結びついて初めて実用的なイオンの分離ができる。…
【制酸薬】より
…
[局所性制酸薬]
塩酸中和後も消化管から吸収されにくい化合物で,粘膜の被覆作用もある。酸化マグネシウム,炭酸カルシウム,水酸化アルミニウムゲル,胃粘膜ムチン,イオン交換樹脂など。二次性酸分泌亢進は起こしにくく,制酸薬として好ましい条件を備えたものが多い。…
【反応性高分子】より
…この固定化の方法の一つは反応性高分子と酵素を反応させることである。 反応性高分子の反応そのものを利用する高分子材料の代表例はイオン交換樹脂である。イオン交換は高分子上のイオン交換基によって行われるが,その基の導入のために反応性高分子が用いられる。…
※「イオン交換樹脂」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...