精選版 日本国語大辞典 「膜平衡」の意味・読み・例文・類語
まく‐へいこう‥ヘイカウ【膜平衡】
化学辞典 第2版 「膜平衡」の解説
膜平衡
マクヘイコウ
membrane equilibrium
溶媒と一部のイオンだけを透過する半透膜を隔てて,異種の電解質を含む溶液を接触させた場合に成り立つ化学平衡をいう.この現象をはじめて組織的に研究したF.G.Donnan(1911年)にちなんでドナンの膜平衡ともいう.膜平衡が成立している系では,膜を透過できないイオンの存在のため,膜透過性イオンは両溶液相中に均等に分布することができず,その結果,両相間に電位差(ドナン膜電位という)を生じる.平衡の条件は,膜透過性イオンについて両溶液相における電気化学ポテンシャルが等しいということによって与えられる.すなわち,膜透過性イオンに対しては次式が成立する.
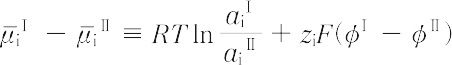
+ 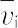 (pⅠ - pⅡ) = 0
(pⅠ - pⅡ) = 0
ここで,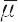 i,ai,zi および
i,ai,zi および 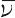 i はそれぞれiイオンの電気化学ポテンシャル,活量,イオン価(符号を含む)および部分モル体積であり,φは内部電位,pは圧力である.上付きの添字ⅠおよびⅡは膜の両側の溶液相を意味する.また,R,TおよびFはそれぞれ気体定数,絶対温度およびファラデー定数である.たとえば,膜透過性イオンがイオンiとjの2種類とし,両溶液相の浸透圧が適当な方法で釣り合わされているとすると,ドナン膜電位 ED は,
i はそれぞれiイオンの電気化学ポテンシャル,活量,イオン価(符号を含む)および部分モル体積であり,φは内部電位,pは圧力である.上付きの添字ⅠおよびⅡは膜の両側の溶液相を意味する.また,R,TおよびFはそれぞれ気体定数,絶対温度およびファラデー定数である.たとえば,膜透過性イオンがイオンiとjの2種類とし,両溶液相の浸透圧が適当な方法で釣り合わされているとすると,ドナン膜電位 ED は,
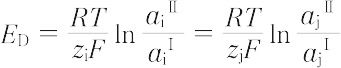
によって与えられ,またイオンiおよびjの活量に対しては,
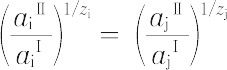
の関係が成立する.膜平衡の理論はコロイドあるいは高分子電解質溶液と半透膜の系,単純電解質の水溶液とイオン選択性膜の系などに応用される.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
改訂新版 世界大百科事典 「膜平衡」の意味・わかりやすい解説
膜平衡 (まくへいこう)
membrane equilibrium
膜で仕切られた電解質溶液の一方に膜を透過できないイオン(固定イオン,コロイドイオンなど)を含むとき,そのイオンの存在によって膜の両側における他のイオンの分布は影響をうけ,電気的中性の条件を満たすように,膜の両側でイオンの不均一分布をとって平衡に達する。これを膜平衡と呼び,その熱力学的理論は,1911年ドイツのドナンFrederick George Donnan(1870-1956)により与えられたので,ドナンの膜平衡ともいう。たとえば,高濃度の固定イオンをもつイオン交換樹脂が塩溶液中にあるとき,樹脂は固定イオンを通さない仮想的な膜で囲まれているとみなすことができるので,この系のイオン交換平衡を膜平衡として取り扱うことができる。樹脂中の固定イオンのために,樹脂相の塩濃度は外部溶液に比べて小さくなる。これをドナン排除という。この不均一分布を償うように,膜の内外に電位差を生じる。これをドナンの膜電位という。
→膜電位
執筆者:妹尾 学
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
ブリタニカ国際大百科事典 小項目事典 「膜平衡」の意味・わかりやすい解説
膜平衡
まくへいこう
「ドナンの膜平衡」のページをご覧ください。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

