日本大百科全書(ニッポニカ) の解説
デバイ‐ヒュッケルの理論
でばいひゅっけるのりろん
Debye-Hückel's theory
強電解質溶液の解離(電離)現象に関する理論。1923年にオランダのデバイとドイツのヒュッケルにより共同発表された。
スウェーデンのアレニウスが1887年に提出した電離説によれば、電解質は溶液の中でイオンに解離するが、これらは中性分子と電離平衡にあるとされた。電離度αは溶液の電気伝導度の測定から求められたが、さらにイオン解離の大きさを考慮して電離定数Kを導き、種々の溶液について測定値と比較したところ、弱酸・弱塩基についてはよい一致を示すが、強電解質では一致が悪いことがわかった。
デバイとヒュッケルは、強電解質では中性分子は完全にイオンに電離していると考え、溶媒を誘電体とし、イオン間にはクーロン力が働くとして理論式をたてた。溶液の浸透圧Pと理想溶液のそれP0との比をgと置き、これを浸透圧係数g=P/P0とすれば、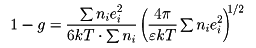
ここで、niは1cc中のイオンの数、eiはイオンの電荷、Tは絶対温度、kはボルツマン定数、εは溶媒の誘電率である。この理論を基として、溶液の性質に関する理論が発展した。コールラウシュの法則(電気伝導率の理論)、濃度と当量伝導度の関係を示したオンサーガーの式などがその例である。
[下沢 隆]
[参照項目] |
