電離定数
でんりていすう
electrolytic dissociation constant
電解質溶液中で電離によって生じたイオンと、電離していない分子の間に成り立つ平衡を電離平衡というが、電離平衡の平衡定数Kを、とくに電離定数あるいはイオン化定数という。たとえば、弱酸HAを水に溶かし、これの一部が解離して水素イオンH+(またはH3O+と書く)と酸の陰イオンA-を生じて平衡に達したとき、その電離定数は、
HA+H2O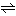 H3O++A-
H3O++A-
K=[H3O+][A-]/[HA][H2O]
である([ ]はそれぞれの濃度を表す)。イオンの濃度が小さいときには、この式のように濃度を用いてもKが一定になるが、濃度が大きくなる場合には補正濃度としての活動度を用いる必要がある。一般にKの値が大きなものを強電解質、小さいものを弱電解質という。
[戸田源治郎・中原勝儼]
出典 小学館 日本大百科全書(ニッポニカ)日本大百科全書(ニッポニカ)について 情報 | 凡例
Sponserd by 
電離定数
デンリテイスウ
electrolytic dissociation constant
電解質溶液中では,溶質MAと,電離してこれから生じたイオン M+ および A- との間に平衡が成り立つ.
MA  M+ + A-
M+ + A-
おのおのの活量を aMA,aM+,aA- としたときに,
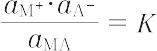
は温度一定のとき一定値を示す.この値を電離定数とよぶ.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
Sponserd by 
世界大百科事典(旧版)内の電離定数の言及
【オストワルトの希釈律】より
…それによると,たとえば2個のイオンに解離する弱電解質MAの電離平衡 MA⇄M++A-において,溶液の希釈度をV,電離度をαとすると α2/(1-α)V=Kの関係が成立する。ここでKは,温度と圧力とをきめれば一定の定数であって,これを電離定数electrolytic dissociation constantという。【玉虫 伶太】。…
【解離】より
…これは,イオンが水和によって安定化するためである。解離反応に対する平衡定数を解離定数といい,電離の場合にはとくに電離定数という。たとえば酢酸の電離は CH3COOH⇄CH3COO-+H+で表され,その電離定数は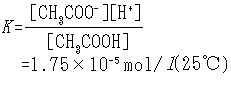 で与えられる。…
で与えられる。…
【電離説】より
… NaCl⇄Na++Cl- CH3COOH⇄H++CH3COO-これらのイオン解離の現象が〈[質量作用の法則]〉に従うものとすると,2個のイオンに解離する電解質の解離平衡の条件が次式で与えられる。 α2c/(1-α)=Kここで,cは電解質の濃度(解離したものと未解離のものとの和),αはイオンに解離した割合を示す電離度,Kは電離定数(または解離定数)とよばれる平衡定数で,近似的には濃度には無関係な定数である。酢酸のような弱電解質の場合には以上の関係がよく成立するが,塩化ナトリウムのような強電解質では,上式による電離定数の値が一定にならず,質量作用の法則からのずれが著しい。…
※「電離定数」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
Sponserd by 
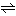 H3O++A-
H3O++A-



 M+ + A-
M+ + A-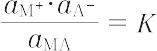
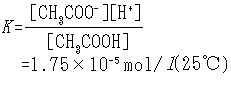 で与えられる。…
で与えられる。…