改訂新版 世界大百科事典 「電子不足化合物」の意味・わかりやすい解説
電子不足化合物 (でんしふそくかごうぶつ)
electron deficient compound
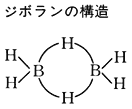
共有性化合物では,一つの結合すなわち結合している原子間に,一つ(あるいはそれ以上)の電子対を割り当てることができるのが普通である。これに対し,そのようにするのには電子が不足している化合物があるが,これらを一般に電子不足化合物といっている。たとえばジボランB2H6およびヘキサメチル二アルミニウムAl2(CH3)6のような化合物では次のような骨格をもっており,隣り合った原子の組合せはいずれも八つあるのに,結合に使われる電子対の数は六つしかない。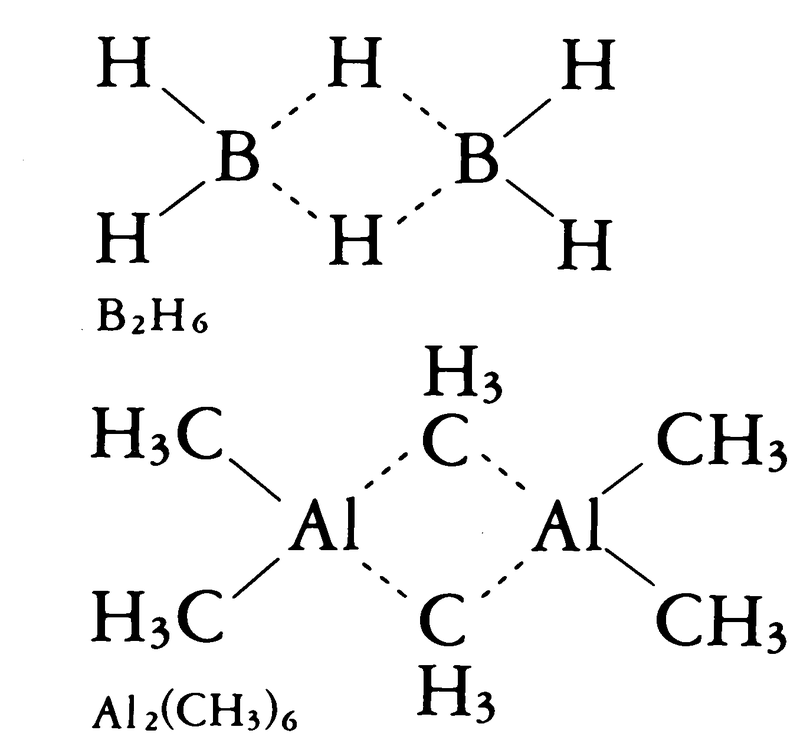
B2H6では六つのHから一つずつ,一つのBから原子価電子3個ずつで計12個,すなわち6電子対,Al2(CH3)6では同様にCH3のCから一つずつ,Alから三つずつで6電子対である。B2H6では両端の四つのB-Hに電子対を割り当てると,残りの中央のB…H…Bにそれぞれ2個の電子を割り当てねばならなくなる。このような場合を三中心二電子結合といっている。Al2(CH3)6の場合でも同様である。電子不足化合物はこのような多中心結合を含む化合物である。
執筆者:中原 勝儼
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報