関連語
日本大百科全書(ニッポニカ) 「二次反応」の意味・わかりやすい解説
化学辞典 第2版 「二次反応」の解説
二次反応
ニジハンノウ
second-order reaction
反応次数が2の反応.原系の成分をA,B,…などで表すと,速度定数をkとして,
v = k[A]2 (1)
あるいは,
v = k[A][B] (2)
の場合が普通である.A,Bの初濃度をa,b,任意の時間tまでの全反応量をxとすると,(1)および(2)式より,
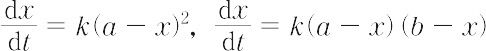
が得られ,積分して,
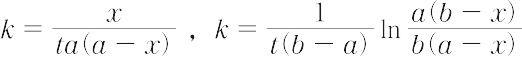
を得る.もっとも普遍的な反応速度式で,例が多い.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
梅雨の季節に入ること。つゆ入り。毎年6月中旬~7月中旬の約1ヵ月間,九州から東北地方は梅雨の季節に入る。これは,北方のオホーツク海高気圧と南方の小笠原高気圧とに挟まれて,揚子江流域から九州,四国,本州...

