内科学 第10版 「心室頻脈」の解説
心室頻脈(心室性不整脈)
定義・病態生理
心室頻拍は3連拍以上連続して出現する心室期外収縮で,通常心室拍数は100拍/分以上である.心室頻拍は多くの場合,Adams-Stokes発作,心不全,胸痛,血圧低下などを惹起し,心停止に至る致死的重症不整脈である.特に心筋梗塞や心筋症などの基礎心疾患を有する例に認める場合には突然死の危険性がきわめて高い.一方,基礎心疾患をなんら有さない心室頻拍を特発性心室頻拍とよび区別される.特発性心室頻拍は左脚後枝のPurkinjeネットワーク内リエントリーによる特発性左室心室頻拍(idiopathic left VT)とトリガードアクティビティによる特発性流出路心室頻拍(idiopathic outflow VT)に細分される.特発性心室頻拍では心機能は正常であるためAdams-Stokes発作や突然死は発現しにくい.しかしながら特発性心室頻拍でも長時間持続することで,拡張障害ついで収縮障害をきたし,心機能の低下をきたすことがあり,頻脈依存性心筋症(tachycardia-induced myopathy)として定義される.
心電図による分類
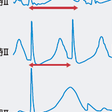
心電図所見ではQRS波形は幅広く0.12秒以上を示す頻拍(100拍/分以上)で基本的にはRR間隔は一定である.心室頻拍の分類は持続時間,QRS波形,心室頻拍レート,出現様式,発生機序および基礎心疾患の有無などによって分類される.代表的なものを以下にあげる.
1)持続時間による分類:
a)持続性心室頻拍:100拍/分以上で,30秒以上持続するか自然停止せず,停止のために薬物,ペーシング,電気ショックなどの緊急治療を要するもの.
b)非持続性心室頻拍:3拍以上連続し30秒以内に自然停止するもの.
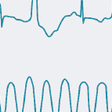
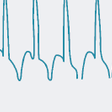
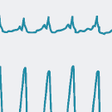
c)反復型またはインセサント型心室頻拍:非持続性心室頻拍が1~数拍の洞性心拍を挟んで繰り返し出現する(図5-6-24).
2)QRS波形による分類:
a)単形性(monomorphic)心室頻拍:心室頻拍のQRS波形が単一のもの(図5-6-24).
b)多形性(polymorphic)心室頻拍:心室頻拍のQRS波形が2種類以上のもの.
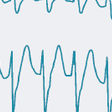
c)torsade de pointes(TDP)心室頻拍(図5-6-25):多形性心室頻拍のなかで,心室頻拍のQRS軸が連続して変化し,QRS波形が基線を軸としてねじれて回転するように周期的に変化する(図5-6-25).反復性を示し,ときに心室細動に移行し,通常はQT時間の延長を伴う(QT延長症候群).
d)二方向性(bidirectional)心室頻拍:2つの異なったQRS波形が交互に出現し,QRSの電気軸は1拍ごとに変化し,左軸偏位と右軸偏位を示す.通常ジギタリス中毒時やカテコールアミン感受性心室頻拍として発現する.
鑑別診断
wide QRSを示すほかの頻拍として,心室内変行伝導を合併する発作性上室頻拍および心房粗細動,WPW症候群を有する心房粗細動およびKent束を順行性に伝導し房室結節を逆行性に伝導する逆方向旋回性上室頻拍などがあげられ,これらの頻拍との鑑別が必要となる.このなかで,最も頻度が高くかつ鑑別が困難な頻拍が心室内変行伝導を有する発作性上室頻拍である(表5-6-6).心室頻拍の特徴的心電図所見として,①房室解離を約50%に認める,②捕捉収縮(洞性興奮が心室を捕捉する),融合収縮(洞性興奮と心室期外収縮による心室内興奮が融合する)を認める(図5-6-26).③右脚ブロック型の場合,V1誘導で三相性(Rsr),V6誘導では非常に深いS波を示すことが多く,左脚ブロック型の場合にはV6誘導でqR,R型,V1誘導で陰性波が深く,幅の広いr波を認める.④QRS電気軸は著明な左軸偏位または北西軸(−90°~−180°)を示す.⑤QRS幅が0.14秒以上である,⑥頻拍の開始時にP波を認めない,などである.また,上室性頻拍では眼球圧迫や頸動脈マッサージなどの迷走神経緊張手技,あるいはアデノシン三リン酸(ATP)などの迷走神経刺激薬の投与によって発作は停止するのに対して,心室頻拍では通常影響されず停止しないことも鑑別の助けとなる.最終的な確定診断には心内心電図による房室乖離の証明が必要である.
臨床的意義
心室頻拍は通常重症不整脈としてとらえる必要があるが,短時間であれば経過観察が容認されるものから緊急措置をしなければ致死的になり得るものまで,その臨床的意義は幅広い.最も重篤なものは,血行動態の破綻をきたす持続性心室頻拍(無脈性心室頻拍)である.持続性心室頻拍は基礎心疾患を伴うことが多いが,基礎心疾患を有さない特発性心室頻拍でも,流出路起源心室頻拍やベラパミル感受性左室起源心室頻拍,カテコールアミン誘発性多形性心室頻拍,Brugada症候群やQT延長症候群などの遺伝性不整脈がある.
心室頻拍の重症度は,①自覚症状,特にAdams-Stokes発作の有無,②基礎心疾患の有無と重症度,③心機能低下の程度(特に左室駆出率35%以下)などによって総合的に評価する.
自覚症状として,最も多いのは動悸であるが,非持続性心室頻拍では無症状であることも少なくない.持続性心室頻拍では,Adams-Stokes発作,心不全または狭心症を惹起し,最終的には心室細動に移行し,死に至ることもまれではない.
基礎心疾患としては,心筋梗塞などの虚血性心疾患,心筋症(拡張型,肥大型,二次性心筋症,催不整脈性右室心筋症など),弁膜症,先天性心疾患,高血圧性心疾患などがあり,基礎心疾患を有する例では特に心機能低下の程度が重要である.
基礎心疾患を有する症例の中で,特に心機能低下を伴う持続性心室頻拍は,突然死をきたしやすく予後不良である.非持続性心室頻拍でも,基礎心疾患を有する例ではAdams-Stokes発作など重篤な症状を有することもあり,無症候性でも左心機能低下を伴う場合には突然死をきたす危険性が高いため注意を要する.
特殊な心室頻拍
1)特発性流出路起源心室頻拍(図5-6-27):
左脚ブロック+正常~右軸偏位を示す流出路起源の心室頻拍であり,トリガードアクティビティを機序とすると考えられ,β遮断薬やNaチャネル遮断薬を用いるが,無効なことも多く心室頻拍の頻度が多く,有症候性であればカテーテルアブレーションのよい適応となる.
2)特発性左室起源心室頻拍(ベラパミル感受性心室頻拍)(図5-6-28):
心室頻拍時のQRS波が右脚ブロック+左軸偏位を示す場合は左脚後枝Purkinjeネットワーク内のCaチャネル依存性組織の異常緩徐伝導部を必須伝導路とするリエントリー機序が考えられ,ベラパミルが有効である.右脚ブロック+右軸偏位を示す場合もあり,このときは左脚前枝Purkinjeネットワーク内のリエントリーと考えられる.
3)カテコールアミン誘発性多形性心室頻拍:
運動により誘発される多形性心室頻拍で失神発作や突然死を惹起する小児に認められ約25%で家族歴を有し,リアノジン受容体の遺伝子異常が原因と考えられている.
4) QT延長症候群【⇨5-5-4】:
QT時間延長(QTc≧0.45秒)を伴い(図5-6-29),torsade de pointes型心室頻拍を生じ,失神発作ないし突然死をきたす(図5-6-25).QT延長症候群は先天性と後天性に大別され,先天性には先天性聾唖を有するJervel-Lange-Nielsen症候群と聾唖を認めないRomano-Ward症候群などがある.それぞれ原因遺伝子とイオンチャネル異常によって細分類されるが,外向きK電流(IKs,IKr)の減少,または内向きNa電流(INa)の増加などのイオンチャネルの機能異常によって活動電位持続時間およびQT時聞が延長する.そのためイオンチャネル病という名前が提唱されている.後天性QT延長症候群の原因として,最も多い薬剤は抗不整脈薬であり,その他抗菌薬,抗真菌薬,三環系抗うつ薬,抗アレルギー薬などもその原因となる.ほかに徐脈(完全房室ブロック,洞不全症候群),電解質異常(低カリウム血症,低マグネシウム血症),中枢神経疾患によることもある.
5) Brugada症候群【⇨5-5-3)】:
1992年にBrugadaにより報告されたことから,この名前がある.日本人を含めたアジア人種に多く,30~60歳代の成人男子が圧倒的に多い.Naチャネルの遺伝子であるSCN5aの遺伝子異常によりNaチャネルの機能異常が生じることがその原因であると考えられ,約25%の例で遺伝的発症を認める.V1~V2の右側胸部誘導でrSr型QRSとST部分の上昇を認め(図5-6-30),ポックリ病や夜間突然死症候群との関連が注目されており,特に突然死生還例の予後は不良である.しかし,最近の研究では,心電図では特徴的な所見を認めるが,一度も心停止や失神の既往を有しない無症候性Brugada症候群では生命予後が良好であるとの報告もなされ,無症候例ではその取り扱いは,いまだ議論の域を出ない.
6)催不整脈性右室異形成/
心筋症(arrhythmogenic right ventricular dysplasia/cardiomyopathy:ARVD/C):
催不整脈性右室心筋症は臨床的には右心室に起源を有する心室頻拍による症状を主症状とし,病理組織学的には右心室優位の心筋細胞の変性・脱落と線維脂肪組織(fibro-fatty tissue)による置換を示す臨床的症候群である.洞調律時にV1誘導に遅延電位(ε波)と陰性T波を認める(図5-6-31).心室頻拍波形は右室起源で左脚ブロック型で,好発部位は右室流入路,右室流出路,右室心尖部である.
治療
心室頻拍の治療は頻拍発作停止治療と頻拍発作予防治療,さらに頻拍による突然死予防治療に大別される(図5-6-32).
1)頻拍発作停止治療:
抗不整脈薬,カルディオバージョンおよび心臓ペーシングがあるが,通常は容易に血行動態が破綻するため,緊急の停止を要する.すでに血行動態の悪化を認める場合には速やかに体外式電気的除細動器によるカルディオバージョン(QRS波同期の電気ショック)を行う.血行動態がある程度安定している場合には抗不整脈薬治療を考慮するが,第一選択薬としてVaughan Williams分類Ⅲ群薬であるアミオダロンあるいはニフェカラントを静脈内投与する.Ⅰ群薬であるリドカインやプロカインアミド,β遮断薬も有効例がある.特殊なものとして,右脚ブロックと左軸偏位を示すベラパミル感受性特発性左室心室頻拍の場合にはⅣ群薬のベラパミルが有効である.先天性QT延長症候群に対してはβ遮断薬,マグネシウム,メキシレチン,イソプロテレノール,心臓ペーシングなどが有効な症例があるが,血行動態が安定していても持続する場合はできるだけ早期にカルディオバージョンを行う.
2)頻拍発作予防治療:
抗不整脈薬,カテーテルアブレーション,手術治療がある.
a)抗不整脈治療:基礎心疾患のない場合はⅠa群の薬剤,運動や情動によって誘発される場合にはⅡ群薬(β遮断薬)が有効である.ベラパミル感受性VTに対してはⅣ群薬,特にベラパミルが有効である.先天性QT延長症候群ではβ遮断薬が有効である.Brugada症候群では心室性不整脈が持続する緊急時には,カテコールアミンの少量投与が効果的であり,発作予防にはキニジンなどが試みられているが確実な治療法として確立されていない.基礎心疾患を有し,特に心機能低下を伴う心室頻拍に対してはCASTの報告以降Ⅰ群薬は禁忌となり,Ⅲ群薬,特にアミオダロンが用いられ有効性が報告されている.
b)カテーテルアブレーション:静脈ないし動脈から挿入したカテーテル先端の電極を介して高周波通電を行い,心室頻拍の起源やリエントリー回路内必須伝導路を焼灼することで,ベラパミル感受性左室起源特発性心室頻拍および右室流出路起源心室頻拍に対しては90%以上の高い成功率が得られ,特発性心室頻拍においては根治療法ととらえられている.一方,陳旧性心筋梗塞や拡張型心筋症,催不整脈性右室異形成/心筋症など基礎心疾患を有する心室頻拍ではリエントリー回路の焼灼に限界があり,成功率はいまだに低く再発率も高い.近年3Dマッピングによるelectro-anatomical mapping(電気-解剖的マッピング)の手法が考案され,さらに最近では心外膜穿刺法による心外膜アブレーションなどの導入によりその治療成績は改善している.
c)手術治療:心室額拍の起源を同定し,心内膜切除,心筋切除,心内膜凍結凝固などを行う.カテーテルアブレーション再発例,心筋梗塞後の心室瘤合併例などがその適応となる.
3)頻拍による突然死予防:
基礎心疾患に伴う持続性心室頻拍に対する薬物・非薬物療法は頻拍の徐拍化や発作頻度の抑制が治療の主体であり,突然死予防には限界がある.最終的には植え込み型除細動器(経静脈的に心内に挿入された電極により心室頻拍/心室細動を感知し自動的に作動する植え込み型除細動器)植え込みの適応となる.特に心機能低下例や血行動態の破綻をきたす心室頻拍例では第一選択治療となる.現在用いられている除細動器はあらゆる心室頻拍に対応可能であり,レートの遅い心室頻拍に対しては抗頻拍ペーシングにより停止可能で,レートの速い心室頻拍に対してはカルディオバージョンによる停止が可能で,最終的には直流除細動による治療がなされる(図5-6-33).心停止発作既往例に対する心停止発作の二次予防には,植え込み型除細動器(ICD)の植え込みが必須である(一次予防).[青沼和隆]
■文献
笠貫 宏:心室性不整脈.内科学 第九版(杉本恒明,矢崎義雄編),pp472-480,朝倉書店,東京,2007.
出典 内科学 第10版内科学 第10版について 情報