内科学 第10版 「慢性合併症」の解説
慢性合併症(糖尿病)
定義・概念
現在,糖尿病の治療目標は,「健康な人と変わらない日常生活の質(QOL)の維持,健康な人と変わらない寿命の確保」であり,このためには「糖尿病細小血管合併症(網膜症,腎症,神経障害)および動脈硬化性疾患(虚血性心疾患,脳血管障害,閉塞性動脈硬化症)の発症,進展の阻止」が重要とされている.この目標達成に向けて「血糖,体重,血圧,血清脂質の良好なコントロール状態の維持」を行うことが糖尿病の治療である.
すなわち,糖尿病は「合併症の病気」といっても過言ではない.合併症は,糖尿病発症後一定期間の後に発症するが,糖尿病状態すなわち高血糖の持続が最も重要な成因であり,特に細小血管症は糖尿病に特異的な合併症である.これらの慢性合併症が,糖尿病症例の予後を規定している.
分類
糖尿病の慢性合併症は基本的に血管障害であり,障害される血管の太さにより細小血管症(microangiopathy)と大血管症(macroangiopathy)に分類される(表13-2-15).細小血管症には網膜症・腎症・神経障害(神経症とはよばない)が含まれ,これらは糖尿病の3大合併症(triopathy)ともよばれている.前述のように,細小血管症は糖尿病に特異的であり,基本的に糖尿病が存在しないと発症しない. 一方,大血管症は動脈硬化症であり,糖尿病は高血圧・脂質異常症と並んで,重要な危険因子の1つである.動脈硬化症は,糖尿病がなくても発症するが,軽度の血糖値の上昇(耐糖能障害)の段階から,その危険因子となる.当然,全身の動脈が障害されるが,イベントとしては,脳卒中・心筋梗塞・閉塞性動脈硬化症がその典型である. ほかに,足病変は神経障害と血流障害の複合により生ずるが,上記とは分けて記載されることが多い.また,歯周病も糖尿病の慢性合併症の1つと解されている.骨病変も存在し,糖尿病性骨症とよばれることもある.さらに最近では,ある種の悪性腫瘍や認知症が糖尿病症例に高頻度で認められることも報告されているが,これらを糖尿病の慢性合併症とよんでいいのかはいまだ確定していない.
a.細小血管症
共通の成因
細小血管症の最も重要な成因は「高血糖の持続」であり,このことは多くの臨床研究でも明らかにされている.ただし,おのおのの合併症の発症には,高血糖に起因する共通因子とともに各組織の局所因子も関連しており,この点に関しては各合併症の項に記載する.
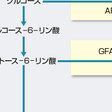
古くから,グルコースの取り込みがインスリンに依存しない組織に細小血管症が生ずることが指摘されており,血糖値の上昇に伴ってグルコースがGLUT1により細胞内に取り込まれ,種々の代謝異常を引き起こすと考えられている.実際には過剰に取り込まれたグルコースが,図13-2-27に示す種々の解糖系の側副路に流入し代謝異常を引き起こす.これらの代謝異常が細胞の機能障害を惹起し,細小血管症に至ると考えられている(Brownlee,2001;Calcuttら,2009).
1)ポリオール経路:
グルコースから直接分かれ,ソルビトール・フルクトースが産生される経路である.律速酵素は,グルコースをソルビトールに変換するアルドース還元酵素である.高血糖状態ではこのポリオール経路が亢進し,細胞内にソルビトールが蓄積する.その結果,細胞内浸透圧の上昇や細胞内情報伝達に重要なミオイノシトールが低下し,細胞障害が惹起されると考えられている.また,補酵素であるNADPHの減少は酸化ストレスの増加とも関連するとされている.さらに,ソルビトールからフルクトースへの経路の補酵素はNAD+であり,この経路が亢進して生ずるNADPが後述のジアシルグリセロール産生経路の補酵素として用いられる.また,生じたフルクトースは非酵素的糖化を惹起する.すでに,アルドース還元酵素阻害薬が開発され,神経障害の治療薬として用いられている.
2)ヘキソサミン経路:
フルクトース-6-リン酸から,グルコサミン-6-リン酸を経て,UDP-N-acetylglucosamine(UDP-GluNAc)が産生される経路である.細胞内リン酸化シグナルの抑制を惹起すると考えられている.残念ながらヒトに応用可能な阻害薬が開発されていないため,その解明も遅れている.
3)ジアシルグリセロール(DAG)産生経路とPKC活性化:
グルコースからグリセルアルデヒド-3-リン酸を経て,ジアシルグリセロール(DAG)がde novoに産生されること,産生されたDAGがプロテインキナーゼC(PKC)を活性化することが,特に高血糖状態にさらされた血管細胞で生ずることが証明され,血管合併症の成因の1つとして注目されている.PKCには種々のアイソザイムが存在するが,糖尿病状態の血管では特にPKC-βが活性化され,種々の細胞機能異常を惹起することが報告されている.すでに,PKC-β阻害薬が開発され,糖尿病動物では種々の血管合併症に有効であることが示されている.しかし,ヒトではいまだ臨床試験が進行しており,治療薬としての臨床応用には至っていない.
4)終末糖化産物(AGE)産生経路:
グルコースが種々の体内構成蛋白を非酵素的に糖化することは,古くから知られていた.初期反応で生ずる物質はアマドリ化合物とよばれており,HbA1cはその1つである.半減期の長い蛋白ではその後の後期反応(Maillard反応)が進行し,終末糖化産物(advanced glycation end-products:AGEs)が形成される.グルコース以外にも,フルクトースやメチルグリオキサールなどがAGEを形成する.AGEが形成されると,その蛋白の分解・機能の低下により細胞機能障害を惹起する.また,AGEには受容体(receptor for AGEs:RAGE)が存在し,RAGEを介する細胞機能障害も想定されている.AGE産生阻害薬,RAGE拮抗薬などが開発されているが,現時点では臨床応用には至っていない.
5)酸化ストレスの亢進:
糖尿病では,酸化ストレス消去系酵素の活性低下,産生系であるNAD(P)H oxidaseの活性化,ミトコンドリアからの活性酸素産生増加,などにより,酸化ストレスが亢進する.酸化ストレスの亢進は,細小血管症のみならず大血管症にも関連しており,共通の成因の1つと考えられている.しかし,多くの抗酸化薬が存在するにもかかわらず,ヒトの糖尿病性血管合併症に対する有効性が証明された抗酸化薬がないことが問題点の1つである.
ⅰ)網膜症
概念・成因
網膜症は,眼底の血管を観察して診断するため,腎症や神経障害に比べて特異性が高く,糖尿病の診断基準にも取り入れられている.網膜症の成因としては,共通因子以外に,局所の血管内皮増殖因子(VEGF)産生増加の関与が示されている.
疫学
Japan Diabetes Complications Study(JDCS)は,1996(平成8)年にスタートし現在も継続中の,日本人2型糖尿病症例を対象とした大規模臨床試験である.その平成20年度総括研究報告書によると,網膜症の発症は1000人年あたり37.4,進展は1000人年あたり8.3であるとされている.また,網膜症の発症に関与する因子(多変量解析)は,糖尿病罹病期間,HbA1c,BMIであり,進展に関与する因子はHbA1cである.HbA1c値1%の増加により,網膜症の発症・進展は約1.3~1.4倍となる. 網膜症は従来,成人中途失明の原因疾患の第1位であった.しかし,平成17年度に発表された,「わが国における視覚障害の現状」では,視覚障害の主原因疾患は,緑内障20.7%,糖尿病網膜症19.0%,網膜色素変性症13.7%,黄斑変性症9.1%,高度近視7.8%であり,糖尿病網膜症は第2位となった.しかし,緑内障の一部には糖尿病に起因するものが含まれると考えられ,糖尿病眼病変による視覚障害は依然第1位とも考えられる.
分類・臨床症状・検査成績
網膜症は眼底検査で診断する.通常,以下の4段階に分類される.①網膜症なし,②単純糖尿病網膜症(simple diabetic retinopathy:SDR,図13-2-28):毛細血管瘤,点状・斑状出血,火焔状出血,硬性白斑,少数の軟性白斑を認める,③増殖前糖尿病網膜症(preproliferative diabetic retinopathy:PPDR,図13-2-29):多発する軟性白斑,網膜内細小血管異常(intraretinal microvascular abnormality:IRMA),静脈異常,無灌流域(蛍光眼底)を認める,④増殖糖尿病網膜症(proliferative diabetic retinopathy:PDR,図13-2-30):新生血管,硝子体出血,線維血管性増殖組織,牽引性網膜剥離,などを認める.単純網膜症では症状はなく,増殖前網膜症でも症状がないことが多い.ただし,黄斑浮腫を伴うと視力低下が生ずる.したがって,定期的な眼底検査(眼科受診)がきわめて重要である.
治療・管理
1)一般的管理事項
: 前述のように,初期には症状がないため,眼底検査が必須である.血糖コントロールが不良な場合,血糖値を急激に低下させると網膜症が悪化する場合もあり,初診時には必ず眼科医による眼底検査を行う.以後の眼科受診の頻度は,眼底所見によって異なるため,眼科医との緊密な連携が必要である.
2)内科的治療
: 最も重要な治療は血糖コントロールである.このことは,すでに多くの臨床研究で明らかにされている.わが国で行われたKumamoto Studyでは,HbA1c(NGSP)<6.9%,空腹時血糖値<110 mg/dL,食後2時間血糖値<180 mg/dL,では,網膜症・腎症の発症・進行を認めなかったことが示されており,この数字が現在の血糖コントロール目標と考えられる.
高血圧を合併した場合の血圧コントロール,および脂質異常症を合併した場合の血清脂質の管理も重要であることはいうまでもない.
3)眼科的治療
: 増殖前網膜症以降では,眼科的治療が必要である.光凝固療法および硝子体手術が該当する.光凝固療法の目標は,増殖網膜症への進行阻止および黄斑浮腫による視力低下阻止である.硝子体手術の目的は,混濁した硝子体の除去・増殖膜の切除と牽引の解除・牽引剥離された網膜の復位,などである.また,近年,黄斑浮腫に対してステロイド局所療法や抗VEGF抗体の硝子体内投与が試みられるようになってきている.
ⅱ)腎症
概念・成因
腎症は微量アルブミン尿の出現で発症し,持続性蛋白尿・慢性腎不全へと進行する連続性の経過をたどる疾患である.
腎症の成因には,高血糖の持続に基づく共通因子とともに,局所因子として糸球体高血圧があげられる(Calcutt,2009).糸球体高血圧は腎臓内血行動態異常,特に輸入細動脈系の拡張に起因する.高血圧が合併すると糸球体高血圧はより助長される.また,細小血管症のなかでは,腎症が最も遺伝因子の影響を受けやすいとされている.現在,腎症疾患感受性遺伝子の解析が全世界で精力的に行われているが,現時点ではその同定には至っていない.
疫学
前述のJDCSでは,腎症の発症(微量アルブミン尿の出現)・進行(顕性蛋白尿の出現)は1000人年あたり7であると報告されている.腎症は,1998年から慢性透析療法導入原疾患の第1位であり,2010年には,16225例で全体の43.7%を占めるに至っている.
分類
腎症は上記のように連続性の経過をたどる疾患であるが,進行の程度に従い治療法が若干異なるため,病期分類が作成されている(表13-2-16).
1)第1期(腎症前期):
尿中アルブミン排泄量が正常で,現在の臨床検査では腎症の存在を診断できない病期である.しかし,この病期にも糸球体病変が存在する症例が報告されており,以下に述べる微量アルブミン尿より早期に腎症を診断できる指標の開発が望まれている.
2)第2期(早期腎症期):
微量アルブミン尿を呈する病期である(診断基準は後述する).腎機能(GFR)は通常正常範囲にある.本病期は種々の治療に対する反応性が良好であり,寛解(第1期への改善)も可能である.
3)第3期(顕性腎症期):
持続性蛋白尿(顕性蛋白尿)が出現する病期である.尿蛋白は試験紙法で持続的に陽性となるが,正確には定量して診断を下す.本病期は尿蛋白量と腎機能から前期(A)と後期(B)に分けられており,尿蛋白1.0 g/日以上,またはクレアチニンクリアランス(CCr)60 mL/分以下が後期に分類される.
4)第4期(腎不全期):
診断および病態はほかの腎疾患による慢性腎不全と同様である.ただ,糖尿病性腎症の場合,末期まで大量の蛋白尿が続くことが多く,溢水が透析療法導入の理由となることが多い.
5)第5期(透析療法期):
透析療法導入以降がこの病期に相当する.糖尿病性腎症の治療という観点からはこの病期はすでにエンドポイントに達しているが,糖尿病性腎症から透析療法に導入された症例の生命予後がきわめて不良であることから,この病期が設定されたと解される.本病期における,生命予後を改善させる治療法の開発が求められている.
臨床症状
顕性腎症後期までは,臨床症状・身体所見ともに出現しないのが通常である.顕性腎症後期に至り,蛋白尿が増加すると,浮腫を含む体液貯留の所見が出現する.慢性腎不全に進行した場合の臨床症状・所見は,ほかの腎疾患による慢性腎不全と同様である.
検査成績・診断
尿検査と血液検査が主体であり,まずすべての糖尿病症例で一般検尿を行う.蛋白尿が陰性もしくは軽度陽性(1+程度)の場合に,尿中アルブミン排泄量を測定する.この値が下記の基準値をこえている場合を微量アルブミン尿とよんでいる.進行すると尿蛋白が試験紙法で持続的に陽性となる.血液検査では特徴的な異常は存在しない.最も重要な血液検査は血清クレアチニン値であり,GFRをCCrで代用するか,あるいは血清クレアチニン値から推算式により算出して評価する.
腎症の早期診断には微量アルブミン尿の検出が必須である.表13-2-17に糖尿病性腎症早期診断基準を示す(猪股,2005).前述のように,尿蛋白陰性あるいは軽度陽性(1+程度)の糖尿病症例で,尿アルブミン濃度と尿クレアチニン(Cr)濃度を同時に測定し,その比を計算する.3回測定中2回の尿アルブミン値が,クレアチニン補正値で表13-2-16の基準値の範囲内にある場合,微量アルブミン尿と診断する.
鑑別診断
微量アルブミン尿と診断した場合,種々の疾患(糸球体腎炎,高血圧(良性腎硬化症),高度肥満,メタボリック症候群,尿路系異常・尿路感染症,うっ血性心不全など)を鑑別したうえで,糖尿病性腎症と診断する.なお,鑑別にあたっては,ある程度以上の糖尿病罹病期間(約5年以上),ほかの糖尿病性合併症(網膜症,神経障害)の存在,高度の血尿を認めないこと,などが参考となる. 顕性腎症は尿アルブミン値が300 mg/gCr以上に増加した場合に診断する.尿蛋白を定量する場合の基準値は500 mg/gCr以上である.
治療
糖尿病性腎症の発症因子は高血糖の持続である.また,腎臓内血行動態異常により糸球体内静水圧の上昇(糸球体高血圧)が生じ,これが発症因子の1つと考えられている.ここに全身血圧の上昇(高血圧)が加わると,糸球体高血圧はより助長される.したがっておもな治療法は,高血糖の是正と糸球体高血圧の是正である.
1)高血糖の是正
: HbA1c(NGSP)6.9%未満を目標とする.薬剤の種類に現時点で差は認められていないが,腎不全に至ると大部分の経口血糖降下薬は禁忌とされている.
2)糸球体高血圧の是正:
レニン-アンジオテンシン系阻害薬(アンジオテンシン変換酵素阻害薬,アンジオテンシンⅡ受容体拮抗薬)が第一選択薬とされているが,同時に長時間作用型Ca拮抗薬や利尿薬を用いて,全身血圧を130/80 mmHg未満に低下させることを目標とする.レニン-アンジオテンシン系阻害薬は輸出細動脈を拡張させ,糸球体高血圧を是正すると考えられている.
ほかに,顕性腎症期以降ではマイルドな蛋白制限食が必要であり,また脂質異常症を呈する場合はその治療も必要である.
ⅲ)神経障害
概念・成因
糖尿病で生ずる神経障害は,末梢神経障害である.成因としては,末梢神経そのものに生ずる代謝異常と神経栄養血管に生ずる代謝異常が重要であり,これらは共通因子に起因している.ただし,共通因子のなかでも.神経そのものにはポリオール経路の亢進の寄与が大きく,神経栄養血管にはPKC活性化の寄与が大きいと考えられている.また,酸化ストレス亢進は両者に関与している.
疫学
一般的に,神経障害は,細小血管症のなかで最も頻度が高い合併症であると考えられている.しかし,簡易診断基準(後述)は存在するが,正確かつ定量的な診断基準ではないため,大規模な疫学調査は行われていない.日本内科医会が行った主治医の判断による有病率は,糖尿病症例12821例中,神経障害37%,網膜症23%,腎症14%と報告されている.
分類・臨床症状・検査成績
神経障害の分類はいくつか提唱されているが,表13-2-18には最もよく使用されている分類を提示する.基本的に,①四肢(下肢末端から始まる)に対称的に生じる多発神経障害(polyneuropathy):表13-2-18では対称性多発神経障害(symmetric polyneuropathy)の中の,感覚/自律神経障害(sensory/autonomic polyneuropathy)が該当する,と②非対称的に生ずる単神経障害(mononeuropathy):表13-2-18では,局所障害性および多巣性神経障害(focal and multifocal neuropathy)が,2大病型である.
簡易診断基準(表13-2-19)が作成され,広く用いられているが,そのなかに臨床症状および検査所見も記載されている.臨床症状は,両側性であること,足趾先および足底から始まることが重要であり,しびれ・疼痛・異常感覚が生ずる.診察では,アキレス腱反射の低下もしくは消失,および内踝の振動覚の低下が重要である.検査では神経伝導速度検査を行う. 自律神経障害も生じるが,自律神経は全身に分布しており,障害の出る部位によって症状が異なっている.症状がない場合は,心電図R-R間隔の変動係数(CV)の低下,起立による血圧低下を検査する.
単神経障害では,外眼筋麻痺や顔面神経麻痺を生ずる.
治療
網膜症・腎症と同様に,血糖コントロールが最も重要である.また,高血圧合併例では血圧コントロールが,脂質異常症合併例では血清脂質の管理が重要であることはいうまでもない.
細小血管症の成因の共通因子のなかで,ポリオール経路の亢進が特に神経障害に関連していると考えられており,アルドース還元酵素阻害薬(エパルレスタット)が治療薬として使用されている.神経障害,特に有痛性神経障害に対しては,対症療法が行われる.非ステロイド系抗炎症薬,三環系抗うつ薬,抗不整脈薬(メキシレチン)などとともに,最近ではプレガバリンやデュロキセチンも用いられるが,治療に難渋する症例が多い.
b.大血管症
概念・成因
基本的に動脈硬化症であり,糖尿病は高血圧・脂質異常症と並んで,重要な危険因子である.したがって,糖尿病に特異性は少ない.成因は,細小血管症の共通因子に加え,動脈硬化症本来の成因が複雑に関係している.
分類
表13-2-15に示したように,脳血管障害,虚血性心疾患,末梢血管障害に分類される.脳血管障害では,アテローム血栓性脳梗塞とラクナ梗塞が多い.
疫学
日本人糖尿病症例の死因は,第1位が悪性腫瘍,第2位が血管障害,第3位が感染症である.血管障害では,心筋梗塞と脳卒中がほぼ同率であり,脳卒中では脳梗塞が多い.JDCSの報告では,冠動脈疾患および脳卒中の年間発生率は,1000人年あたり,それぞれ9.6,7.9であるとされている.また,糖尿病症例での冠動脈疾患の危険因子は,LDLコレステロール,中性脂肪,HbA1cであり,脳卒中の危険因子は,収縮期血圧である.
臨床症状・検査成績・治療
これらに関しては,それぞれの項を参照していただきたい.
治療の基本は,細小血管症と同様,血糖コントロール・血圧コントロール.血清脂質のコントロールであり,これらを強力に行う(集約的治療)ことにより,心血管イベントが有意に減少することが示されている.ただし,細小血管症とは異なり,厳格な血糖コントロール単独の有効性は示されていない.
c.その他
種々の合併症が存在するが,ここでは足病変と歯周病に関して記載する.
ⅰ)足病変
足病変は,足の皮膚障害や軽微な外傷から潰瘍形成・壊疽へと進行する病変であり,切断に至る症例も存在する.基本的に,神経障害と血流障害の両者に起因しているが,進行過程には細菌感染症も関連している. まず,予防が大切であり,足の観察およびフットケアが重要である.
ⅱ)歯周病
歯周病は,歯肉炎と歯周炎の総称である.歯肉炎は炎症が歯肉に限局している場合である.歯周炎は,歯と歯肉の接合部に存在する歯肉溝へ,Gram陰性桿菌などの細菌感染が起きることによって惹起される炎症性疾患である.糖尿病症例で歯周病の合併が多いこと,および歯周病が合併すると血糖コントロールが悪化することが示されている.[羽田勝計]
■文献
Brownlee M: Biochemistry and molecular cell biology of diabetic complications. Nature, 414: 813-820, 2001.
Calcutt NA, Cooper ME, et al: Therapies for hyperglycemia-induced diabetic complications: from animal models to clinical trials. Nature Reviews Drug Discovery, 8: 417-429, 2009.
Thomas PK: Classification, differential diagnosis, and staging of diabetic peripheral neuropathy. Diabetes, 46(Suppl 2): S54-S57, 1997.
出典 内科学 第10版内科学 第10版について 情報