精選版 日本国語大辞典 「平均自由行路」の意味・読み・例文・類語
へいきん‐じゆうこうろ‥ジイウカウロ【平均自由行路】
改訂新版 世界大百科事典 「平均自由行路」の意味・わかりやすい解説
平均自由行路 (へいきんじゆうこうろ)
mean free path
気体,液体中の分子や金属中の自由電子が他の粒子と衝突しないで自由に動ける平均的な距離。平均自由行程ともいう。平均自由行路の考え方を最初に導入したのはドイツのR.クラウジウスである。一般に,粒子が他の粒子と衝突した瞬間から,次の衝突が起こるまでに動ける距離を自由行路という。自由行路の値は,個々の粒子によって異なり,ある種の統計的分布を示す。自由行路を粒子全体に対して平均したものが平均自由行路である。粒子が平均自由行路だけ進むと,平均的に1回衝突が起こると考えてよい。
気体分子を直径Dの球と考え,平均自由行路lを見積もってみよう。分子の速度ベクトルをvとすれば,図からわかるように,分子が運動するとき,半径Dの円を底としvの方向に伸びた円筒中に他の分子の中心が入っていると衝突が起こる。分子がlだけ進むと平均して1回の衝突が起こるから,高さlの円筒中に平均として分子が1個存在するであろう。単位体積中の分子数をnとすれば,上述の円筒中の分子数はπD2lnと表されるから,πD2ln≅1,すなわち平均自由行路lは,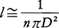 で与えられる。以上述べたことは,電子と金属イオンとの衝突に拡張することもできる。電子を質点とみなし,また金属イオンを半径Rの球と考えれば,電子の平均自由行路は,
で与えられる。以上述べたことは,電子と金属イオンとの衝突に拡張することもできる。電子を質点とみなし,また金属イオンを半径Rの球と考えれば,電子の平均自由行路は,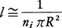 と表される。ただし,niは単位体積中の金属イオンの数である。
と表される。ただし,niは単位体積中の金属イオンの数である。
気体の場合,0℃,1気圧における気体分子の平均自由行路は10⁻5cmの程度である。気体の粘性率,熱伝導度,拡散係数などは平均自由行路によって表される。
執筆者:阿部 龍蔵
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
百科事典マイペディア 「平均自由行路」の意味・わかりやすい解説
平均自由行路【へいきんじゆうこうろ】
出典 株式会社平凡社百科事典マイペディアについて 情報
世界大百科事典(旧版)内の平均自由行路の言及
【統計力学】より
…気体内の分子が毎秒数百mの平均速度で器壁間を往復するとすれば,室内のタバコの煙がゆっくり拡散するという日常生活の経験事実に反する。この異論に答えてクラウジウスは平均自由行路の概念を導入した(1858)。分子の飛行経路を曲げる分子間衝突を無視する計算が正しいのは,分子の平均自由行路λが分子間力の有効半径aに比べて十分に長い場合であるが,λは日常生活の尺度から見れば非常に短いために拡散は遅いのである。…
※「平均自由行路」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...


