内科学 第10版 「Sjögren症候群」の解説
Sjögren症候群(リウマチ性疾患)
Sjögren症候群(Sjögren’s syndrome:SS)は,慢性唾液腺炎と乾燥性角結膜炎を主徴とし,多彩な自己抗体の出現や高ガンマグロブリン血症をきたす自己免疫疾患の1つである.唾液腺,涙腺において腺房の破壊,萎縮による乾燥症(sicca syndrome)を主症状とするが,全身の外分泌腺も系統的に障害されるため,自己免疫性外分泌腺症(autoimmune exocrinopathy)とも称される.
分類
SSはほかの膠原病の合併がみられない一次性(primary)SSと関節リウマチ(RA)や全身性エリテマトーデス(systemic lupus erythematosus:SLE)などの膠原病を合併する二次性(secondary)SSとに大別される.
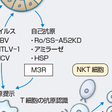
原因・病因,病態(図10-3-1)
SSの発症機序は,当初,抗原特異的免疫応答が関与し,続いて抗原非特異的免疫応答が関与していると考えられる(藤林ら,1999;Fujibayashiら,2004).経時的に,①先行因子,②炎症の誘導期,③炎症の慢性期,④唾液腺破壊期と進行する.先行因子は不明であるが,細菌やウイルスなどの感染症が引き金となり一部の唾液腺組織が壊れることで炎症が誘導される.その結果,壊れた細胞よりさまざまな自己抗原(ムスカリン作働性アセチルコリン受容体,熱ショック蛋白など)が流出し,プロフェッショナルな抗原提示細胞や唾液腺上皮細胞などに抗原ペプチドが提示され,抗原特異的なT細胞が活性化される.活性化されたT細胞はIL-2などのサイトカインを産生しポリクローナルなT細胞の増殖を惹起する.一方,産生されたIL-6などによりポリクローナルなB細胞の活性化が誘導され,自己抗体産生やリンパ増殖性病態を引き起こす.最終的には,IFN-γやIL-17などの炎症性サイトカインにより炎症は増幅され,細胞傷害性T細胞も誘導される.CD4+細胞傷害性T細胞はFasリガンドを介して,CD8+細胞傷害性T細胞はパーフォリン,グランザイムを介して,唾液腺上皮細胞をアポトーシスに陥らせる.このような流れにより唾液腺炎,唾液腺破壊が惹起されると考えられている.
疫学
2010年度の厚労省特定疾患自己免疫疾患調査研究班の疫学調査結果では,Sjögren症候群患者総数は66000人であることが明らかにされた.一方,欧米では日本の有病率の10倍であり,関節リウマチ患者数と同等である.男女比は1:17で女性に圧倒的に多く,発症年齢のピークは40〜60歳代である.
病理(図10-3-2)
病理学的には,唾液腺や涙腺の導管,腺房周囲の著しいリンパ球(T細胞およびB細胞)浸潤,線維化,上皮腺炎が特徴とされる.
臨床症状
1)自覚症状:
ドライマウスおよびドライアイがあれば本症を疑う. a)ドライマウス:自覚症状は,口腔内乾燥感,唾液の粘稠感,口腔内灼熱感,飲水切望感,夜間の口腔内疼痛,味覚異常,食物摂取困難,などである.他覚所見は,口腔内乾燥,口腔内発赤,舌乳頭萎縮,歯牙,口腔汚染,口角びらん,齲歯の多発,歯肉炎・歯周炎,耳下腺・顎下腺の腫脹などである. b)ドライアイ:自覚症状としては,涙が出ない,目がごろつく,目が熱い,目が疲れる,目が充血する,目がかすむ,まぶしい,悲しいときに涙が出ない,などである.他覚所見は,眼科的に乾燥性角結膜炎がみられる.
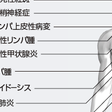
2)他覚症状:
全身の臓器に多彩な臨床症状を生じる(図10-3-3). a)発熱:10〜30%のSS患者に発熱が認められるが,37℃台の微熱であることが多い. b)血液・リンパ球異常:骨髄病変に伴う症状として,貧血(30〜60%),白血球減少(おもにリンパ球減少)(30〜60%),血小板減少(10%)がみられる.多クローン性高ガンマグロブリン血症(60〜80%)やクリオグロブリン血症(5〜10%)による紫斑がみられることがある.全身のリンパ節腫脹(偽性リンパ腫)が約30%でみられる.悪性リンパ腫の発生頻度は健常人の40〜80倍と報告されている.おもにB細胞リンパ腫であり,MALT(mucosa-associated lymphoid tissue)リンパ腫の出現も報告されている. c)関節・筋:全身の関節痛,関節腫脹(30〜60%)は,関節リウマチの早期症状との鑑別が難しいことがある.血清学的にはリウマトイド因子(70%),抗核抗体(80〜90%)が陽性であり関節リウマチと共通点があるが,抗CCP抗体が陽性となる頻度は低い.
筋痛,筋力低下,筋脱力感などが認められることがあるが,頻度は高くない.筋脱力感の原因として,間質性腎炎に起因する尿細管性アシドーシスによる低カリウム血症性ミオパチーも念頭に入れるべきである. d)皮膚:環状紅斑(20%),Raynaud現象(20〜30%),高ガンマグロブリン血症に伴う紫斑(15%),凍瘡・凍瘡様皮疹,日光過敏,浸潤性紅斑などがみられることがある.SSでは,複数の薬剤に対してアレルギーを起こすことが多く薬疹がでやすい. e)甲状腺:甲状腺に対する自己抗体(抗甲状腺ペルオキシダーゼ抗体あるいは抗ミクロソーム抗体,抗サイログロブリン抗体)の陽性率は,17〜36%である.びまん性甲状腺腫大とともに甲状腺自己抗体陽性であり慢性甲状腺炎(橋本病)と診断される症例の頻度は約25%である.甲状腺機能障害を伴う頻度はSSの7〜8%である. f)肺:間質性肺炎が20〜25%に合併する.症状は咳と呼吸困難である.CT画像上の分類では,NSIP(nonspecific interstitial pneumonia)パターンが60%であり,LIP(lymphoid interstitial pneumonia)パターンは少ない. g)心血管系:抗SS-A抗体,特にSS-A52kD蛋白に対する自己抗体陽性患者が妊娠した場合に,18〜24週齢の胎児に完全房室ブロックが生じる可能性があり(2〜5%),新生児の完全房室ブロックの頻度(0.005%)の約1000倍であることは注意を要する.出生後ただちにペースメーカ治療が必要となる重篤な症例もあり,予防,治療対策が必要となる. h)消化管:唾液腺分泌低下による嚥下障害や胸やけなどの食道炎症状もみられる.慢性萎縮性胃炎が約50%の症例で認められる.胃のMALTリンパ腫の発生頻度も高い.原発性胆汁性肝硬変症が5%前後,慢性膵炎は5〜20%に合併すると報告されている.近年,自己免疫性膵炎はSSの合併とは異なり,IgG4関連疾患としてとらえられるようになった.
i)腎:25%で尿所見異常,腎機能障害,尿細管性アシドーシスなどがみられる.間質性腎炎は15%に,糸球体腎炎は7.5%に認められる. j)神経系:末梢神経障害は10〜20%に認められ,感覚失調性ニューロパチー,有痛性感覚性ニューロパチー,多発性単神経炎,三叉神経炎の頻度が高い.中枢神経障害としては,多発性脳梗塞,横断性脊椎炎,多発性硬化症様症状がみられることがある.
検査成績
1)一般検査:
CRP陽性,赤沈値亢進,高ガンマグロブリン血症が60〜80%にみられる.特に,IgG,IgAが増加しており,またクリオグロブリン(IgM-IgG)も高率に検出される.貧血,白血球減少症は約30〜60%にみられる.10%以下で血小板減少症がみられ,その中には特発性血小板減少性紫斑病の合併もある.
2)免疫学的検査:
自己抗体としては抗核抗体が80〜90%に検出され,染色型は斑紋型(speckled pattern)が多い.抗Ro/SS-A抗体は50〜70%と本症において最も高頻度に出現する自己抗体である.同抗体はほかの膠原病にも検出されるため,特異性は抗La/SS-B抗体より低い.抗La/SS-B抗体は,20〜30%に見い出され本症に特異性が高く診断意義が高い.本抗体陽性例は常に抗Ro/SS-A抗体も陽性である.リウマトイド因子は約70%の症例で認められる.
3)特殊検査:
a)小唾液腺,涙腺生検:口唇の小唾液腺および涙腺生検は診断に有用である.陽性所見は,小唾液腺組織で4 mm2あたり1focus(導管周囲に50個以上のリンパ球浸潤)以上認められることである(Greenspanらの基準ではグレード3と4). b)唾液腺造影(sialography):造影剤をStenon管より注入し耳下腺を造影する方法である.Rubin and Holtの分類でステージⅠ(直径1 mm未満の小点状陰影)以上を陽性とする(図10-3-4). c)唾液腺シンチグラフィ:99mTcO4を用いた唾液腺のRI検査.軽症例では耳下腺,顎下腺への集積が著明にみられるが,高度の唾液腺障害例では,集積はほとんどみられない.
4)眼科的検査:
a)Schirmer試験:涙液量を測定する方法でWhatman濾紙を下眼瞼耳側に5分間かけておき,5 mm以下の涙液分泌を陽性としている. b)ローズベンガル染色,リサミングリーン染色,蛍光色素染色:乾燥性角結膜炎の存在を検討するための生体染色検査である.ローズベンガル液,リサミングリーン染色液,蛍光色素液を点眼し,細隙灯顕微鏡で検査する.眼裂部およびそれより下方球結膜の染色(ローズベンガル試験ではvan Bijsterveldスコアが3以上)があれば陽性所見とする(図10-3-5).
診断
SSはいくつかの特徴的な症状を呈するために,診断基準が設けられている.おもな診断基準は,旧厚生省の改訂診断基準(1999年),アメリカ・ヨーロッパ改訂分類基準(2002年),国際登録ネットワーク診断基準(SICCA,2012年)である.現時点では,日本における唯一の公式な診断基準は旧厚生省改訂基準である(表10-3-1)(藤林ら,1999;Fujibayashiら,2004).
鑑別診断
鑑別すべき疾患として,ほかの膠原病(特に関節リウマチ,全身性エリテマトーデス)やIgG4関連Mikulicz病があげられる.SSの関節炎は,関節リウマチ(RA)と同様に朝のこわばりがあり両側性の関節痛を呈するが,こわばりの持続時間が短時間であり軟骨破壊・関節の変形をきたすような激しい関節炎は少ない.
ドライアイ,ドライマウスの症状・所見や抗SS-A抗体,抗SS-B抗体などの疾患特異的な自己抗体が鑑別診断に役立つ.両側の唾液腺腫脹や涙腺腫脹をきたしSSと臨床所見が類似しているIgG4関連Mikulicz病は,抗SS-A抗体,抗SS-B抗体がともに陰性であること,血清中IgG4が高値であることや唾液腺組織にIgG4陽性形質細胞浸潤が認められることなどから鑑別は容易である.
その他,ドライアイをきたす眼疾患やドライマウスを起こす,糖尿病,唾液腺萎縮症,薬剤の副作用,高年齢などが鑑別される.
合併症
慢性甲状腺炎(橋本病),原発性胆汁性肝硬変症,尿細管性アシドーシス,悪性リンパ腫などを合併することがある.
経過・予後
予後は比較的良好で10〜20年後に重症化する頻度は低く(5%),診断・治療の進歩により約20年前に比べて死亡例が1/8に減少している(0.4%).乾燥症状に限定したタイプは一般に予後良好であるが,全身症状を合併した場合は,活動性が高く予後の悪いことがある.特に,進行性の間質性肺炎,糸球体腎炎,自己免疫性肝炎,中枢神経障害,高粘度症候群などの合併により予後は大きく左右される.膠原病や悪性リンパ腫などの合併症(発症率は健常人に比して40〜80倍高い)には治療が必要である.さまざまなアレルギー反応を起こしやすい点に留意する.
治療・予防・リハビリテーション
治療は全身症状の有無により異なる.
一般に,腺症状だけの腺型SSでは,ドライアイやドライマウスに対しては,QOLの改善を目指した対症療法が治療の中心となる.多様な臓器病変に対しては,生命予後の改善を目指しステロイドや免疫抑制薬の適応となる.
1)QOLの改善を目指した治療:
a)ドライアイ:人工涙液が治療の中心.難治性の場合は,眼科専門医による涙点プラグを挿入する. b)ドライマウス:口腔乾燥症状に対してムスカリン作働性アセチルコリン受容体3(M3R)を刺激する2種類の薬剤(塩酸セビメリン,塩酸ピロカルピン)が保険適応となっている.
2)生命予後の改善を目指した治療:
a)活動性が低い場合:発熱,反復性唾液腺腫脹,リンパ節腫脹(偽性リンパ腫),関節症状などに対しては,プレドニゾロン換算で5〜15 mg/日を用いることで十分な効果が認められる. b)活動性が高い場合:①進行性の間質性肺炎,糸球体腎炎,自己免疫性肝炎,中枢神経障害,②高ガンマグロブリン血症やクリオグロブリン血症に伴う高粘度症候群,③膠原病を合併する場合,プレドニゾロン換算で30〜60 mg/日を投与する.免疫抑制薬(シクロホスファミド)も重症例では有効とされているが,腎毒性,悪性リンパ腫続発の危険性を考慮する必要がある. c)合併症の治療:慢性甲状腺炎,原発性胆汁性肝硬変症,尿細管性アシドーシス,悪性リンパ腫などを合併する場合,個々の治療が必要となる.[住田孝之]
■文献
住田孝之:厚生労働科学研究費補助金,難治性疾患克服研究事業自己免疫疾患に関する調査研究平成23年度,総括・分担研究報告書,p3-10, 2012.
藤林孝司,他:シェーグレン症候群改訂診断基準.厚生省特定疾患自己免疫疾患調査研究班,平成10年度研究報告書,135-138,1999.
Fujibayashi T, Sugai S, et al: Revised Japanese criteria for Sjögren’s syndrome (1999): availability and validity. Mod Rheumatol, 14: 425-434, 2004.
Sjögren症候群(膠原病・血管炎の腎障害)
Sjögren症候群は眼や口腔の乾燥症状を主症状とするが,関節症状のほかに間質性肺炎のような呼吸器障害,慢性膵炎,腎障害,末梢神経障害など多彩な内臓病変を呈する.一次性のものと全身性エリテマトーデスや関節リウマチに伴う二次性のものがある.合併した膠原病に伴うループス腎炎のような腎病変もあるが,Sjögren症候群自体に伴う腎病変が知られている.
a.尿細管間質性腎炎
Sjögren症候群では耳下腺など唾液腺にTリンパ球を主体とする細胞浸潤がみられるが,腎組織にも同様の細胞浸潤がみられる.間質に浸潤する細胞はCD4陽性のTリンパ球と形質細胞が主体であり,尿細管上皮内に浸潤して尿細管炎を引き起こす細胞はCD8 陽性のTリンパ球が主体である.慢性化すると間質は線維化をきたし尿細管上皮は萎縮する.すなわち尿細管間質性腎炎である(図11-6-9).尿中にはβ2-ミクログロブリン,α1-ミクログロブリンのような尿細管性蛋白尿が増加し,長期にわたると腎機能が低下してくる.Sjögren症候群による尿細管間質性腎炎では臨床的には尿細管性アシドーシスをきたすことが知られている.アニオンギャップ正常の高クロール性アシドーシスで,特に遠位尿細管からのH+イオン分泌が障害される遠位尿細管性アシドーシスが多い.塩化アンモニウム負荷試験で尿を酸性化することができない.症状としては低カリウム血症による四肢脱力,高カルシウム尿症による腎結石,尿濃縮力低下がある.近位尿細管にまで病変が及んで近位尿細管性アシドーシスをきたした場合はHCO3-再吸収が障害されるが,同時にアミノ酸,グルコース,リン酸の再吸収が障害され,ときにFanconi症候群を呈する.尿細管性アシドーシスの治療としてはカリウム,カルシウム補充,炭酸水素ナトリウム投与が行われる.
b.糸球体腎炎
Sjögren症候群自体に伴う膜性腎炎やメサンギウム増殖性腎炎がまれではあるが報告されている.[山田 明]
■文献
遠藤平仁:強皮症腎クリーゼ(SRC)高血圧性,非高血圧性.日臨免誌,23: 656-670,2000.
Helfrich DJ, et al: Normotensive renal crisis in systemic sclerosis. Arthritis Rheum, 32: 1128-1134, 1989.
Steen VD: Scleroderma renal crisis. Rheum Dis Clin North Am, 22: 861-878, 1996.
Sjögren症候群(膠原病にみられる肺病変)
SSは乾燥性角結膜炎と口腔内乾燥症を主症状とする自己免疫性外分泌障害が特徴である.ほかの膠原病の合併のない一次性SSと合併のある二次性SSに大別される.呼吸器系では,気道の乾燥と関連して気管支粘膜が萎縮,間質性肺炎は,NSIP所見,UIP所見,器質化肺炎(organizing pneumonia:OP)所見,リンパ球性間質性肺炎(lymphocytic interstitial pneumonia:LIP)所見が報告されている.このほか,細気管支病変(濾胞性細気管支炎)をはじめ,リンパ腫(5%程度,相対危険度40〜70倍),アミロイドーシス,囊胞性疾患も認められる.ステロイドや免疫抑制薬を含む治療への反応性は良好であるが,シクロホスファミドはリンパ腫発症の頻度を高める.[千田金吾]
出典 内科学 第10版内科学 第10版について 情報