改訂新版 世界大百科事典 「ラウールの法則」の意味・わかりやすい解説
ラウールの法則 (ラウールのほうそく)
Raoult's law
気-液平衡現象の一つである蒸気圧降下に関する古典的法則で,1888年にフランスの物理化学者ラウールFrançois Marie Raoult(1830-1901)が実験的に見いだした。それによると,不揮発性溶質Bを含む溶液中の溶媒Aの蒸気圧pA(溶液と平衡にある気相中の成分Aの分圧)と溶液の組成との間には次の関係が成立する。
(pA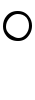 -pA)/pA
-pA)/pA =xB,またはpA=pA
=xB,またはpA=pA xA
xA
ここで,pA は純溶媒Aの蒸気圧,xAおよびxBはそれぞれ溶液中のAおよびB成分のモル分率である。この法則は,溶液中の溶質の濃度が十分に低く,溶質粒子間の相互作用を無視できるような場合(理想溶液)にはよく成立するが,溶液の濃度が高くなったり,気相の圧力が増大したりするにつれて,一般には法則からのずれが現れてくる。この法則が成立する条件下における蒸気圧の測定によって,不揮発性溶質の分子量を決定することができる。ラウールの法則は〈ヘンリーの法則〉と密接な関係をもっており,気-液平衡を溶媒側からみたのがラウールの法則,溶質側からみたのがヘンリーの法則ということができる。
は純溶媒Aの蒸気圧,xAおよびxBはそれぞれ溶液中のAおよびB成分のモル分率である。この法則は,溶液中の溶質の濃度が十分に低く,溶質粒子間の相互作用を無視できるような場合(理想溶液)にはよく成立するが,溶液の濃度が高くなったり,気相の圧力が増大したりするにつれて,一般には法則からのずれが現れてくる。この法則が成立する条件下における蒸気圧の測定によって,不揮発性溶質の分子量を決定することができる。ラウールの法則は〈ヘンリーの法則〉と密接な関係をもっており,気-液平衡を溶媒側からみたのがラウールの法則,溶質側からみたのがヘンリーの法則ということができる。
執筆者:玉虫 伶太
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「ラウールの法則」の意味・わかりやすい解説
ラウールの法則
らうーるのほうそく
Raoult's law
フランスのラウールが19世紀の終わりごろ実験的にみいだした法則。これは、のちにスウェーデンのアレニウス、オランダのファント・ホッフにより理論的にも理想溶液について証明された。希薄溶液では、溶媒n1モルに溶質n2モルを溶解したとき、その溶媒の蒸気圧p1と溶液の蒸気圧p2との間には、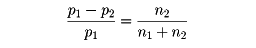
の関係がある、すなわち溶液の蒸気圧降下は溶液の溶質の濃度に比例するという法則。溶媒あるいは溶質のモル数nは、それぞれの質量wを分子量Mで割ったもの(n=w/M)であることから、蒸気圧降下を測定することによって溶質の分子量を決定することができる。蒸気圧降下は、浸透圧、凝固点降下、沸点上昇とも関係があり、いずれにしても、これらの測定により、この法則を用いて溶質の分子量が決定されている。
[中原勝儼]
ブリタニカ国際大百科事典 小項目事典 「ラウールの法則」の意味・わかりやすい解説
ラウールの法則
ラウールのほうそく
Raoult's law
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
最新 地学事典 「ラウールの法則」の解説
ラウールのほうそく
ラウールの法則
Raoult’s law
フランスの化学者F.M.Raoultによって1886年に見いだされた液体混合物の蒸気圧に関する法則。2種のAとBからなる液体混合物では,それぞれの純成分の蒸気圧をpA*・pB*,混合物中のモル分率をxA,1-xAとすると,全蒸気圧pは蒸気分圧pAとpBの和であるから,p=pA+pB=xApA*+(1-xA)pB*=pB*+(pA*-pB*)xAとなることをいう。このようなふるまいを示す液体を理想溶液という。
執筆者:吉田 尚弘
出典 平凡社「最新 地学事典」最新 地学事典について 情報
法則の辞典 「ラウールの法則」の解説
化学辞典 第2版 「ラウールの法則」の解説
ラウールの法則
ラウールノホウソク
Raoult's law
溶媒に溶質を溶解することによって生じる蒸気圧降下の大きさが,溶液中での溶質のモル分率に比例するという法則をいい,
p° - p = xp°
と表される.p°およびpは,それぞれ純溶媒およびこれに溶質が溶解したときの蒸気圧で,xはそのときの溶質のモル分率である.この関係を利用し,蒸気圧降下量から溶質の分子量を求めることがある.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「ラウールの法則」の意味・わかりやすい解説
ラウールの法則【ラウールのほうそく】
→関連項目溶液
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「ラウールの法則」の解説
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...