翻訳|phosphine
改訂新版 世界大百科事典 「ホスフィン」の意味・わかりやすい解説
ホスフィン
phosphine
リンの水素化物およびその水素をアルキル基またはアリール基で置換した化合物の総称。これらのうち水素化物(リン化水素)をホスフィンという場合が多い。
リン化水素
化学式PH3。無色の気体。有毒で,特有なにおいがある。融点-133℃,沸点-87℃。水に対する溶解度26ml/100mlH2O(17℃)。シクロヘキシルアルコールに溶けやすい。ジホスファンP2H4が混入すると常温でも自然発火する。白リン(黄リン)に水酸化カリウム水溶液を加え,60℃に熱すると,P2H4とともに気体として得られる。リン化カルシウムCa3Pと希酸,ヨウ化ホスホニウムPH4Iと水酸化カリウムとの反応,ホスホン酸H2PHO3の熱分解でも発生する。
アルキル,アリール置換ホスフィン
ヨウ化ホスホニウムとヨウ化アルキルとの反応,リン化カルシウムとハロゲン化アルキルの反応などで生成する。PH3の水素原子が置換される個数により,1個から第一ホスフィン,第二ホスフィン,第三ホスフィンと呼ぶ。また橋架け構造をもつジホスフィン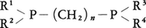 などもある。たとえば,ジエチルホスフィン(C2H5)2PHは沸点85℃,メチルジフェニルホスフィン(CH3)(C6H5)2Pは沸点284℃の無色の液体で特有の臭気があり,水に不溶,エチルアルコール,エーテルに易溶である。トリアルキルおよびアリールホスフィン類は,リン原子の空の3d電子軌道に遷移金属の電子の満たされたd軌道から電子を受け入れる(逆受容)能力が大きく,安定な各種の興味深い錯体をつくる。たとえば1963年バスカL.Vaskaによって初めて合成された[IrCl(CO)(PPh3)2]は,分子状酸素O2を可逆的に付加する。そのほか第三ホスフィンを配位子として含む遷移金属錯体は,水素,窒素分子,およびエチレンなどの各種オレフィンを可逆的または非可逆的に付加するものが多い。
などもある。たとえば,ジエチルホスフィン(C2H5)2PHは沸点85℃,メチルジフェニルホスフィン(CH3)(C6H5)2Pは沸点284℃の無色の液体で特有の臭気があり,水に不溶,エチルアルコール,エーテルに易溶である。トリアルキルおよびアリールホスフィン類は,リン原子の空の3d電子軌道に遷移金属の電子の満たされたd軌道から電子を受け入れる(逆受容)能力が大きく,安定な各種の興味深い錯体をつくる。たとえば1963年バスカL.Vaskaによって初めて合成された[IrCl(CO)(PPh3)2]は,分子状酸素O2を可逆的に付加する。そのほか第三ホスフィンを配位子として含む遷移金属錯体は,水素,窒素分子,およびエチレンなどの各種オレフィンを可逆的または非可逆的に付加するものが多い。
執筆者:漆山 秋雄
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「ホスフィン」の意味・わかりやすい解説
ホスフィン
ほすふぃん
phosphine
水素化リン(リン化水素)PH3とその誘導体の総称。ホスフィンPH3は、無水のホスホン酸H2PHO3を200℃に熱するか、あるいはヨウ化ホスホニウムPH4Iをアルカリで加水分解してつくる。アルカリ金属やアルカリ土類金属のリン化物を、水または希酸と反応させても得られる。白リンに水酸化ナトリウム水溶液を反応させるとき発生する気体は、大部分がPH3であるが、ジホスフィンP2H4が副生するので、空気に触れて自然発火して燃える。きわめて有毒な無色の悪臭のある気体。融点-133.5℃、沸点-87.7℃。比重0.746(-90℃)。水、ベンゼン、二硫化炭素に溶ける。ホスホニウムイオンPH4+はアンモニウムイオンに比べて不安定である。PH3のアルキルあるいはアリール置換誘導体PR3、PHR2、PH2Rなどもホスフィンとよばれている。これら有機ホスフィンは各種のものが知られている。たとえばP(CH3)3(沸点40℃)、P(C2H5)3(沸点127℃)、P(C6H5)3(融点80℃)などの無色の物質である。これら有機ホスフィンは遷移金属に配位して、安定な低酸化数錯体をつくる。とくにトリフェニルホスフィンP(C6H5)3を配位した錯体はよく知られており、たとえば、ウィルキンソン錯体[RhI(Cl)(P(C6H5)3)3]はオレフィンの水素添加反応の触媒として用いられる。
[守永健一・中原勝儼]
化学辞典 第2版 「ホスフィン」の解説
ホスフィン
ホスフィン
phosphine
リンの水素化物とそのアルキル,アリール置換体の総称であるが,普通には水素化リンPH3をさす.PH3(34.00)は黄リンをKOH水溶液と煮沸するか,リン化カルシウムCa3P2を加水分解すると得られる.天然にも含リン有機物(魚など)の腐敗の際に少量生じる.無色,悪臭(魚などの腐敗臭)のある気体.気体分子は三方すい型.密度0.746 g cm-3(-90 ℃).P-H約1.42 Å.∠H-P-H約93°.融点-133 ℃,沸点-87.7 ℃.水に微溶.氷酢酸,CS2に易溶.普通は微量のジホスファンP2H4を含むため,空気に触れると自然発火する(純粋なら150 ℃ で発火).酸素,ハロゲン単体とはげしく反応する.金属と反応してリン化物をつくる.還元性が大きい.有機反応原料,ホスフィン錯体の製造原料,穀物の燻(くん)蒸などに用いられる.猛毒.[CAS 7803-51-2][別用語参照]ホスファン
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「ホスフィン」の意味・わかりやすい解説
ホスフィン
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「ホスフィン」の解説
ホスフィン
毒性のあるガスで,リンの最も還元された状態の化合物.また,H3Pの水素を有機基Rで置換した物質を総称していう.例えば RH2Pを第一級ホスフィン,R2HPを第二級ホスフィンという.
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...

