最新 心理学事典 「非侵襲的脳機能研究法」の解説
ひしんしゅうてきのうきのうけんきゅうほう
非侵襲的脳機能研究法
non-invasive measurements of human brain function
非侵襲的脳機能研究では,1次信号・2次信号・3次信号のいずれかを,頭部あるいは頭部の周囲に配置したセンサーによって計測する。主要な計測法として,後述する機能的磁気共鳴画像(fMRI),陽電子断層撮影法(PET),脳波(EEG),脳磁波(MEG),近赤外分光法(NIRS)がある。上記の定義からは外れるが,経頭蓋磁気刺激(TMS)も用いられる。また直接脳活動を計測しなくても,脳損傷患者の損傷部位と,損傷により欠損した精神機能の関連を調べる神経心理学や,精神物理学の一部,たとえば知覚学習perceptual learningの成立に一次視覚野の可塑性が関与することを心理実験だけで示した研究(Karni,A.,& Sagi,D.,1991)も広義の非侵襲的脳機能研究法に含まれる。
図2に非侵襲的脳機能研究の主要な計測法における空間分解能spatial resolution,時間分解能time resolution,temporal resolution,および侵襲性と計測可能な脳領域を概略的に示す。空間分解能とは,脳の異なる部位が同時に2ヵ所以上活動した場合に,それぞれを独立した活動として分離できる最小の距離である(図2のd)。時間分解能とは,脳の同一の場所が短期間に2回以上活動した場合に,それぞれを時間的に分離できる最短の間隔である(図2のt)。各計測法の空間分解能と時間分解能は,脳の神経活動に伴うどのような現象を計測し,その現象が局所の神経活動に対してどのような空間スケール・時間スケールで生じているかということと,計測・解析の過程において生じる誤差の大きさに依存し,EEG・MEG・NIRSのセンサー数,fMRIやPETの画素サイズ,サンプリングレートなどは2次的要素にすぎない。
【非侵襲的脳機能研究におけるインフォームドコンセント】 EEG,MEGは神経細胞の電気的活動を電位・磁場として記録するだけで,計測が脳に不可逆的変化を起こす可能性はない。他の計測法は,脳にさまざまな形でエネルギーを与える。PETでは放射能,fMRIでは静磁場・変動磁場・電磁波,NIRSでは近赤外光,TMSでは変動磁場である。それぞれの装置は主に医療用として開発され,薬事法などによって定められた基準内で使用すれば,計測が直接の原因となって脳に不可逆的変化を起こす可能性はきわめて低いが,絶対的な安全性は保証されていない。医療での計測は,それに基づく診断が患者にもたらす利益と,想定される危険性とのバランスの上に成立している。被験者に直接の利益をもたらさない基礎研究では,より慎重を期すべきである。想定される危険性を事前に十分に説明したうえでインフォームドコンセントinformed consentを得る必要がある。
【非侵襲的脳機能研究の主要な計測法】
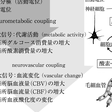
1.機能的磁気共鳴画像functional Magnetic Resonance Imaging(fMRI) 磁気共鳴によって生体の断層像を撮像する磁気共鳴画像(MRI)の装置で,脳活動を反映した画像が得られることから,機能的磁気共鳴画像とよばれる。装置は高価だが,高い空間分解能を有し,臨床検査用の装置をそのまま使用できることから,非侵襲的脳機能研究の中心的な計測法となっている。fMRIの中核となる原理がボールド効果(BOLD効果)blood oxygen level dependence effectである(図3)。細胞への酸素の供給は,赤血球の大部分を占めるヘモグロビンhemoglobinを介して行なわれる。肺で酸素と結合した酸素化ヘモグロビン(oxy-Hb)は動脈→細動脈を経由し,毛細血管で酸素を放出して脱酸素化ヘモグロビン(deoxy-Hb)となり,細静脈→静脈を経て肺に戻る。ヘモグロビンは酸素との結合によって磁化率(磁場中での磁化のされやすさ)が変化し,oxy-Hbは弱い反磁性を,deoxy-Hbは常磁性を示す。したがって強い磁場中でdeoxy-Hbは磁化され,deoxy-Hbを多く含む血管周囲の組織では磁場の均一度が低下する(図3a)。磁気共鳴の信号源である水素原子のスピンの歳差運動の周波数は磁場強度に依存するため,磁場が不均一な領域のスピンの位相は早く乱れ,磁気共鳴信号は急速に減衰する(図3cのa)。したがって通常の状態では,脱酸素化ヘモグロビンを含む毛細血管と周囲の組織の磁気共鳴信号は低下している。これをボールド効果とよぶ。神経活動によって局所酸素消費量が増大するが,酸素を供給するための局所血流量の増加は,実際の酸素消費量を大幅に上回る。その結果,活動した神経細胞周囲の毛細血管capillaryとその下流の細静脈での血流量・流速が上がり,deoxy-Hbは急速に灌流されて減少する(図3b)。磁性体であるdeoxy-Hbの減少によって磁場が均一化され,磁気共鳴信号の減衰が遅くなり信号の増大として計測される(図3cのb)。サルを用いたfMRIと神経生理学的活動の同時記録から,ボールド効果による信号変化は多ニューロン発射活動multi unit activity(MUA)よりも,局所電場電位local field potential(LFP)との相関が高いことが示された。すなわちfMRIの信号は,個々の神経細胞の出力である活動電位action potentialよりも,他の神経細胞からの入力と,それに伴う領域内での神経細胞の活動によるシナプス電流(シナプス後電位)の総和を強く反映している。
MRI装置は撮像法と解析法を変えることにより,機能画像以外にも,構造画像から特定の領域の灰白質や白質の容積を計測するvoxel based morphometry(VBM),脳領域間の神経線維を画像化する拡散テンソル画像diffusion tensor image(DTI),脳内の血管だけを選択的に画像化する磁気共鳴血管造影magnetic resonance angiography(MRA)など,脳活動や脳機能と関連した種々の画像が得られる。またPETと同様に,磁気共鳴分光法magnetic resonance spectroscopy(MRS)によって,代謝に伴うグルコース,アミノ酸の濃度変化や局所脳温変化などの2次信号も計測できるが(図1),撮像時間や信号対雑音比の制限から,いまだ研究段階にある。
2.陽電子断層撮影法positron emission tomography(PET) 15Oは,陽電子(電子と同じ質量で,正の電荷をもつ電子の反粒子)を放出する放射性同位元素の一種で,きわめて短い半減期(約2分)をもつ。15Oを含む水を静脈に注入すれば,血液を介して脳内に流入し,放出される陽電子が周囲の電子と衝突して消滅する際にガンマ線が発生する。これを頭部の周囲にリング状に配置したガンマ線検出器で計測することによって,15Oの脳内分布から局所脳血流量を求め,脳活動に伴い局所的に脳血流量が増加した部位を断層画像として得ることができる。fMRIが,血流の相対的変化しか計測できないのに対して,局所脳血液量cerebral blood volume(CBV),局所脳血流量cerebral blood flow(CBF),酸素摂取率oxygen extraction fraction(OEF),脳酸素代謝率cerebral metabolic rate of oxygen(CMRO2)など,脳における血液循環動態を定量的に評価することが可能である。また18F,11C,13Nなどの放射性同位元素と体内に存在する代謝物質との化合物を投与することにより,グルコース消費量やドーパミンなどの神経受容体の脳内分布など,種々の代謝物質や神経伝達物質の計測が可能である。しかし15Oを用いた場合でも一回の撮像に1分から数分を要するため,計測結果はその間の脳活動の時間的な総和であり,脳活動の動的な変化を追うことはできない。放射能に被曝するため,同一被験者を短期間に何度も計測することもできない。また半減期の短い放射性同位元素を製造する加速器を併設する必要があり,装置の設置・維持には多額の費用がかかるため,健常者の脳血流計測法としてはfMRIに取って代わられている。
3.脳波electroencephalography(EEG)と脳磁波magnetoencephalography(MEG) シナプス活動により大脳皮質の錐体細胞pyramidal neuronにシナプス後電位が発生すれば,細胞体と尖端樹状突起apical dendriteの間で細胞内電流が流れる。細胞内電流は細胞外へ流れ出て,細胞内へ戻る帰還電流を形成する。個々の神経細胞に流れる電流はきわめて小さいが,錐体細胞は皮質表層に向かって樹状突起が垂直に伸び,各細胞が平行に並んでいるので,多数の錐体細胞がいっせいに活動すれば,頭部外から観測可能な電流源となる。頭の周囲に多数の電極あるいはコイルを配置してその電位分布あるいは電流によって生じる磁場分布を計測すれば,電流源の位置・強度・方向を推定できる。MEGは主に錐体細胞の活動によって樹状突起内を流れる細胞内電流が作る磁界(図4a,帰還電流も磁場を作るが,放射状に流出・流入する電流が作る磁界は打ち消し合ってゼロとなる)を,EEGおよび脳表に直接電極を置く皮質脳波Electrocorticography(ECoG)は主に細胞外帰還電流による電極間の電位差(図4b)を計測している。また活動電位は持続時間が短いため,同期的加重が起こりにくく,EEG・MEGの発生には寄与しないと考えられている。計測される信号強度は,EEGで数µV(マイクロボルト)から数百µV,MEGで数十fT(フェムトテスラ:1fT=10-15T)から数百fTにすぎず,MEGでは微弱で低周波の磁場を計測可能な超伝導量子干渉素子superconducting quantum interference device(SQUID)が用いられる。
EEG・MEGの周波数帯域は,1Hz以下から数十Hz,さらに数百Hzの成分も報告されており,高い時間分解能を有する。空間分解能に関しては,脳は脳脊髄液・頭蓋骨・皮膚など,導電率の異なる組織によって何重にも覆われているため,局所的な電気活動の頭皮上での電位分布は歪み,EEGによる脳内電流源の正確な推定は困難である。一方,磁束の通りやすさを示す透磁率は一様で磁場分布は歪まないため,MEGはEEGより正確な推定が可能である。しかしMEGで計測されるのは,脳溝内で頭蓋表面に平行に樹状突起が伸びている錐体細胞の活動であり,脳回にある錐体細胞の活動は検出されない。また,磁束密度は距離の2乗に反比例して低下するため,脳深部の活動の計測は困難であり,樹状突起が平行に並んでいない領域の活動も計測できない。EEG・MEGに共通する最大の問題点は,複数の信号源を推定する手法が確立されていないことである。たとえば眼から入った視覚情報は,数十ms(ミリ秒)後には一次視覚野に到達し,二次・三次視覚野に送られ,同時に五次視覚野にも送られる。さらに二次・三次視覚野からもさまざまな領域に並列的に情報が伝達される。すなわち刺激の呈示から100ms後には複数の領域が活動しており,これらの活動の総和である電位分布・磁場分布から,一つの電流源を推定することの妥当性については,以前から批判がある。
4.近赤外分光法near infra-red spectroscopy(NIRS) 近赤外光とは可視領域と赤外領域の間で,700~2500nm(ナノメートル)の波長の光を指す。可視光に比べて生体組織による吸収が少なく,頭皮上に発光部と受光部を置けば,発光部から入射した近赤外光は,皮膚・頭蓋骨・脳脊髄液・脳組織で散乱し,一部を受光部で検出できる。血液中のoxy-Hbとdeoxy-Hbでは近赤外光領域での吸収スペクトルが異なっているので,700~900nmの複数の波長の近赤外光をフォトダイオード・フォトマルなどの光センサーで検出すれば,光が透過してきた領域のoxy-Hbとdeoxy-Hbの濃度変化を計測できる(図5)。長所としては,⑴被験者の頭部に送光と受光のための光ファイバーを装着するだけなので,fMRIやMEGに比べて,EEGと同様に被験者を拘束することなく,比較的自然な状態で計測ができ,乳幼児や臨床のベッドサイドでの記録も容易である。⑵PETやfMRIでは計測できない,oxy-Hbとdeoxy-Hbの濃度変化を独立に計測できる。ただし,現在の連続光を用いた装置では光路長(光が通過してきた生体組織内の距離)がわからないため,計測で得られる値はoxy-Hbとdeoxy-Hbの絶対量ではなく,ある時点を基準にした相対的な変化量である。⑶fMRIやMEGに比べて,小型で維持費が安い。短所としては,①空間分解能が低い(25mm程度)。②脳表に近い部分で散乱して戻ってくる光を検出するので,脳深部の活動は計測できない。③fMRIと同様に血流を計測しているため,時間分解能は低い。④受光部で検出された光は頭皮も通過している。したがって,計測された信号は脳実質だけでなく頭皮血流の変動も含んでおり,NIRS単独で脳実質のみの血流変化を識別することは困難である。
5.経頭蓋磁気刺激transcranial magnetic stimulation(TMS) 大容量のコンデンサーに蓄電し,頭部に置いたコイルに瞬間的に大電流を流して急激な変動磁場(1~2.5T/100~300µs)を発生させると,電磁誘導によりコイルに流した電流とは逆方向の渦電流がコイル直下の脳領域に流れ,皮質の神経細胞を興奮させる。TMSは本来刺激装置であり,臨床医学では,主に一次運動野を刺激して誘発される誘発筋電図の潜時や振幅から,運動神経の機能評価に使われている。しかし運動を誘発するだけでなく,視覚野の刺激で閃光phospheneが知覚されたり,種々の感覚刺激の呈示直後や特定の課題の遂行中に磁気刺激を与えると,刺激した部位やタイミングに応じて特定の知覚や運動が抑制されることから,健常者の脳に可逆的な損傷lesionを作ることにより(virtual lesion),その部位の機能を調べる方法としても使われるようになった。TMSは皮質を直接刺激することにより,末梢の感覚器官を経由せず,したがって脳幹網様体の活動水準を変えることなく,実験的に知覚を引き起こすことが可能であり,今後の心理学研究においても重要な研究手段になると思われる。ただし,コイルに流れる電流によって発生する磁束密度はコイル中心ではゼロで,コイルの内縁に近づくほど大きくなるため,局所を選択的に刺激することは困難である。8の字型にした二つのコイルに同時に逆方向に電流を流し,より局所的な刺激を可能にしたタイプもある。また,磁場の強さはコイルからの距離の2乗に反比例するので,脳深部の刺激はできない。
【非侵襲的脳機能研究と心理学】 非侵襲的脳機能研究を志す者は,まず何のために脳活動を計測するのかについて考えるべきである。ある課題に伴う脳活動を計測し,単に課題と脳活動パターンとの相関を調べるだけでは,高価な装置を用いて計測を行なう意味はほとんどない。燃焼・腐蝕から,細胞におけるエネルギー代謝,ボールド効果まで,一見まったく異なる現象に「酸化」という共通の過程が関与している。観察される現象の見かけにとらわれずに,それらに共通する概念・過程を帰納的に見つけ出し,それを実験的手法により計測して法則性を見いだし,演繹する過程こそが科学の本質である。非侵襲的脳機能研究も,多様な精神現象・行動に共通する神経基盤を探究し,そのふるまいからヒトの脳と行動に関する法則を導き出し,行動を理解・予測するための一手段である。そのためには,研究者は心理学だけではなく,神経生理学,電子工学,コンピュータ・プログラミングにも精通する必要がある。一例を挙げれば,頭部の2ヵ所に電極を装着して電位差を増幅すれば脳波が計測できる。しかし実際に得られるのは,脳波以外に筋電図electromyography,眼電図electrooculography,心電図electrocardiography,皮膚電気活動electrodermal activityなどを含む生体電位の集合である。そこから脳波(信号)と脳波以外の成分(雑音)を識別し,雑音を除去するための信号処理が必須であり,そのためには上記の分野の知識を基に,用いる計測法の原理・特徴を理解して研究を行なうことが重要である。 →視覚領野 →認知神経科学 →脳機能研究法 →脳波
〔宮内 哲〕
出典 最新 心理学事典最新 心理学事典について 情報