翻訳|rhodopsin
精選版 日本国語大辞典 「ロドプシン」の意味・読み・例文・類語
ロドプシン
- 〘 名詞 〙 ( [英語] rhodopsin ) 視細胞の一種で、棒細胞に含まれる感光性の色素蛋白質。光吸収による構造変化が視覚の第一段階として働く。視紅。桿状体視物質。
日本大百科全書(ニッポニカ) 「ロドプシン」の意味・わかりやすい解説
ロドプシン
ろどぷしん
rhodopsin
脊椎(せきつい)動物の網膜retinaにある視細胞のうち桿体(かんたい)rodまたは桿状体細胞外節の円板体膜に含まれる赤い色素タンパク質(視物質または視色素)で、視紅visual purpleともよばれる。ビタミンAのアルデヒド誘導体である11-シス-レチナールを発色団とし、これとアミノ酸348個、分子量3万9048、直径約10ナノメートル(1ナノメートルは10億分の1メートル)のタンパク質オプシン(ロドプシンのタンパク質部分)とが、リジンのε(イプシロン)-アミノ基とシッフ塩基をつくって結合したものである。暗所では紫紅色、光に当てると赤色から橙色を経て黄色のレチナール(レチネン=視黄)となり、さらに、無色のレチノール(ビタミンA1=視白)となる。それぞれ異なる吸収帯を示す5~6種の中間体、バソロドプシン(ヒプソロドプシンを経由することもある)、ルミロドプシン、メタロドプシン-Ⅰ、-Ⅱ、-Ⅲを経て全トランス‐レチナールになって退色し、光を遮ると回復する(これを視覚サイクルという)。オプシンには明暗を区別する(薄明視)桿体オプシン(スコトプシン、分子量約3万8000)と、色を区別する(昼間視)錐体(すいたい)オプシン(フォトプシン)がある。
ロドプシンは1877年、ドイツの生理学者キューネWilhelm Kühne(1837―1900)がカエルの網膜から初めて抽出した。オプシンは、水不溶の膜タンパク質なので界面活性剤を用いた。ウシのオプシンは単糖7~8個からなる糖鎖(グルコースなどの糖がいくつかつながったもの)を二つもち、2分子のパルミチン酸で修飾されている。348個のアミノ酸配列は1982年に決定された。アミノ酸組成では疎水性アミノ酸が半分を占める。ロドプシンのポリペプチド鎖はアミノ末端を円板体内部に、カルボキシ末端を桿体細胞質側に露出し、中間部分は7回円板体膜を横切っている。膜内部分はほとんどα(アルファ)-ヘリックス(ポリペプチド鎖がとりうる安定な螺旋(らせん)構造の一つ)を形成している。ロドプシンは光を受けると、寿命が非常に短く、色の異なる数種の中間体を経て全‐トランス‐レチナールとオプシンに分離する。この過程で、膜表面にあるGTP(グアノシン三リン酸)結合タンパク質(G-タンパク質)の一つであるトランスデューシンtransducinがロドプシンに結合して活性化され、これがさらにフォスフォジエステラーゼ(リン酸モノエステルを生成する酵素)を活性化するため、サイクリック(環状)GMPが5'-GMP(グアニル酸)に変化する。これによりナトリウムイオン(Na+)の桿体細胞内への流入停止とカルシウムイオン(Ca2+)の流出、円板膜の表面電位の変化などが生じ、光のエネルギーと情報が神経信号へ変換して脳へ伝えられる。ビタミンAの不足で特発性夜盲症nyctalopiaになるのは、ロドプシンの生成が不十分になるからである。なお、ある種の高度好塩菌はロドプシンによく似たバクテリオロドプシンをもち、光合成を行う。
また、網膜視細胞にあるアレスチンarrestin(S抗原)は分子量約4万8000、アミノ酸438個で、リン酸化されたロドプシンに結合してロドプシンとトランスデューシンとの相互作用を阻害する。ウシ‐ロドプシンの立体構造は2000年に2.8オングストローム(Å)解像度で決定された。なお、2003年(平成15)、琵琶湖(びわこ)のアユの網膜オプシンの一部がクローニング(特定の遺伝子を単離すること。クローン化)された。さらに同年、ヨーロッパ分子生物学研究機構のグループが二次元結晶を用いて超低温電子顕微鏡によって立体構造を決定した。
[野村晃司]
『前田章夫著『視覚』(1986・化学同人)』▽『高木雅行著『図説 情報生物科学』(1988・朝倉書店)』▽『葛西道生他編『神経情報伝達分子――脳機能の分子レベルでの理解をめざして』(1988・培風館)』▽『森川耿右編『蛋白質立体構造の新しい視点』(1991・講談社)』▽『前田章夫著『視覚のメカニズム』(1996・裳華房)』
改訂新版 世界大百科事典 「ロドプシン」の意味・わかりやすい解説
ロドプシン
rhodopsin
視紅visual purpleともいう。網膜の杆状体(かんじようたい)の外節に含まれる紫紅色の色素タンパク質で,光の受容体として機能する。網膜には2種類の視細胞,錘状体と杆状体がある。前者は強い光に反応して色覚をつかさどり,後者は弱い光のもとで明暗を識別するが,色覚には関係しない。ロドプシンは,細胞内のディスク膜の成分である分子量3万8000のオプシンopsinに,ビタミンAの誘導体11-シス-レチナールretinalが結合した複合タンパク質である。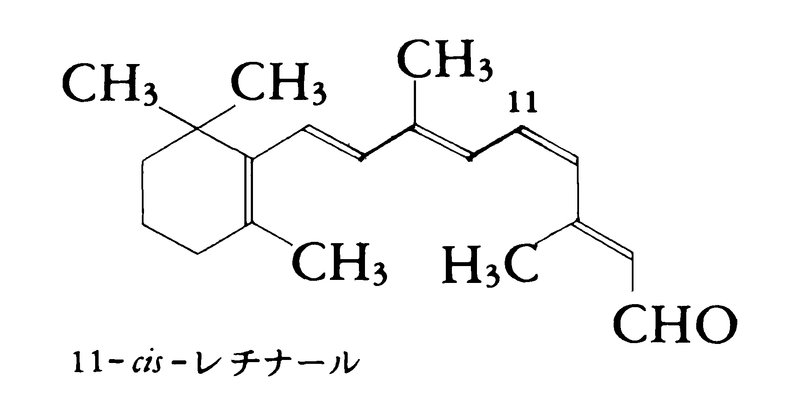
ビタミンAが欠乏するとロドプシンの合成が損なわれ夜盲症の原因となる。光を受けたロドプシンは一連の複雑な光化学的異性化反応を経て,最終的に全トランス-レチナールとオプシンに解離し,それに伴って杆状体細胞膜に一過性の膜電位変化が起きる結果,視神経が刺激されて視覚が生じる。全トランス-レチナールは暗所で異性化して再び11-シス-レチナールになり,オプシンと再結合してロドプシンを再生する。ある種の好塩性細菌がもつバクテリオロドプシンは,光エネルギーを利用して水素イオンH⁺の能動輸送を行い,一種の光合成色素として機能している。
執筆者:川喜田 正夫
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「ロドプシン」の解説
ロドプシン
ロドプシン
rhodopsin
視細胞の膜に多数埋め込まれた光受容タンパク質で,膜7回貫通型のタンパク質部分(オプシンという)の中央に,光センサーとなるレチナール(アルコールレチノールが酸化されてできるアルデヒドレチノール)が結合している.レチナールの光異性化がロドプシン分子の構造変化を引き起こし,それがきっかけとなって視細胞内で一連の反応が起こり,最終的に視細胞の電気的興奮として脳に情報が伝えられる.可視光に広く応答するロドプシンや,色の三原色によく応答するロドプシンなどがある.これらは同じレチナールを有するが,それを取り囲むタンパク質オプシンのアミノ酸配列がわずかに異なり,異なる波長の光に応答できるようになっている.[CAS 9009-81-8][別用語参照]視紅
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「ロドプシン」の意味・わかりやすい解説
ロドプシン
→関連項目夜盲症
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「ロドプシン」の意味・わかりやすい解説
ロドプシン
rhodopsin
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「ロドプシン」の解説
ロドプシン
世界大百科事典(旧版)内のロドプシンの言及
【視覚】より
… 視細胞に光が当たったときに,光のエネルギーを吸収して光化学変化を起こすのが感光色素である。杆体の感光色素はロドプシンで,光が当たると分解してビタミンA1のアルデヒドであるレチナール1とオプシンというタンパク質になる。暗黒中では,十分レチナール1が存在するときには,レチナール1とオプシンからロドプシンが再生する。…
※「ロドプシン」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

