化学辞典 第2版 「濃淡電池」の解説
濃淡電池
ノウタンデンチ
concentration cell
電池反応が通常の化学反応ではなく,一つの相からほかの相への濃度差による物質移動に相当する電池.大別して2種類がある.
(1)液-液界面を含む濃淡電池:溶液相の濃度が異なる以外はまったく同様な二つの電極系を二つの溶液相があい接するように構成された電池.物質の移動が二つの溶液相界面を通して直接的に起こる.たとえば,塩酸濃度のみが異なる二つの銀-塩化銀電極で構成される電池,
Ag|AgCl|HCl(cⅠ)∥HCl(cⅡ)|AgCl|Ag
はその一例であり,この電池の平衡電圧 Ueq は次のように与えられる.
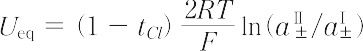
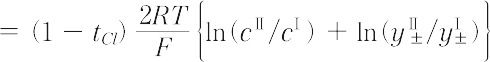
ここで,tCl は塩化物イオンの輸率,a± および y± はそれぞれイオンの平均活量および平均活量係数であり,R,T,Fはそれぞれ気体定数,絶対温度およびファラデー定数である.したがって,平均活量係数の比がわかっていれば,この平衡電圧の測定値から塩化物イオンの輸率を算出することができる.一般に,この種の電池はイオンの輸率の測定に用いられる.
(2)液-液界面のない濃淡電池:濃度の異なる二つの相が直接あい接しないように構成され,物質の移動が電極反応を介して間接的に起こるように工夫された濃淡電池.活量の異なる同じ金属の電極(たとえば,アマルガム電極)をその金属イオンを含む溶液中に挿入して構成された電池,
Naアマルガム(cⅠ)|NaCl|Naアマルガム(cⅡ)
はその一例であり,この場合の電池をアマルガム濃淡電池という.また,ガス電極を用いる場合には気体の圧力が異なる組合せによっても同じような濃淡電池ができる.
Pt|H2(pⅠ)|H2SO4|H2(pⅡ)|Pt
この電池をガス濃淡電池という.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報

