内科学 第10版 の解説
発作性夜間ヘモグロビン尿症(後天性溶血性貧血)
概念・分類
発作性夜間ヘモグロビン尿症(PNH)は後天性にPIGA変異を獲得した造血幹細胞のクローン性拡大により血管内溶血と血栓症を呈するが,造血不全も高率に併発する.病因は不明である.PNH病型には古典型,再生不良性貧血(AA)-PNH症候群で代表される骨髄不全型,混合型がある.PNHは遺伝性球状赤血球症と自己免疫性溶血性貧血とともに日本の3大溶血性疾患であり,また造血不全と白血病化を共有するAAや骨髄異形成症候群(MDS)とともに骨髄不全症候群に含まれる.
疫学
1866年の第1例報告以来,世界中で患者が確認され日本でも1940年に第1例が報告されている.推定有病率は100万人に1~5人で性差は乏しい.診断時年齢は10歳から86歳,平均45歳,と幅広い.欧米に比べると日本では溶血や血栓より造血不全が全面に出る例が多い.PNH患者における白血病発症率は約3%で,一般人口の場合より高い.血栓症は日本4.3%で欧米(米国31.8%)と比べるときわめて低い.
病態生理
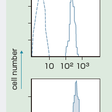
PNH赤血球は補体介在性に血管内で溶血し,遊離ヘモグロビンが尿中へ排泄され,その一部は尿細管で吸収され,尿中脱落の上皮内にヘモジデリンとして検出される.溶血は慢性持続性であるが感染症などで一過性に増強される.患者赤血球は補体感受性の程度により正常(Ⅰ型),3~5倍の軽度亢進(Ⅱ型),15~25倍の高度亢進(Ⅲ型)に分類される.この補体感受性亢進は補体制御蛋白のdecay-accelerating factor(DAF,CD55)やCD59の欠損に起因する.ほかにも欠損蛋白は20以上ある.いずれも正常血球ではグリコシルホスファチジルイノシトール(glycosylphosphatidylinositol:GPI)とよばれる糖脂質と結合して膜に発現するが,PNH血球ではGPIがなく発現できない(図14-9-14).原因はX染色体遺伝子PIGAの変異にあり,この変異によりGPIが合成されない.PNH発症に必要な変異クローン拡大にはPIGA変異に加えて増殖亢進も必要と指摘されている.一方,血球減少が免疫抑制療法により改善することなどから自己免疫による造血細胞傷害が想定されている.なお,血栓形成には溶血の影響が大きく,また貧血の発生には溶血,ヘモグロビンの尿中排泄による鉄欠乏,造血障害,出血などが影響する.
臨床症状・所見
症状は溶血亢進時に顕著になり,胸骨下痛,腰痛,頭痛,発熱,倦怠感,食道平滑筋の攣縮による嚥下困難や嚥下痛,勃起障害を訴える.これらは溶血に伴い血中へ遊離するヘモグロビンが一酸化窒素の作用を阻害するためと考えられる.また血小板減少や血栓に伴う循環障害のために紫斑,鼻出血,点状出血,消化管出血などが現れる.血栓は門脈域,肝静脈(Budd-Chiari症候群)に多く発生し,腹痛や悪心,イレウス,肝脾腫,腹水を呈する.感染症は上気道,尿路,腸に多い.
検査成績
溶血と造血不全を反映して網赤血球の相対的増加と血球減少を認める.診断時平均値はHb 8.2 g/dL,平均赤血球容積(MCV)103 fL,白血球数3500/μL,血小板数9.6万/μLであり,好中球減少は72%,血小板減少は63%である.ほかに,LDH高値(1572 U/L),間接ビリルビン増加,ハプトグロビン低値,血漿遊離ヘモグロビン,ヘモグロビン尿,ヘモジデリン尿,尿中ウロビリン体増加を認める.溶血の補体消費量は少なく,血清補体価は低下しない.ヘモグロビン尿が続くほど鉄欠乏になり小球性低色素性貧血に傾き,また造血不全が進行すると溶血が不鮮明になる.骨髄は過形成から低形成までみられる.PNH特有の染色体異常はなくMDSと似てモノソミー7やトリソミー8がある.
診断
後天性Coombs陰性血管内溶血,血球減少,鉄欠乏,血栓症,腹痛や腰痛はPNHを疑う.Ham試験や砂糖水試験ではPNH赤血球を補体介在性に溶血させて検出する.最近は,PNH血球の種類と数,欠損膜分子の種類と欠損程度を評価できるフローサイトメトリー法が普及している(図14-9-14).PNH赤血球は1%あればよい.診断精度の向上には顆粒球と赤血球の二血球系における複数GPI結合膜蛋白の同時欠損をとらえる(図14-9-14).GPI発現血球と欠損血球の共存はPNHに特有で,HEMPAS(hereditary erythroblastic multinuclearity associated with a positive acidified serum test,酸溶血試験陽性の遺伝性多核赤芽球症)などの先天性疾患との鑑別は容易である.
治療
溶血,血栓症,造血不全に対する治療が主である.これらの病態が重度で,かつHLA適合ドナーがいる若い患者ほど造血幹細胞移植を考慮する.しかし,補体C5を阻害する新しい抗体医薬のエクリズマブが登場し,溶血と血栓症を確実に抑制することから,移植対象者は減ると予想される.溶血発作に対するエクリズマブ効果は未確認であり,現実には誘因を除き,貧血に血漿成分を除去した洗浄赤血球を輸血するとともに,輸液,利尿,ハプトグロビンを用い,腎を保護する.血栓症の防止にはエクリズマブが有効である.発症後には急性期にヘパリン持続点滴,慢性期にワルファリン内服で治療する.一方,造血不全に対する治療は再性不良性貧血の治療に準じ,シクロスポリンや抗胸腺細胞グロブリンなどの免疫抑制薬や造血サイトカインを用いる.反応が乏しい場合には輸血を行うが鉄過剰症の発生に注意する.なお,エクリズマブは造血障害には無効である.
予後
診断後平均生存期間は32年で,死因は60%が出血と感染症である.ほかに腎不全,心不全,MDSや白血病,血栓症がある.日本の症例は造血不全,欧米例では溶血や血栓の影響を強く受ける.予後悪化要因として,血栓症,MDSや白血病の発生,汎血球減少,診断時年齢50歳以上などがある.自然寛解は4.8%である.[中熊秀喜]
■文献
金倉 譲,他:発作性夜間ヘモグロビン尿症. 特発性造血障害疾患の診療の参照ガイド(平成22年度改訂版),厚生労働科学研究費補助金難治性疾患克服研究事業 特発性造血障害に関する調査研究班(代表 小澤敬也),pp 99-139,2011.
中熊秀喜:発作性夜間ヘモグロビン尿症(PNH). 三輪血液病学,第3版(浅野茂隆,池田康夫,他監修),pp1163-1181,文光堂,東京,2006.
発作性夜間ヘモグロビン尿症(血液疾患と腎障害)
間質尿細管障害を背景とした腎障害はPNH患者に高頻度に認められる.通常,補体制御因子はglycosylphosphatidylinositol(GPI)を含む糖脂質をアンカーとして赤血球膜表面に結合している.しかし,PNH赤血球では遺伝子変異によりGPIアンカーの合成が障害され,補体制御因子が欠損し,補体感受性が亢進して溶血を生じる.夜間睡眠中に血液pHが酸性に傾くと補体が活性化され血管内溶血が生じる.遊離したヘモグロビンは糸球体で濾過され,近位尿細管で再吸収されるが,鉄処理能をこえて再吸収されたヘモグロビンはヘモジデリンとして沈着し尿細管障害を引き起こす.溶血の程度が激しい場合は,円柱形成による尿細管閉塞による急性腎不全も生じうる.腎障害の予防として,溶血発作時には輸液を行い,尿量を確保する.[前嶋明人・野島美久]
出典 内科学 第10版内科学 第10版について 情報