精選版 日本国語大辞典 「溶解度積」の意味・読み・例文・類語
出典 精選版 日本国語大辞典精選版 日本国語大辞典について 情報
改訂新版 世界大百科事典 「溶解度積」の意味・わかりやすい解説
溶解度積 (ようかいどせき)
solubility product
塩類MAの飽和溶液中では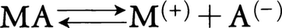 の平衡が成立し,陽イオンと陰イオンの濃度[M⁽⁺⁾],[A⁽⁻⁾]の積[M⁽⁺⁾][A⁽⁻⁾]は,一定温度における難溶性塩の場合に一定であることが実験で確かめられている。この値を溶解度積KsPという。この場合も化学平衡であるから,KsPは系の標準自由エネルギー変化⊿G°と関連づけられる(⊿G°=-RTlnKsP)。⊿G°は物質に固有の一定値であるから,一定温度において,KsPは一定であるということが熱力学的にも示される。溶解度積は化学分析(金属イオンの分析,沈殿滴定など)に利用される。とくに陰イオンの濃度を水素イオンの濃度や陽イオンの濃度により調節することが可能であるから,KsPの大きさの違いにより他の金属イオンの共存系から特定の金属イオンだけを沈殿させることができる。また陰イオンの濃度を抑制することにより錯形成を防ぐことも可能である。溶解度積は一般に一つの分子から解離するイオンの数によってべきの形で表す。塩
の平衡が成立し,陽イオンと陰イオンの濃度[M⁽⁺⁾],[A⁽⁻⁾]の積[M⁽⁺⁾][A⁽⁻⁾]は,一定温度における難溶性塩の場合に一定であることが実験で確かめられている。この値を溶解度積KsPという。この場合も化学平衡であるから,KsPは系の標準自由エネルギー変化⊿G°と関連づけられる(⊿G°=-RTlnKsP)。⊿G°は物質に固有の一定値であるから,一定温度において,KsPは一定であるということが熱力学的にも示される。溶解度積は化学分析(金属イオンの分析,沈殿滴定など)に利用される。とくに陰イオンの濃度を水素イオンの濃度や陽イオンの濃度により調節することが可能であるから,KsPの大きさの違いにより他の金属イオンの共存系から特定の金属イオンだけを沈殿させることができる。また陰イオンの濃度を抑制することにより錯形成を防ぐことも可能である。溶解度積は一般に一つの分子から解離するイオンの数によってべきの形で表す。塩 のとき
のとき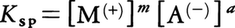 である。溶解度積は固体と溶媒和したイオンについて考えるもので,難溶性塩についてのみ意味をもつ値である。
である。溶解度積は固体と溶媒和したイオンについて考えるもので,難溶性塩についてのみ意味をもつ値である。
執筆者:橋谷 卓成
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「溶解度積」の解説
溶解度積
ヨウカイドセキ
solubility product
難溶性の塩の飽和水溶液中に存在する陽イオン濃度と陰イオン濃度の積.溶解度定数ともいう.たとえば,Pb(OH)2は次のようにイオンになって水に溶ける.
Pb(OH)2(s)  Pb2+ + 2OH-
Pb2+ + 2OH-
このときの25 ℃ における溶解度積 Ksp は次のように表される.
Ksp = [Pb2+][OH-]2 = 1.42×10-20 (mol/L)3
代表的な難溶性塩の25 ℃ における溶解度積を示す.
AgCl 1.77×10-10,BaSO41.07×10-10,CaCO34.96×10-9,Fe(OH)32.64×10-39,ZnS 2.9×10-25.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「溶解度積」の意味・わかりやすい解説
溶解度積
ようかいどせき
solubility product
AB(固体)⇔AB(未解離分子)⇔A++B-
したがって質量作用の法則から
[A+][B-]=K[AB] ( K は平衡定数)
K[AB] の値は一定温度では一定値であるので [A+][B-] は一定値となる。このイオン積を溶解度積と呼ぶ。 [B-] の濃度の値が大きくなると [A+] の値が小さくなり,AB の未解離分子が多くなる。この効果を共通イオン効果と呼び,難溶性塩の沈殿促進法としてよく用いられる。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
日本大百科全書(ニッポニカ) 「溶解度積」の意味・わかりやすい解説
溶解度積
ようかいどせき
solubility product
難溶性の塩の飽和溶液における陽イオンと陰イオンの濃度積(分析濃度積)をいう。この値は温度によって定まる条件定数であり、AmXn型の塩においては、[A]m[X]nの形である。固相の活量を1と置いた不安定度定数とみなすこともできる。イオンの沈殿条件を定めるのには重要な指標である。
溶解度積は分析濃度の積であるから、難溶性塩の場合にのみ大きな意義をもつ。もし濃度の積が溶解度積よりも大となれば、沈殿が生成して濃度は低下する。定性分析でよく用いられる硫化物の溶解度積も、0.3モル塩酸酸性の硫化水素水(ほぼ0.3モル/リットル)中の硫化物イオンの濃度は、酸解離定数から考えると10-22mol/lとなり、鉄(二価)イオンは1モル以上ないと沈殿が生じない(溶解度積を超えない)が、銅や水銀はほぼ定量的に沈殿してしまうことがわかる。
[山崎 昶]
世界大百科事典(旧版)内の溶解度積の言及
【海水】より
…
[溶解度]
いま海水に少量の食塩を加えても溶けるように,海水は塩化ナトリウムの溶解度に関して未飽和である。塩が飽和している状態では,その塩を構成するイオン濃度の積が一定であり,これを溶解度積と呼んでいる。海水の主要成分の濃度をそれらの塩類の溶解度(積)と比べたとき,海洋表層の炭酸カルシウムの場合を除いて,ほとんどが未飽和の状態にある。…
※「溶解度積」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
お知らせ
4/12 日本大百科全書(ニッポニカ)を更新
4/12 デジタル大辞泉を更新
4/12 デジタル大辞泉プラスを更新
3/11 日本大百科全書(ニッポニカ)を更新
2/13 日本大百科全書(ニッポニカ)を更新
