改訂新版 世界大百科事典
「コールラウシュの法則」の意味・わかりやすい解説
コールラウシュの法則 (コールラウシュのほうそく)
Kohlrausch's law
F.W.G.コールラウシュが1875年に発見した法則。〈コールラウシュのイオン独立移動の法則〉ともいう。無限希釈溶液中における電解質の当量伝導率Λ∞は,電解質を構成している陽イオンおよび陰イオンの無限希釈状態におけるイオン当量伝導率λ+∞およびλ-∞の和に等しい,という法則。無限希釈状態ではイオン間の相互作用を無視できるから,電場下における個々のイオンの移動速度(したがってイオン当量伝導率)は,そのイオン自身の性質(形,大きさ,電荷など)と媒質の性質(温度,圧力,粘度など)とだけで決まるからである。弱電解質HAの無限希釈における当量伝導率を電気伝導の実験値から直接決定するのは困難であるが,この法則を用いると適当な強電解質についての測定値からΛ∞HAを求めることができる。たとえば,酢酸については,酢酸ナトリウム,塩酸,および塩化ナトリウムの当量伝導率を用いて次式から計算すればよい。
Λ∞(CH3COOH)=Λ∞(CH3COONa)+Λ∞(HCl)-Λ∞(NaCl)
執筆者:玉虫 伶太
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
Sponserd by 
コールラウシュの法則
コールラウシュノホウソク
Kohlrausch's law
【Ⅰ】希薄溶液中における強電解質の濃度と当量電気伝導率との間の関係で,F.W.G. Kohlrauschにより実験的に見いだされた経験則.濃度c(モル濃度)における当量電気伝導率Λは,無限希釈における当量電気伝導率を Λ∞ とすると,次のように表される.
Λ = Λ∞ - A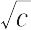
ここで,Aは温度,溶媒と電解質の種類により決まる定数である.この関係式は,Λが と直線関係にあるので平方根則とよばれ,のちに,L. Onsager(オンサガー)により理論的に導き出された(オンサガーの式).なお,濃度が0.001 mol L-1 以上になると,Λの実測値は上式よりはずれてくるので,実測値とできるだけ合うように補正項を加えた半実験式も提出されている.【Ⅱ】無限希釈溶液中では,当量イオン伝導率の値は,共存するイオンの種類には無関係に,溶媒の性質(温度,圧力,粘度など)とそのイオン自身の性質だけで定まり,したがって,無限希釈の状態下での電解質の当量電気伝導率は,電解質を構成するイオンの当量イオン伝導率の総和で与えられるという,Kohlrauschにより実験的に確かめられた法則.コールラウシュの加成則あるいはイオン独立移動の法則ともよばれる.
と直線関係にあるので平方根則とよばれ,のちに,L. Onsager(オンサガー)により理論的に導き出された(オンサガーの式).なお,濃度が0.001 mol L-1 以上になると,Λの実測値は上式よりはずれてくるので,実測値とできるだけ合うように補正項を加えた半実験式も提出されている.【Ⅱ】無限希釈溶液中では,当量イオン伝導率の値は,共存するイオンの種類には無関係に,溶媒の性質(温度,圧力,粘度など)とそのイオン自身の性質だけで定まり,したがって,無限希釈の状態下での電解質の当量電気伝導率は,電解質を構成するイオンの当量イオン伝導率の総和で与えられるという,Kohlrauschにより実験的に確かめられた法則.コールラウシュの加成則あるいはイオン独立移動の法則ともよばれる.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
Sponserd by 
法則の辞典
「コールラウシュの法則」の解説
コールラウシュの法則【Kohlrausch law】
出典 朝倉書店法則の辞典について 情報
Sponserd by 


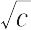
 と直線関係にあるので
と直線関係にあるので