内科学 第10版 「アルコール性肝障害」の解説
アルコール性肝障害(肝・胆道の疾患)
アルコール性肝障害とは,長期(通常は5年以上)にわたる過剰の飲酒が肝障害のおもな原因と考えられる病態で,以下の条件を満たすものを指す(表9-8-1).①過剰の飲酒とは,1日平均純エタノール60 g以上の飲酒(常習飲酒家)をいう.ただし女性やアルデヒド脱水素酵素 (aldehyde dehydrogenase:ALDH)2活性欠損者では,1日40 g 程度の飲酒でもアルコール性肝障害を起こしうる.②禁酒により,血清AST,ALTおよびγ-GTP値が明らかに改善する.③肝炎ウイルスマーカー,抗ミトコンドリア抗体,抗核抗体がいずれも陰性である.
病型分類
病型分類を表9-8-2に示す.アルコール性脂肪肝,アルコール性肝線維症,アルコール性肝炎,アルコール性肝硬変,アルコール性肝癌がおもな病型である(図9-8-1).
病因・病態生理
1)アルコール代謝:
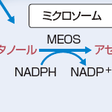
摂取されたアルコールは約80%が空腸から吸収され,その約90%が肝臓で代謝される.アルコール脱水素酵素(alcohol dehydrogenase:ADH)を介する代謝系が主体である(図9-8-2).慢性的な飲酒によりミクロソームにチトクロームP4502E1(CYP2E1)を中心とするミクロソームエタノール酸化系(microsomal ethanol oxidizing system:MEOS)が誘導される.慢性的な飲酒により誘導されたときや血中アルコール濃度が高いときはMEOSの経路の比率が高くなる.そのほかにカタラーゼによっても代謝されるが,その関与は少ない.いずれの系でもアセトアルデヒドが産生され,ALDHで代謝され酢酸となる.
2)発症機序:
a)エタノール代謝に伴うNADH/NAD比上昇:肝内でのアルコール代謝が亢進すると,ADH,ALDHの補酵素であるニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD) からNADHへの転換が亢進し,NADH/NAD比が上昇する(図9-8-2).脂肪肝の成因として,①このエタノール代謝に伴うNADH/NAD比上昇によりクエン酸回路が障害され,アセチル-CoAが増加して脂肪酸合成が亢進する機序と,②脂肪酸のβ酸化を抑制する機序が深く関与しており,さらに③末梢からの脂肪動員の増加,④肝臓から末梢への脂肪運搬障害も影響している. b)酸化ストレス:肝循環の下流に位置する小葉中心部では生理的に酸素分圧が低いが,アルコール代謝による酸素消費の増加が,アルコール性肝障害に特徴的な小葉中心性の肝障害を惹起していると考えられている. また,慢性的な飲酒により誘導されるCYP2E1は,さまざまな活性酸素種を産生することが知られており,慢性アルコール投与時の酸化ストレス発生に深く関与している.さらに,CYP2E1の活性化に続くミクロソームのNADPH酸化酵素の活性化が脂質過酸化反応を惹起し,肝障害を進展させる.好中球など炎症性細胞由来のNADPH酸化酵素群も,活性酸素の産生源として重要な役割を担っている. c)サイトカイン・微小循環障害:慢性的な飲酒により腸管からのエンドトキシン透過性が亢進し,高率にエンドトキシン血症をきたす.エンドトキシンは,Kupffer細胞を活性化し,炎症性サイトカイン産生を介して細胞傷害を直接惹起する一方で,血管作動性物質による肝類洞径や肝血管抵抗の変化,接着因子の発現増強などにより肝微小循環障害を惹起する.微小循環障害の形成に白血球の役割も重要で,アルコール性肝炎では多核白血球の浸潤がその病態進展に深く関与している.
エタノールによる血中アディポネクチン値の減少が,肝臓内の脂肪酸合成や脂肪酸の酸化に関与する受容体の発現や,転写因子を修飾し,アルコール性脂肪肝を進展させる.
d)アセトアルデヒド:アセトアルデヒドは,チュブリン蛋白の重合を阻害して微小管を減少させ,合成された糖蛋白や脂質の分泌障害を引き起こし,これが肝細胞の泡沫脂肪化や肝細胞の風船化を伴った傷害につながっている.また,種々の蛋白や脂質などと結合し,抗原性をもったアセトアルデヒドアダクトを形成する.アセトアルデヒドアダクトは,肝細胞の機能を障害し,肝炎や肝発癌に関与している.
e)肝線維増生作用:アルコールやその代謝産物がKupffer細胞や単核球を刺激し,transforming growth factor(TGF)-βなどの発現誘導,産生促進により星細胞が活性化され,肝線維化を促進する.
f)栄養障害と生活習慣病の関与:飲酒に伴う栄養障害としては,以前は栄養素の欠乏や低栄養状態が取り上げられてきたが,近年はむしろ過栄養がアルコール性肝障害の進展を増強することが示唆されている.アルコール性肝硬変において糖尿病や肥満の合併率が高く,糖尿病,肥満の合併例では比較的少量(60~100 g/日)の飲酒で肝硬変に進展している症例が多い.糖尿病,肥満の合併や年齢は,アルコール性肝細胞癌発症の危険因子でもある.
g)アルコール性肝障害の性差:飲酒量が同等の場合には,女性においてアルコール性肝障害が進展しやすい.エストロゲンは,アルコール性肝炎の進展を増強させている可能性がある一方で星細胞活性化を抑制し,肝線維化進展に抑制的に働くことから,閉経によるエストロゲン低下が,女性飲酒者の線維化を促進する可能性も示唆されている.
疫学・発生頻度
近年,戦後から増加を続けていたわが国のアルコールの総消費量は,今世紀に入り若干の減少傾向を示しているが,全肝疾患に占めるアルコール性の比率はむしろ増加していて,約20%の肝疾患に大量飲酒が関与している.問題飲酒者と判定される人数は,300万人超と推計され,さらに肝炎ウイルスに起因する肝疾患の減少に伴い,今後も全肝疾患に占めるアルコール性の割合は増加すると予想される.
肝硬変の成因についての検討では,アルコール単独のものは近年微増し14%を占めるが,アルコール+ウイルス性の症例は6%とこの10年で10%近く激減している.肝細胞癌の成因についての検討でも,アルコール性がその成因の7%を占める.
病理
各病型の病理組織像と定義を以下に示す(表9-8-2).
1)アルコール性脂肪肝(alcoholic fatty liver)(図 9-8-3A):
肝組織病変の主体が,肝小葉の30%以上(全肝細胞の約1/3以上)にわたる脂肪化(fatty change)であり,そのほかには顕著な組織学的な変化は認められない.
2)アルコール性肝線維症(alcoholic hepatic fibrosis)(図9-8-3B):
肝組織病変の主体が,①中心静脈周囲性の線維化(perivenular fibrosis),②肝細胞周囲性の線維化(pericellular fibrosis),③門脈域から星芒状に延びる線維化(stellate fibrosis,sprinkler fibrosis)のいずれか,ないしすべてであり,炎症細胞浸潤や肝細胞壊死は軽度にとどまる.
3)アルコール性肝炎(alcoholic hepatitis)(図9-8-3C):
肝組織病変の主体が,肝細胞の変性・壊死であり,①小葉中心部を主体とした肝細胞の著明な膨化(風船化,ballooning),②種々の程度の肝細胞壊死,③Mallory体(アルコール硝子体),および④多核白血球の浸潤を認める.
Mallory体は,胞体内の雲状構造物で細胞骨格の中間径フィラメントが凝集したもので,アルコール性肝炎の重要な所見であるが,常に出現するわけではない.ミトコンドリアの腫大や巨大ミトコンドリアを伴うことが多い.
4)アルコール性肝硬変(alcoholic liver cirrhosis):
肝の組織病変は,定型例では小結節性,薄間質性である.肝硬変の組織・形態学的証拠は得られなくとも,飲酒状況と画像所見や血液生化学検査から臨床的にアルコール性肝硬変と診断できる.
5)アルコール性肝癌(alcoholic hepatocellular carcinoma):
アルコール性肝障害で,画像診断,または組織診断で肝癌の所見が得られたもので,ほかの病因を除外できたものをアルコール性肝癌と診断する.
臨床症状・臨床所見
アルコールの過飲により最初に起こる疾患は脂肪肝であり,大量飲酒者のほとんどに認められる.症状はほとんどなく,AST,ALTが軽度上昇する例が認められる.
アルコール性肝炎は,飲酒量の増加を契機に発症し,AST優位の血清トランスアミナーゼの上昇や黄疸を認める.著明な肝腫大,腹痛,発熱,末梢血白血球数の増加,ALPやγ-GTPの上昇を認めることが多い.このような所見を伴う場合,臨床的アルコール性肝炎として取り扱う.一部のアルコール性肝炎では,禁酒しても肝腫大などアルコール性肝炎の症状が持続するものもあり,肝性脳症,肺炎,急性腎不全,消化管出血などの合併症を伴う場合は予後不良である.表9-8-3のアルコール性肝炎重症度(JAS)スコアで10点以上の症例は,重症(アルコール性肝炎)であり,積極的な治療介入が必要である.8~9点の症例は10点以上に移行する可能性があり,注意深い経過観察が必要である.3点以上の項目がある場合もその障害に即した早期からの治療介入が望まれる.
肝硬変の臨床症状・臨床所見は,ほかの原因の肝硬変と同様である.
診断・検査所見
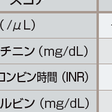
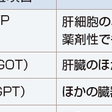
問診による飲酒歴の把握が重要である.大量飲酒を否認し,過少申告するケースが多く,可能なら家族からも飲酒量を調査する. 禁酒による血清AST,ALT,γ-GTP活性の改善が条件である.病型分類は組織学的な診断が最も確実である.診断に有用な血液検査項目としては,γ-GTPやAST/ALT比の上昇が特徴的である.しかし,単一所見でアルコール性肝障害の診断を確定するような有力な検査は存在せず,種々の指標を組み合わせてアルコール性肝障害の診断に至ることになる.診断に有用な検査項目を表9-8-4に示す.脂肪肝,肝硬変では,画像診断も有用である. アルコール性肝癌例では腫瘍マーカーが正常範囲内のことが多く,アルコール性肝障害を認める例では,定期的な画像検査が重要である.
合併症
慢性的な多量の飲酒は,肝臓のみならず全身の臓器障害を引き起こす.肝硬変に伴う食道静脈瘤や肝不全に伴う肝腎症候群,免疫低下に伴う感染症が合併症として重要で,予後にも影響する.脂質異常症,高尿酸血症といった代謝性疾患も引き起こす.
経過・予後
アルコール性脂肪肝は,日本酒換算で1日5合程度(純エタノール換算で約110 g)を1週間続けただけで惹起されるが,2~4週間の断酒で消失する.脂肪肝の状態にある人が,連続大量飲酒を繰り返すと,その約20%にアルコール性肝炎が発症する(図9-8-1).その一部が重症化し重症アルコール性肝炎に至るが,重症アルコール性肝炎の死亡率は,以前は70%以上であったが,治療法が進歩した現在でも40%近くあり,特に消化管出血や腎不全を合併すると予後不良である.
重症化せずに長期に大量飲酒をすると,肝の線維化が進み,アルコール性肝線維症からアルコール性肝硬変に至る場合がある.アルコール性肝硬変は日本酒換算で5合程度以上を20~30年以上続けている人に多発する.ただし,女性の場合はその2/3の飲酒量で,飲酒期間も12~20年程度で肝硬変に至る場合が多い.大量飲酒者のうち10~30%程度の人に発病する.アルコール性肝硬変で飲酒を継続した群は予後不良で,5年生存率は30%程度であるが,断酒した群ではほかの成因による肝硬変症例より予後は良好である.禁酒により改善しない肝不全症例では肝移植も検討すべきであるが,移植後の再飲酒の評価や予防が重要である.再飲酒がなければ移植後の成績は良好である.
アルコール性肝硬変でも,ウイルス性肝炎の合併なしに肝細胞癌を発症する例が少なからず認められる.ステージが進行して発見される症例が多いが,各ステージでの予後はほかの肝細胞癌と差はない.
治療・予防
治療の基本は禁酒であり,その他の療法は補助的である.その予防には,生活習慣病の予防と合わせた生活指導,節酒指導が重要と考えられる.アルコール性肝炎や肝硬変に至るようなアルコール依存症者では,早い段階で肝障害の進展を防止するために,節酒ではなく断酒が必要であり,精神科医や専門医への紹介が推奨される. アルコール性肝障害は栄養障害を伴っていることが多く,ビタミンBの不足がクエン酸回路障害を引き起こし,β酸化の障害を惹起することが示唆されており,ビタミンBの補給が栄養療法と同時に行われる.アルコール性肝硬変の治療法はほかの肝硬変と同様で,腹水や浮腫には利尿薬を投与し,肝不全例では,蛋白制限(0.5~0.7 g/kg/日)をした上で,分岐鎖アミノ酸製剤を投与する.離脱症状には鎮静薬を用いる. 重症アルコール性肝炎では,新鮮凍結血漿を用いた肝補助療法とともに,副腎皮質ホルモンによるサイトカイン産生の抑制や多核白血球除去による救命例の報告が増えている.一般の肝庇護療法では救命率が低く,早期診断と早期からの集学的治療が重要となる.[堀江義則]
■文献
アルコール医学生物学研究会:アルコール性肝障害診断基準2011年版.2012.堀江義則,山岸由幸,他:アルコール関連障害の現状と対策―アルコール性肝障害-.日本医師会雑誌,141: 1864-1868, 2011.中野雅行:アルコール性肝障害の病理・病態生理―病理,最新医学 別冊 新しい診断と治療のABC 62/消化器9 アルコール性肝障害(高後 裕編),pp69-77,最新医学社,東京,2009.
出典 内科学 第10版内科学 第10版について 情報




 アルコール性脂肪肝(せいしぼうかん)
アルコール性脂肪肝(せいしぼうかん)