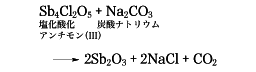酸化アンチモン (さんかアンチモン)
antimony oxide
アンチモンの酸化物の総称で,3種類が知られている。
酸化アンチモン(Ⅲ)antimony(Ⅲ)oxide
化学式Sb2O3。三酸化二アンチモンともいう。アンチモン華および方安鉱として産出する。硫化アンチモンまたはアンチモンを燃焼しても得られるが,空気が十分にあると二酸化アンチモンが混じるので空気を制限して低温で,または1000℃以上の高温で焙焼する。無色の結晶で2種の変態がある。昇華して得られたものは等軸晶系,比重5.2,熱すると570℃付近で斜方晶系,比重5.7へ転移する。融点656℃,沸点1550℃。pH8.6を等電点として両性であり,これよりも高いpHあるいは低いpHで溶解度は増す。等電点における水に対する溶解度は0.0016g/100g(15℃)。濃硫酸,濃塩酸に溶けてアンチモン(Ⅲ)塩,アルカリにより亜アンチモン酸塩となる。プラスチック,繊維の難燃剤,ガラスの清澄剤などに使用。
二酸化アンチモンantimony dioxide
化学式SbO2。白色の粉末。アンチモン,酸化アンチモン(Ⅲ),硫化アンチモンを空気中で熱すると生成する。また700~1000℃に熱すると溶融も揮発もせずに酸素を放出して酸化アンチモン(Ⅲ)に変化する。このように酸素を吸収したり放出したりするので溶融ガラスのガス抜きに用いられる。X線回折実験などによりアンチモン(Ⅴ),アンチモン(Ⅲ)の混合酸化物と考えられている。
酸化アンチモン(Ⅴ)antimony(Ⅴ)oxide
化学式Sb2O5。酸化アンチモン(Ⅴ)ともいう。金属アンチモンを濃硝酸で処理して得られる水和物を脱水すると生成する。淡黄色粉末。完全に脱水することはむずかしい。300℃で分解。水和状態ではコロイド液となる。
執筆者:漆山 秋雄
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
Sponserd by 
酸化アンチモン
さんかあんちもん
antimony oxide
アンチモンの酸化物。次の3種の化合物が知られている。
(1)酸化アンチモン(Ⅲ) 三酸化二アンチモンともいう。天然には方安鉱およびバレンチン鉱として産する。塩化アンチモン(Ⅲ)の加水分解生成物を炭酸ナトリウム水溶液と煮沸すると、無色の立方結晶(方安鉱)が得られる。
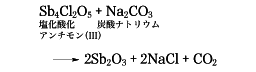
Sb4O6分子が含まれ、1000℃以下の蒸気密度はこれに相当する。570℃で斜方結晶(バレンチン鉱)に転移する。水に難溶だが、塩酸、アルカリに溶ける。アルカリ水溶液に溶けると、亜アンチモン酸イオンSbO2-をつくる。炭素または水素と熱すると金属アンチモンが得られる。白色塗料、不燃化剤に用いられる。
(2)酸化アンチモン(Ⅴ) 五酸化二アンチモンともいう。塩化アンチモン(Ⅴ)の加水分解生成物を275℃で脱水する。黄白色粉末。化学式Sb2O5、式量323.5。300℃で分解して酸化アンチモン(Ⅲ)になる。アルカリ水溶液には溶けてアンチモン酸イオン[Sb(OH)6]-をつくる。無機陽イオン交換体としての用途がある。
(3)酸化アンチモン(Ⅴ)アンチモン(Ⅲ) 四酸化二アンチモンともいう。酸化アンチモン(Ⅲ)を約900℃に熱する。黄色結晶。普通Sb2O4と記されるが、酸化アンチモン(Ⅴ)と酸化アンチモン(Ⅲ)の混合物と考えられ、水、エタノールに難溶。式量307.5。
[守永健一・中原勝儼]
酸化アンチモン(データノート1)
さんかあんちもんでーたのーと
酸化アンチモン(Ⅲ)
Sb2O3
式量 291.5
融点 656℃
沸点 1550℃
比重 5.19(立方晶系)
5.76(斜方晶系)
斜方晶系の構造(無限鎖)
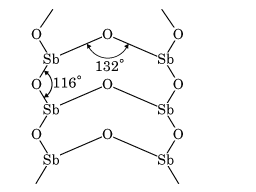
酸化アンチモン(データノート2)
さんかあんちもんでーたのーと
酸化アンチモン(Ⅴ)
Sb2O5
式量 323.51
比重 3.5~4.0
出典 小学館 日本大百科全書(ニッポニカ)日本大百科全書(ニッポニカ)について 情報 | 凡例
Sponserd by 
酸化アンチモン
サンカアンチモン
antimony oxide
天然に得られる低温安定型の方安鉱,高温型のバレンチン鉱はSb2O3を主成分とする.また,セルバンタイトとよばれる黄色の鉱物はSb2O4組成である.【Ⅰ】酸化アンチモン(Ⅲ):Sb2O3(291.50).三酸化二アンチモンともいう.融点656 ℃,沸点1425 ℃.立方晶系(密度5.19 g cm-3)と斜方晶系(密度5.76 g cm-3)の結晶があり,その転移点は約570 ℃ である.電子材料,難燃加工剤,重合触媒,還元剤,光学レンズの清澄剤,ほうろうなどに用いられる.[CAS 1309-64-4]【Ⅱ】酸化アンチモン(Ⅴ):Sb2O5(323.50).五酸化二アンチモンともいう.金属アンチモンと濃硝酸の反応で得られるSb2O5水和物を,350 ℃ で脱水すると無水物が得られる.白色の粉末.密度3.78 g cm-3.水にはわずかに溶け,酸性を示す.約450 ℃ で分解しはじめ,700~900 ℃ の間では四酸化二アンチモンSb2O4組成のものになり,1200 ℃ 以上では三酸化二アンチモンSb2O3となる.顔料原料,難燃加工剤,無機陽イオン交換体などに用いられる.[CAS 1314-60-9]【Ⅲ】四酸化二アンチモン.Sb2O4(307.50).SbⅢと SbⅤの混合酸化物とみられる.三酸化二アンチモンを空気中で400 ℃ に長時間加熱すると,Sb2O4組成の酸化物となる.このように,500~1200 ℃ の間で酸素を吸収したり放出したりするので,融解ガラスのガス抜きのための清澄剤として用いられる.[CAS 1332-81-6]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
Sponserd by 
酸化アンチモン
さんかアンチモン
antimony oxide
(1) 酸化アンチモン (III) Sb2O3 。方安鉱,バレンチン鉱として産出する。無色の結晶で,熱すると黄色になる。融点 656℃。 (2) 酸化アンチモン (IV) Sb2O4 。セルバンテス鉱として産出する。無色ないし淡黄色固体。 (3) 酸化アンチモン (V) Sb2O5 。黄白色粉末。加熱すると 780゜で Sb2O4 になる。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
Sponserd by 
世界大百科事典(旧版)内の酸化アンチモンの言及
【酸化アンチモン】より
…アンチモンの酸化物の総称で,3種類が知られている。
[酸化アンチモン(III)antimony(III) oxide]
化学式Sb2O3。三酸化二アンチモンともいう。…
【酸化アンチモン】より
…アンチモンの酸化物の総称で,3種類が知られている。
[酸化アンチモン(III)antimony(III) oxide]
化学式Sb2O3。三酸化二アンチモンともいう。…
※「酸化アンチモン」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
Sponserd by