翻訳|actin
精選版 日本国語大辞典 「アクチン」の意味・読み・例文・類語
日本大百科全書(ニッポニカ) 「アクチン」の意味・わかりやすい解説
アクチン
あくちん
actin
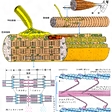
筋肉を構成する主要なタンパク質の一種。動物の大きな特徴の一つである運動の原因をなすのは、筋肉の収縮、弛緩(しかん)であるが、アクチンはミオシンと並んで、その筋収縮系の基本をなす物質の一つである。発見は1942年であるが、当時すでにミオシンは筋収縮の立役者と考えられており、ATP(アデノシン三リン酸)によってミオシンが収縮する条件をみつけようとする試みがハンガリーのストラウブB. F. Straub(1914―1996)によってなされた。しかし、ATPを加えただけではミオシンの収縮はみられず、これに新たなタンパク質を加えて初めて収縮するということが発見された。このタンパク質がアクチンであり、ミオシンに活性activityを与えるという意味でアクチンと命名された。筋肉から塩化カリウム溶液でミオシンを抽出したあとアセトンで乾かし、水で抽出すると得られるのがG-アクチン(分子量はウサギ骨格筋由来のアクチンで約4万2000。ほぼ球状をなし直径約55オングストローム)である。このG-アクチンは1分子につきATPとカルシウムを各1分子ずつ強く結合している。G-アクチンに中性塩を加えると重合して二重螺旋(らせん)フィラメントを形成するが、これがF-アクチンである。このときATPからリン酸が1個とれてADP(アデノシン二リン酸)となる。塩を除けばG-アクチンに戻るがATPがないとG-アクチンは変性する。F-アクチンは、G-アクチンが数珠(じゅず)のように重合したものが二重螺旋をなしている。天然には1マイクロメートルの長さで存在しているが、ガラス器内ではいろいろな長さを示す。筋肉以外でも、粘菌(変形菌類。動物と植物との境界に位置する生物)の変形体で発見(1966)されて以来すべての生物の細胞からみいだされており、その一次構造は種を問わずよく似ている。G-アクチン、F-アクチン間の相互転換は大きな特徴の一つであるが、種々のアクチン調節タンパク質により分子の重合・脱重合およびフィラメントの長さや安定性が調節される。非筋細胞では、細胞骨格が細胞構造を保持するとともに、細胞運動、分裂、形態変化など多くの機能を果たしている。この細胞骨格を形成する線維構造の一つがミクロフィラメント(マイクロフィラメント)であるが、これはアクチンフィラメントともよばれ、アクチンを主成分としている。
[飯島道子]
『丸山工作著『アクチンと調節タンパク質』(1986・東京大学出版会)』▽『上代淑人・矢原一郎編『細胞増殖・細胞運動』(1989・丸善)』▽『新井健一編『水産動物筋肉タンパク質の比較生化学』(1989・恒星社厚生閣)』▽『神谷律・丸山工作著『細胞の運動』(1992・培風館)』▽『James Darnell他著、野田春彦他訳『分子細胞生物学』下(1993・東京化学同人)』▽『岡山繁樹著『生物科学入門――分子から細胞へ』(1994・培風館)』▽『B・アルバーツ他著、中村桂子他監修『細胞の分子生物学』第3版(1995・教育社)』▽『馬渕一誠・山本正幸編『英語論文セミナー 現代の細胞生物学』(1996・講談社)』▽『日本水産学会監修、西田清義編『魚貝類筋肉タンパク質――その構造と機能』(1999・恒星社厚生閣)』▽『宝谷紘一・神谷律編『細胞のかたちと運動』(2000・共立出版)』▽『日本水産学会監修、関伸夫・伊藤慶明編『かまぼこの足形成――魚介肉構成タンパク質と酵素の役割』(2001・恒星社厚生閣)』▽『竹縄忠臣編『細胞骨格と細胞運動――その制御のメカニズム』(2002・シュプリンガー・フェアラーク東京)』▽『R・K・マレー他著、上代淑人・清水孝雄監訳『ハーパー生化学』原書28版(2011・丸善)』
改訂新版 世界大百科事典 「アクチン」の意味・わかりやすい解説
アクチン
actin
筋肉を構成するタンパク質の一つ。分子量4万1785の球状の分子で,ある条件下では重合し糸状に長く連なる。前者をGアクチン,糸状に連なった後者をFアクチンという。1942年,ハンガリーのストラウプStraub Ferenc Brunó(1914-96)によって発見された。FアクチンはGアクチンの二重らせんからなり,筋肉(骨格筋)の細いフィラメント(Iフィラメント)の主成分である。筋肉の収縮は,このフィラメントを形成するアクチンと太いフィラメント(Aフィラメント)を形成するミオシンとの間の反応によっておこる。アクチンは,筋肉以外の種々の細胞にも広く分布し,細胞分裂,アメーバ運動,原形質流動などに関与する。これらの細胞では,筋肉と異なり,アクチンはつねにFアクチンのフィラメントとして存在しているのではなく,たとえば細胞分裂の際には細胞のくびれの部分の表層に,原形質流動の際には活発に流動のみられる部分にFアクチンが多数出現する。つまり,これらの細胞では,GアクチンとFアクチン間の変換(G-F変換)が絶えずおこっていると考えられる。
→筋収縮
執筆者:杉 晴夫
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「アクチン」の解説
アクチン
アクチン
actin
筋肉細胞内の筋原繊維を構成している二つのフィラメントのうち,細いフィラメントをおもに構成している筋肉タンパク質.球状(G)と繊維状(F)の二つの型がある.F-アクチンはファロイジンで染色される.G-アクチンは Mg2+ とともに中性塩を加えるか,または溶液を弱アルカリ性か弱酸性にすると重合してF-アクチンになり,同時にG-アクチン1分子当たり1個結合していたATPがADPとなる.塩を取り去ると可逆的にG-アクチンになる.ミオシンと結合してアクトミオシンを形成しミオシンATPアーゼ活性を増大させ,ミオシンATPアーゼを Mg2+ で活性化されるATPアーゼにかえる.ウサギの骨格筋から得られたG-アクチンは分子量4.6×104 の球状タンパク質でプロリン含量が高く,7個のシステインと異常アミノ酸であるε-N-メチルリシンを1個含む.[CAS 132579-20-5]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「アクチン」の意味・わかりやすい解説
アクチン
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「アクチン」の意味・わかりやすい解説
アクチン
actin
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「アクチン」の解説
アクチン
世界大百科事典(旧版)内のアクチンの言及
【ATPアーゼ】より
…すなわち生体は,常になんらかの物理的仕事に対するエネルギーの供給と共役したかたちでATPを分解するように造られており,ATPがむだに加水分解されることはない。たとえば筋肉の収縮タンパク質であるミオシンは機械的仕事と共役したATPアーゼの一つであり,反応過程におけるそれ自身の高次構造変化やアクチンとの相互作用などを通じて,ATPのエネルギーを筋収縮の仕事に変換する機能をもっている。一方,筋小胞体と呼ばれる筋肉の細胞器官の膜に大量に存在する別種のATPアーゼは,ATPの分解に先立って細胞質中のCa2+イオンを強く結合し,小胞体内のCa2+濃度が細胞質より高い場合でも,ATPの分解とともにそれを膜の内腔に輸送する性質を示す。…
【筋収縮】より
…平滑筋の収縮は交感神経と副交感神経によって調節されており,一方が収縮を他方が弛緩をおこすが,そのしくみには不明な点が多い。
[脱分極と収縮との関係]
筋収縮は,筋フィラメントを形成するタンパク質アクチンとミオシン間の反応によるものであり,このエネルギー源はATPである(図2)。静止状態の筋肉では,アクチンとミオシン間の反応がトロポミオシンおよびトロポニンというタンパク質によって抑制されているので収縮はおこらない。…
※「アクチン」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...