改訂新版 世界大百科事典 「フリーデルクラフツ反応」の意味・わかりやすい解説
フリーデル=クラフツ反応 (フリーデルクラフツはんのう)
Friedel-Crafts reaction
芳香族化合物にアルキル基またはアシル基RCO-を導入する反応。1877年,フランスのフリーデルCharles Friedel(1832-99)とアメリカのクラフツJames Mason Crafts(1839-1917)の2人の共同研究で発見された。アルキル化とアシル化の2種の反応が知られているが,いずれも触媒として塩化アルミニウムAlCl3のような強いルイス酸を必要とする。
(1)アルキル化 ベンゼンなどの活性化されたベンゼン核を有する芳香族炭化水素は塩化アルミニウムの存在下でハロゲン化アルキルと反応して,アルキルベンゼンを与える(式(1))。ハロゲン化アルキルとして通常は塩化物が用いられる。
この反応には,ふつう三つの段階がある。最初の段階では,触媒がハロゲン化アルキルと反応して,式(2)に示すようなアルキルカチオンを生成する。このアルキルカチオンは反応系中に微量存在し,出発物質と平衡にある。
このカチオンは非常に求電子的で,ベンゼン環と反応して,新たに別のカチオン中間体を生成する(式(3))。
このカチオンはプロトンを放出して,式(4)のように炭化水素を生成する。
その際放出されるプロトンは式(2)で生じた四塩化アルミニウムアニオンにトラップされて塩酸となる。
この反応機構で推察されるように,アルキルカチオンが生成すればベンゼン環のアルキル化が起こる。たとえば,塩化アルミニウムの代りに,臭化アルミニウムAlBr3,フッ化ホウ素BF3,塩化鉄(Ⅲ)FeCl3,塩化亜鉛ZnCl2などの触媒が有効であり,オレフィンをプロトン化して生成するカチオン(プロトン化試剤としてフッ化水素HF,硫酸H2SO4などが使われる)をベンゼン環と反応させる別法も考案されている。アルコールから生成するアルキルカチオンなどもフリーデル=クラフツ反応に使われる。ニトロベンゼンなどのように,ベンゼン環が不活性化されている場合にはこのようなアルキル化は起こらない。実際ニトロベンゼンはフリーデル=クラフツ反応の溶媒に使われることがある。
フリーデル=クラフツ反応によるアルキル化では,生成するアルキルベンゼンのベンゼン環がアルキル基により活性化され,求核的になっているので,さらにアルキル化が進行して多重アルキル化が副反応として起こる。また,用いるハロゲン化アルキルの種類によっては式(5)に示すように,アルキル基の転位生成物が主生成物となる。これらの反応はアルキルベンゼンの非常に重要な工業的合成法となっている。
(2)アシル化 ベンゼン環のアシル化は酸塩化物をアシル化剤として用い,同様に塩化アルミニウムを触媒として行われる(式(6))。
この反応では,まず酸塩化物と塩化アルミニウムとの反応により,アシリウムイオンが生成する(式(7))。
これがベンゼン環を求電子的に攻撃して,カチオン中間体を生成するが,これが脱プロトンしてアシルベンゼンが生成する(式(8))。
ここで生成するアシルベンゼンはアシル基の強い電子求引性により,求電子置換反応に対して不活性化されているので,さらにアシル化反応が進行することはない。したがって,フリーデル=クラフツ反応によるアシル化は副反応が少ない。
トルエンなど,置換ベンゼン系ではアシル化の反応位置が3ヵ所あり,異性体が3種類生成する可能性があるが,パラ置換体が優先して生成する(式(9))。オルト位はメチル基があるため,立体的に込み合っており,アシリウムイオンが接近しにくいことが一つの大きな原因と考えられる。
酸塩化物の代りに,酸無水物を用いて同様の条件下で反応させてもフリーデル=クラフツ反応が進行し,酸塩化物の場合と同様の生成物が得られる。また,この反応では,塩化アルミニウムは触媒として作用しているので,原理的には触媒量あれば十分であるが,反応速度を適当に上げるためには1当量以上用いる必要がある。フリーデル=クラフツ反応は分子内環化反応にも使われる(式(10))。
執筆者:友田 修司
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「フリーデルクラフツ反応」の意味・わかりやすい解説
フリーデル‐クラフツ反応
ふりーでるくらふつはんのう
Friedel-Crafts reaction
ベンゼンなどの芳香環を、無水塩化アルミニウムの存在下でハロゲン化アルキルによりアルキル化する反応(式(1))、およびハロゲン化アシルによりアシル化する反応(式(2))をいう。有機合成化学のきわめて重要な反応の一つ。

1877年にフランスのフリーデルとその共同研究者であるアメリカのクラフツJames Mason Crafts(1839―1917)が、ペンテンを得る目的で、ベンゼン溶液中で塩化ペンチルに塩化アルミニウムを作用させたところ、ベンゼンの芳香環のアルキル化がおこってペンチルベンゼンが生成することをみいだした。2人はこのアルキル化反応の研究を進め、芳香環をアルキル化する一般的方法を確立した。この反応を拡張して、塩化アルミニウムの存在下でベンゼンと塩化アセチルとを反応させてアセトフェノンを合成するアセチル化反応にも成功し、多くのアシル化反応に応用した。
塩化アルミニウムのほかに、臭化アルミニウム、塩化スズ(Ⅳ)、フッ化アンチモン(Ⅴ)、フッ化ホウ素、塩化亜鉛などのルイス酸(アメリカの物理化学者G・N・ルイスの定義した酸)や濃硫酸、ポリリン酸などのプロトン酸が触媒として有効である。アルキル化試薬にはハロゲン化アルキルのほかオレフィン、アルコール、エステルが用いられ、アシル化試薬にはカルボン酸無水物も用いられる。反応機構は、ルイス酸により生成する炭素陽イオンあるいはアシル陽イオンによる芳香環の求電子置換であり、アルキル化では二つ以上のアルキル置換の可能性があるが、アシル化の場合にはアシル基が一つ入ると芳香環が不活性化されて反応しにくくなるので、アシル基は一つしか入らない。芳香環以外にオレフィンの二重結合でも塩化アルミニウムによる求電子置換がおこり、ルイス酸によるオレフィンの重合も広義にはこの反応に属する。
[湯川泰秀・廣田 穰 2015年7月21日]
化学辞典 第2版 「フリーデルクラフツ反応」の解説
フリーデル-クラフツ反応
フリーデルクラフツハンノウ
Friedel-Crafts reaction
無水塩化アルミニウムAlCl3を触媒にして芳香族化合物をハロゲン化アルキルによってアルキル化したり,ハロゲン化アシルまたは酸無水物によってアシル化する反応.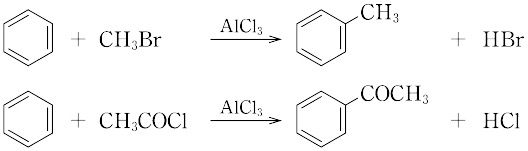 AlCl3のほかに,SbCl3,SnCl4,ZnCl2,BF3,P2O5,HF,H2SO4,P2O5なども触媒として用いられる.また,アルケン,アルコールなどによってアルキル化したり,エステルによってアシル化することもできる.合成反応として広く利用され,工業的にも重要である.
AlCl3のほかに,SbCl3,SnCl4,ZnCl2,BF3,P2O5,HF,H2SO4,P2O5なども触媒として用いられる.また,アルケン,アルコールなどによってアルキル化したり,エステルによってアシル化することもできる.合成反応として広く利用され,工業的にも重要である.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「フリーデルクラフツ反応」の意味・わかりやすい解説
フリーデル=クラフツ反応
フリーデル=クラフツはんのう
FriedelCrafts reaction
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
世界大百科事典(旧版)内のフリーデルクラフツ反応の言及
【無水酢酸】より
…この反応はセルロースの水酸基のアセチル化にも適用できる。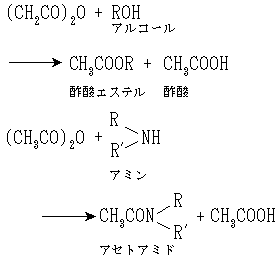 また塩化アルミニウムを触媒にしてベンゼンと反応させるとアセトフェノンが得られる(フリーデル=クラフツ反応)。酢酸ナトリウムの存在下にベンズアルデヒドと反応させるとケイ皮酸を生じる(パーキン反応)。…
また塩化アルミニウムを触媒にしてベンゼンと反応させるとアセトフェノンが得られる(フリーデル=クラフツ反応)。酢酸ナトリウムの存在下にベンズアルデヒドと反応させるとケイ皮酸を生じる(パーキン反応)。…
※「フリーデルクラフツ反応」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

