精選版 日本国語大辞典 「芳香族化合物」の意味・読み・例文・類語
ほうこうぞく‐かごうぶつハウカウクヮガフブツ【芳香族化合物】
日本大百科全書(ニッポニカ) 「芳香族化合物」の意味・わかりやすい解説
芳香族化合物
ほうこうぞくかごうぶつ
aromatic compound
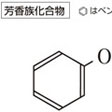
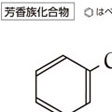
すべての有機化合物は、脂肪族化合物と芳香族化合物に大別され、「芳香族化合物」はベンゼン環に代表されるような芳香族性を有する環をもつ化合物の総称である。
[廣田 穰 2016年2月17日]
芳香族化合物の発見とベンゼンの構造式
芳香族化合物の名前の変遷
芳香族の名称が使われるようになったのは、植物から天然化合物を分けて取り出すことが有機化学とされていた19世紀前半の時代にさかのぼる。この時代にはまだ有機化合物の化学構造という概念がはっきりしていなかったので、自然界の植物などから得られた有機化合物のうちに、冬緑油(とうりょくゆ)(ウィンターグリーン油)、バニリン、桂皮(けいひ)油、アニス油などの「芳香をもつ一群の化合物」があることに化学者たちが気づき、これらを芳香族化合物とよぶようになった。のちに、これらの芳香をもつ化合物の多くがベンゼン環をもつという共通点があることが知られたので、「ベンゼン環などの芳香環をもつ化合物」を芳香族化合物と分類するようになった。この過程で、芳香族の名前は、化合物が「よい香りをもつという性質」には直接は関係ないことになり、それ以前には芳香族とされていた芳香をもつハッカ、ピネン、樟脳(しょうのう)などはベンゼン環がないという理由から脂肪族に分類されることになった。
[廣田 穰 2016年2月17日]
ベンゼンの発見と構造式
芳香族化合物の構造の解明は、1825年イギリスのM・ファラデーが、鯨油を熱分解して得られた油の一成分として、芳香をもつ一つの化合物(現在のベンゼン)を発見したことから始まった。さらに1833年にドイツのE・ミッチェルリヒは、安息香酸benzoic acidを石灰といっしょに加熱・蒸留して同じ物質を得るのに成功し、これをベンジンBenzinと名づけた。現在使われているベンゼンbenzeneの名はドイツのA・W・ホフマンによる。ベンゼンがC6H6の組成をもつと決定したのは、1835年ミッチェルリヒであるが、このベンゼンの組成は、脂肪族化合物に比べると、きわめて不飽和度の高い化合物(炭素に比べて水素の比率が低い化合物のこと)で、当時の常識からいうと化学反応を受けやすい不安定な化合物と考えられた。それにもかかわらず、実在のベンゼンは安定で、付加反応ではなく置換反応を行うなど特異な性質を示したので、化学者の興味を集めた。1845年にホフマンがコールタールから多量のベンゼンを単離するのに成功してからは、実験も容易にできるようになり、ベンゼンの研究が盛んになった。
ドイツのF・A・ケクレは、1865年に当時の炭素の原子価の概念を基礎として、ベンゼンに対して6個の炭素原子からなる六角形の環をもち、単結合C-Cと二重結合C=Cが交互に並んだケクレの構造式(古典的なケクレの構造式)を提案した()。しかし、の(Ⅰ)または(Ⅱ)のいずれか一つだけではベンゼンの化学的性質を十分に説明できなかったので、1872年に、ベンゼン分子はこの二つの構造の間を振動していて、分離することのできない非常に速い平衡が存在するという考えに到達した。この考えによれば、ベンゼン環が平面構造を形成し、6個の炭素原子が等価であり、二重結合は位置が局限されず、またベンゼンの炭素環の結合は脂肪族の二重結合とは性質の異なるものであり、ベンゼンが高度の対称性をもつことが理解できる。ベンゼン環のもつこのような特異な安定性は「芳香族性」とよばれている。
ベンゼンの構造に関してはその後も多くの提案がなされたが、原子価の概念が確立していない当時では、当然のことながら満足できる構造の説明は得られなかった。そのなかで1890年にドイツのバンベルガーEugen Bamberger(1857―1932)が発表した6中心原子価構造と、1899年に同じくドイツのF・K・J・ティーレが提案した炭素原子部分原子価構造は、両者とも炭素原子の4番目の原子価の置き場所に特徴がある点で、注目に値する()。
20世紀になって有機反応における電子の挙動が明らかになるに及んで、1925年にはイギリスのR・ロビンソンにより芳香族六隅子説が提案された。これはベンゼン環の芳香族性の核心に迫るもので、ベンゼンが付加反応よりも置換反応を受けやすいのは、6個の電子の集合によるという説である。六隅子説によると、ベンゼンのみならず、ピリジンやピリミジンなどの6員環複素環式化合物や、ピロール、フラン、チオフェンなどの5員環複素環式化合物の芳香族性を普遍的に説明できる。
[廣田 穰 2016年2月17日]
芳香族性の理論――π(パイ)電子の非局在化
ヒュッケルの4n+2則とπ電子系の安定性">ヒュッケルの4n+2則とπ電子系の安定性
芳香族性の真の解明は、1931年にドイツのE・A・A・J・ヒュッケルにより提案された量子力学理論によって完成された。ヒュッケルは、分子軌道法(ヒュッケルMO法)による近似計算で、環状共役不飽和系ではπ電子の数が(4n+2)個のときに縮重分子軌道(等エネルギーの分子軌道が二つ以上あることを「縮重」という。を参照)が完全に電子で満たされた状態になり、分子が安定化することを示して、ベンゼンの安定性を解明した。この法則を「ヒュッケルの4n+2の法則」という(ヒュッケル則、4n+2則などともよばれる)。ベンゼンは6個のπ電子をもち、4n+2則のn=1の場合に相当する。環状のπ電子系であっても、π電子数4のシクロブタジエンやπ電子数8のシクロオクタテトラエンが芳香族性を示さないのは、π電子数がこの法則から外れているからである。ヒュッケル則はπ電子数が4n個の環状共役不飽和化合物は不安定な反芳香族化合物であると予測している。
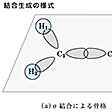
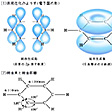
ここで重要なことは、炭素は4価であるので、ベンゼンの場合のように一つの水素原子と両隣の二つの炭素原子とσ(シグマ)結合をつくっても、なお一つの価電子(結合をつくる手)が残ることである。この価電子はp軌道(炭素の場合2p軌道)に入っていて、π結合を形成するのに使われている。π結合を構成しているp電子は、の(b)にあるように、軸が分子面に垂直な亜鈴(あれい)形をしていて、軌道の側面の重なり合いにより結合しているので、同時に二つないしは三つの隣接する他のp軌道と結合することが可能である。の(1)のベンゼンでは一つのp軌道(正確には2p原子軌道)が両隣のp軌道と結合して輪になって、6員環のπ電子系を構成している。このようなπ結合の特性により、π電子系を長い鎖や環などの不飽和系全体に広げることができる。これをπ電子の非局在化といい、π電子が、環を構成する不飽和原子(sp2混成)上を自由に動き、環を構成する全原子に分布することを可能にしている。
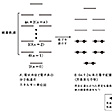
環状π電子系について、π分子軌道のエネルギーを計算すると、のような分子軌道のエネルギー準位図が得られる。これらの分子軌道に最低エネルギーの軌道から順に電子を満たしていって、二重縮重した最高被占軌道(電子が入っている軌道の内でエネルギーが最高のもの)の両方に2個ずつの電子が入り「完全に満たされた状態」になるとエネルギー的に非常に安定になる。これがπ電子数(4n+2)のときに相当し、環状π電子系が芳香族性を示す電子配置である。
ヒュッケル則によれば、nが1以外の(4n+2)π環状共役不飽和化合物、すなわちπ電子数が6だけでなく2、10、14、18、……である場合でも、芳香族性をもつことが予見された。この予見の正しさはその後の諸研究、たとえば日本の野副(のぞえ)鉄男のヒノキチオールの研究(1940)や、アメリカのブレスローRonald Breslow(1931― )、デーリングWilliam von Eggers Doering(1917―2011)によるシクロプロペニウムイオン(1957)や、トロピリウムイオン(1954)の発見と合成により証明された。また、1959年以降、大環状芳香族化合物がイギリスのソンドハイマーFranz Sondheimer(1926―1981)らによって合成されていて、ヒュッケルの予測したとおり、6員環のベンゼン系以外に、10員環、14員環、18員環などの非ベンゼン系芳香族化合物の存在が実証されて、4n+2則が実験的に裏づけられた。
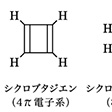
π電子数が4nのときは、二重縮重した最高被占軌道にそれぞれ電子1個が入り()、電子対をつくっていないのでラジカルの性質が強く、不安定で、反応性が高くなる。このような電子配置をとっているのが、4π電子のシクロブタジエン、8π電子のシクロオクタテトラエンなどの反芳香族化合物である()。
[廣田 穰 2016年2月17日]
ベンゼン環の幾何構造と芳香族性
芳香族の基本骨格であるベンゼン環の構造は、現在ではX線回折法や電子線回折法により明らかにされていて、炭素原子間の結合角(∠CCCと∠CCH)はどちらも120°、炭素原子間の結合距離はすべて等しく0.1399ナノメートルであり、6個の水素原子と6個の炭素原子はすべて同一平面上にあって6個の炭素原子は正六角形をなしていることがわかっている(の(2))。ベンゼンのC-C結合距離は脂肪族のエタンの単結合距離0.154ナノメートルより短く、エチレンの二重結合距離0.134ナノメートルより長く、単結合と二重結合の中間である。ここに述べたベンゼン環の平面性と結合距離もベンゼンのπ電子の非局在化により説明でき、これが芳香族性の根源になっている(「ベンゼン」の項目を参照)。
まとめると、すべての芳香族化合物は平面構造の環状共役不飽和系をもっていて、かつ環を構成するπ電子数が(4n+2)個である。
芳香族化合物の特徴を要約すると次のようになる。
(1)共役不飽和結合系が環状平面構造を形成し、その系に属するすべてのπ電子が系の炭素原子上を自由に移動して、環を構成する原子全部に分散していること。このような状態をπ電子が非局在化(共鳴理論の「共鳴」に相当)しているという。非局在化に伴い環を構成する二重結合と単結合の結合距離の差は少なくなる(結合交替が小さくなる)。
(2)非局在化しうるπ電子の数が(4n+2)個でヒュッケル則を満足していること。ヒュッケル則では、環状π電子系の分子軌道論に基づいて、環状π電子系の電子数が(4n+2)個のときにはπ電子エネルギーは低くなり安定化することを示している。
(3)反応性からみると、ベンゼンは形式上環内に3個の二重結合をもつにもかかわらず、付加反応や酸化・還元などのベンゼンのπ電子系が壊れる化学反応を受けにくく、かわりにベンゼン環が保持されたままベンゼン環上の水素が他の原子と置き換わる置換反応(芳香族置換反応という)がおこりやすいという特徴的な性質をもつ。
このような性質は芳香族化合物に共通の特性として知られていて、「芳香族性」とよばれる。
[廣田 穰 2016年2月17日]
芳香族化合物の分類
ベンゼン環を母体とするベンゼン系芳香族化合物のほかに、環を構成する原子として炭素原子以外のヘテロ原子(異原子)を含む複素環式芳香族化合物(複素芳香族化合物ともいう)が多数知られている。また、ベンゼンを母体としない、すなわち6員環以外の芳香族性をもつ炭素環により構成されている非ベンゼン系芳香族化合物もある()。
[廣田 穰 2016年2月17日]
ベンゼン系芳香族化合物
ベンゼンおよびベンゼン環が他の炭素環と縮合した多環式化合物とそれらの誘導体の総称である。
にあるようなベンゼン置換体は、すべてベンゼン系芳香族化合物で、ベンゼン環上に存在する置換基名をつけて命名する。また、二置換体になるとオルト、メタ、パラの3種の異性体が存在する。これらの置換体は芳香族に特有の求電子反応により、母体のベンゼンから芳香環を保持したままで合成できる。
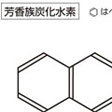
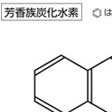
2個の環が2個の隣接した炭素原子を共有しているのが縮合多環式化合物で、縮合している環のうち一つ以上が芳香環である化合物は縮合多環式芳香族化合物(縮合多環芳香族化合物ともいう)である。重要なものとして、ナフタレン、テトラリン、アントラセン、フェナントレン、ピレンなどがある。縮合している環の数が多い縮合多環式芳香族化合物には発癌(はつがん)性を有するものがいくつか知られている。ベンゾ[a]ピレンなどがその一例である。
工業的には、ナフタレン、アントラセンなどは石炭タールから分離して製造するが、ベンゼン、トルエン、キシレンなどはナフサを原料として接触的改質(リフォーミング)法により製造されている。また高級アルキルベンゼンやその他の誘導体は、ベンゼンなどの芳香族化合物を、芳香族求電子置換反応を利用しアルキル化して合成される。にベンゼンおよびその誘導体の代表的な芳香族置換反応を示す。これらの反応では、反応のおこる位置と反応性は前から環についている置換基によって決まる。アルキル基、ヒドロキシ基、アミノ基などは置換反応を活性化する置換基として作用し、反応が速くなり、オルトおよびパラ置換体を優先的に与える。これに対しニトロ基、カルボン酸基、スルホン酸基は不活性基として作用し、反応は遅くなり、主としてメタ置換体を生成する。
高温で触媒を使うような過激な条件下では、ベンゼン環上のハロゲンやスルホン酸基を他の置換基に置き換えることもできる。この反応はベンゼン環の求核置換反応であり、環のニトロ置換基がオルトおよびパラ位での反応を活性化する()。
[廣田 穰 2016年2月17日]
非ベンゼン系芳香族化合物
ヒュッケルの4n+2則を満たす化合物は、ベンゼンに代表される6員環化合物ばかりでなく、7員環、5員環、4員環などの化合物からもみいだされる()。たとえば、シクロペンタジエニル陰イオンや、シクロヘプタトリエニル陽イオンはπ電子数が6でヒュッケル則を満たす。また、8員環や9員環の中環状化合物でもn=2にあたる10個のπ電子をもつ芳香族化合物が知られている。また、3員環でn=0の場合がシクロプロペニル陽イオンである。これらの化合物はいずれも、X線回折により平面正多角形構造で環を構成する各炭素原子が等価であるという芳香族化合物の条件を満たすことが確認されている。
ヒュッケル則で予測されたnが3以上の大環状の共役ポリエンの芳香族性にも関心が集まり、1962年には、ソンドハイマーによって18個の環状π電子系(n=4)をもつ[18]アヌレンが合成され、続いて[14]アヌレン(n=3に相当)、[22]アヌレン(n=5に相当)も合成された。環が大きくなるにつれて、炭素環のひずみが増すこと、環を構成する炭素のp軌道間の重なりが悪くなること、熱振動による変形が大きくなることなどにより、分子全体が平面を保ちにくくなる。このような理由により、環が大きくなると芳香族性が減少してしまうので、安定性が減少することが知られている。
[廣田 穰 2016年2月17日]
複素芳香族化合物
複素環式化合物とは、炭素以外の元素を環内に含む環式化合物を意味する。したがって環内に窒素、酸素、硫黄(いおう)、リンなどの異原子を含む芳香族化合物が、これに属する。ポルフィリンなどの中・大環状化合物に属する複素芳香族化合物が注目されるようになっているが、重要なものは6π電子系のものが多く、6員環化合物と5員環化合物に分類される。前者の代表はピリジンやピリミジンなどのπ電子不足型(π電子欠乏型)の化合物である。後者の代表はピロール、フラン、チオフェンなどの電子過剰型の化合物であり、求電子置換反応を受けやすい。キノリンのように複素芳香族のピリジン環と炭素芳香族のベンゼン環の両方をもつ化合物は通常、複素芳香族化合物に分類される(「複素環式化合物」の項目を参照)。
有機化合物のなかで、複素環式化合物の占める位置は大きく、たとえば医薬・農薬・染料・写真材料・高分子材料などの合成原料や中間体として重要である。さらに天然物として存在する生理活性物質や、生体での代謝物質も複素芳香族化合物を含むものが多い。たとえばビタミン類、補酵素、光合成色素のクロロフィル、血液中のヘモグロビンや、その分解産物である胆汁色素・核酸塩基などは、いずれも単環式または多環式の含窒素芳香族化合物である。
[廣田 穰 2016年2月17日]
『佐々木正著『複素環式化合物の化学』(1972・東京化学同人)』▽『西脇太郎三衛門著『ヘテロ環化学序説』(『現代の化学シリーズ17』1973・講談社)』▽『日本化学会編『新しい芳香族系の化学』(『化学総説 15』1977・日本化学会)』▽『土屋隆・小泉徹・熊懐稜丸著、梅沢文輔編『基礎有機化学』改訂第2版(1991・南江堂)』▽『H・ハート著、秋葉欣哉・奥彬訳『基礎有機化学』改訂版(1994・培風館)』▽『大嶌幸一郎著『基礎有機化学』(2000・東京化学同人)』▽『水野一彦・吉田潤一編著『役にたつ化学シリーズ5 有機化学』(2004・朝倉書店)』
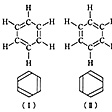
ケクレの6員環構造〔図A〕
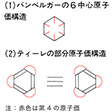
6中心原子価構造と部分原子価構造〔図B…
環状共役π電子系のエネルギー準位と芳香…
エチレンの共有結合〔図D〕
ベンゼン分子〔図E〕
反芳香族化合物の例〔図F〕
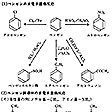
ベンゼンおよびベンゼン誘導体の求電子置…
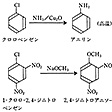
ベンゼン誘導体の求核置換反応〔図H〕
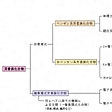
芳香族化合物の分類〔表1〕

非ベンゼン系芳香族化合物〔表2〕
改訂新版 世界大百科事典 「芳香族化合物」の意味・わかりやすい解説
芳香族化合物 (ほうこうぞくかごうぶつ)
aromatic compound
ベンゼン環,またはベンゼン環が2個以上縮合した環をもつ化合物をいう。ベンゼン,ナフタレンのように炭素と水素のみからできている芳香族炭化水素と,その水素の一部を官能基で置換した誘導体が含まれる。また環をつくる炭素原子の一部が炭素以外の原子で置換されたたとえばピリジンなどの芳香族複素環式化合物とその誘導体も多い(図)。芳香族化合物という名称は歴史的なものであり,19世紀前半までに知られていたこの化合物の多くは,精油やバルサムなどの芳香物質から得られていたためである(たとえば安息香酸はバルサムの一種である安息香から得られた)。有機化合物の構造理論が未発達であったこの時代までは,比較的よくわかっていた脂肪族化合物に比べて〈炭素に富んでいる〉ことがその特徴とされていた。1865年F.A.ケクレは,これらの化合物には6個の炭素原子が交互に二重結合と単結合で結合してつくる環構造が存在すると仮定すれば,それまで未解決であった問題がすべて解決しうることを示した。そのころからコールタール中に含まれている芳香族化合物を原料とする化学工業とくに合成染料工業が盛んとなり,芳香族化合物の化学もそれにともなって急速な発展をとげた。
ベンゼン環はきわめて安定な環であり,芳香族化合物は脂肪族化合物や脂環式化合物とは異なる反応性をもつ。この性質を芳香族性とよぶ。芳香族性の起源に関しては議論があったが,1938年ドイツのヒュッケルErich Armand Arthur Joseph Hückel(1896-1980)が分子軌道法によってその説明に成功した。6員環化合物だけではなく,炭素以外の原子を含む5員環共役不飽和化合物(たとえばピロール)にも弱い芳香族性があることは以前から認められていたが,50年ごろから前述の芳香族化合物とはまったく異なる形の化合物,たとえばトロポロン,シクロペンタジエニリドC5H5⁻などにも芳香族性があることがわかってきた。これらはいずれもヒュッケル則(π電子数が4n+2個の環状共役系は芳香族性をもつという理論)に適合し,核磁気共鳴スペクトルその他の分光学的データもこれを支持した。これらの非ベンゼン系芳香族化合物の化学は60年代の有機化学の最大のテーマであった。
執筆者:竹内 敬人
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「芳香族化合物」の解説
芳香族化合物
ホウコウゾクカゴウブツ
aromatic compound
ベンゼン,ナフタレン,アントラセン,ビフェニル,インデンなどのように,芳香族性を有するベンゼン環または縮合ベンゼン環を含む炭化水素(芳香族炭化水素),およびそれらの誘導体.フラン,ピロール,チオフェンなどのヘテロ原子からなる芳香族複素環化合物も,広い意味で芳香族化合物に含めることがある.
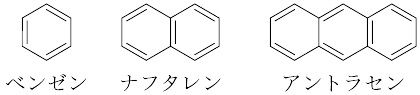
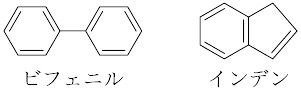
いずれもヒュッケル則に従った(4n+2)個のπ電子系を有し,安定である.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「芳香族化合物」の意味・わかりやすい解説
芳香族化合物
ほうこうぞくかごうぶつ
aromatic compound
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
百科事典マイペディア 「芳香族化合物」の意味・わかりやすい解説
芳香族化合物【ほうこうぞくかごうぶつ】
→関連項目染料|炭化水素|炭素環式化合物
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「芳香族化合物」の解説
芳香族化合物
世界大百科事典(旧版)内の芳香族化合物の言及
【化学】より
…1864年ケクレはベンゼンの環状構造を提案した。これによって芳香族化合物の化学の扉が開かれた。芳香族化合物が工業的に重要な意味をもつことは,このころからしだいにはっきりしてきた。…
※「芳香族化合物」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...