内科学 第10版 「胃粘膜下腫瘍」の解説
胃粘膜下腫瘍(胃・十二指腸疾患)
胃粘膜下腫瘍とは,胃の隆起性病変のうち主病巣が粘膜下に存在するものの総称である.したがって,胃粘膜下のさまざまの組織から発生した,良性あるいは悪性の腫瘍性病変はもちろん,非腫瘍性病変もその中に含まれる.たとえば,平滑筋腫や平滑筋肉腫のような筋原性腫瘍,消化管間質腫瘍(gastrointestinal stromal tumor:GIST),神経原性腫瘍(神経鞘腫),好酸球性肉芽腫,脂肪腫,迷入膵,炎症性類線維ポリープ(inflammatory fibroid polyp:IFP),囊腫,リンパ管腫,血管腫などが含まれる.悪性リンパ腫,カルチノイド腫瘍,転移性腫瘍も形態的には粘膜下腫瘍であるが,別に取り扱われることが多い.そのなかでもGISTはその概念や由来する細胞について最近急速に理解が深まった疾患で,頻度も多く注目されている.
分類
1)肉眼分類:
Skandakakisは胃平滑筋腫瘍(現在のGISTを含む)をその発育形式から,胃内発育型,壁内発育型,胃外発育型,混合型の4つに分類した.超音波内視鏡検査やX線CTなどの画像診断により,推定可能である.
2)病理分類(特にGISTの病理):
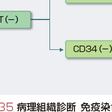
消化管に発生する粘膜下腫瘍のうち,組織学的に紡錘形細胞や類上皮細胞からなる腫瘍は,通常平滑筋腫,平滑筋肉腫や神経鞘腫と診断されてきた.その後,電子顕微鏡による微細構造の観察や,免疫組織化学的検討からこれらの腫瘍細胞の多くは平滑筋細胞や神経細胞としての特徴を,いずれも示さないことが明らかになった.つまり,c-kit蛋白やCD34の発現の有無や,筋原性マーカー(α-SMA,デスミン)あるいは神経原性マーカー(S-100蛋白)の染色性から,GISTが定義されるようになった(図8-4-35).
疫学・発生率・統計的事項
以前は良性胃粘膜下腫瘍には胃平滑筋腫が多いとされてきたが,実はそのうちかなりのものは現在GISTとして認識されているものであったと推定される.消化管のGISTの発生頻度は人口100万人あたり20人/年と推測されている.また,GISTは全消化管腫瘍の0.2~0.5%程度と考えられ,胃に限ると胃悪性腫瘍の2~3%程度,小腸では小腸腫瘍の14%程度,大腸では大腸悪性腫瘍の0.1~0.3%程度と推定されている.消化管のGISTの60~70%が胃に発生し,20~30%が小腸,5%が大腸,5%が食道に発生する.胃粘膜下腫瘍の中には神経原性腫瘍も認められるが,絶対数で一番多いのはGISTである.特に胃体上部から穹隆部にかけて発生するものはほとんどがGISTである.
臨床症状
無症状で内視鏡検査の際にたまたま発見されることが多いが,発生部位によっては狭窄症状を訴えるものもある.病巣から出血して,吐血,黒色便,貧血を契機として発見されることもある.また,巨大なものでは,腫瘍を腹部触診で触知できる場合もある.一般には腹痛,消化管出血,腫瘤触知が3大徴候とされる.
診断
胃内視鏡検査あるいは胃X線検査で,表面が胃正常粘膜で覆われた隆起性病変として観察される.隆起の辺縁はなだらかな立ち上がりを示す.また,粘膜下腫瘍に特徴的な所見として,粘膜ひだが隆起性病変の辺縁に橋をかけるようにみられる,いわゆるbridging fold(架橋ひだ)が認められる(図8-4-36).大きな粘膜下腫瘍では隆起の頂部に潰瘍を形成することもある.サイズが小さいにもかかわらず,潰瘍を形成する場合には悪性のことが多い.
鑑別診断
カルチノイド,転移性腫瘍,悪性リンパ腫,IFPなどの多くは生検で鑑別できる.その他胃静脈瘤,胃壁外からの他臓器(胆囊,肝,結腸など)や他臓器の腫瘍の圧迫が粘膜下腫瘍と間違えられることがあるが,病巣の恒常性を確認したり,超音波内視鏡検査やX線CT検査などの画像診断により鑑別できる(図8-4-37).また,可能であれば,超音波内視鏡下穿刺吸引生検法(endoscopic ultrasonography guided fine needle aspiration biopsy:EUS-FNAB)を行うのが望ましい.
経過・予後
良性の場合には臨床的には問題にならないが,悪性の場合は病巣からの大出血や破裂のほかに,肝転移や腹膜播種を起こす.転移が認められた場合,再度切除しても再発を繰り返すことが多く,予後はきわめて不良である.GISTの場合,悪性と良性は明確に分けられるものではなく,基本的には悪性のpotentialを有する.GISTの悪性の基準となる病理組織学的因子は,5 cm以上の腫瘍径,周囲組織への浸潤,血行性転移(肝臓),腹膜播種(腫瘍破裂による),強拡大の50視野あたり5個以上の腫瘍細胞分裂像である.これらの因子がひとつでも該当するものは,悪性度の高いGISTと判断される.
治療
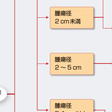
胃粘膜下腫瘍で悪性が疑われる場合は手術による切除が原則である.臨床的には5.1 cm以上のものは,悪性と考えて手術の適応とされている.この場合,開腹手術とし,可能であれば胃の部分切除(楔状切除)を行うが,その際のリンパ節廓清は原則として不要である.5 cm未満であれば,腹腔鏡下手術に熟練した外科医がいれば,腹腔鏡下手術も選択肢となる.2 cm未満の場合には,原則として6カ月から1年ごとの内視鏡あるいは,超音波やX線CTによる経過観察でよい.ただし,急激に大きくなる傾向が認められたり,悪性を示唆する所見がある場合には手術適応となる.2 cmから5 cm未満の場合には,CT,EUSおよび可能であればEUS-FNABにより精査を行ったうえで治療方針を決めることが望ましい(図8-4-38).
再発したGISTに対しては,完全切除が可能であれば再切除が行われるが,その予後はきわめて不良である.分子標的薬であるチロシンキナーゼ阻害薬のメシル酸イマチニブが臨床で使用されるようになり,その効果の高さから再発例の第一選択とされるようになった.薬剤効果判定はRECISTの基準に従い,CTなどの断層画像上で2 cm以上の標的病変を定め,その腫瘍最大径の変化を観察する.また,18FDGの取り込みを示す例では,18FDG-PETが有用と考えられるが,コストの問題もありいまのところ保険適応に至っていない.イマチニブに対して耐性になったときには,血管新生に関与するVEGF(血管内皮細胞増殖因子)受容体と,腫瘍増殖に関与するPDGF(血小板由来増殖因子)受容体など複数の受容体を標的とした分子標的薬であるスニチニブが使用される.[山口俊晴・藤崎順子・齋浦明夫]
■文献
Demetri GD, et al: Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Eng J Med, 347: 472-480, 2002.
GIST診療ガイドライン 2010年11月改訂 (第2版補訂版), 一般社団法人日本癌治療学会 / 日本胃癌学会 / GIST研究会編,金原出版,2010.
Hirota S, Isozaki K, et al: Gain-of–function mutations of c-kit in human gastrointestinal stromal tumors. Science, 279: 577-580, 1998.
出典 内科学 第10版内科学 第10版について 情報