翻訳|casein
精選版 日本国語大辞典 「カゼイン」の意味・読み・例文・類語
カゼイン
日本大百科全書(ニッポニカ) 「カゼイン」の意味・わかりやすい解説
カゼイン
かぜいん
casein
乳汁の主成分で、リンタンパク質に属し、乾酪素ともいう。牛乳のカゼインについてもっともよく研究されており、ヒトやヒツジの乳のカゼインも似た性質をもっていることが知られているが、ここではおもに牛乳のカゼインについて述べる。
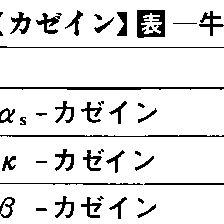
カゼインは牛乳中に約3%含まれ、牛乳に含まれる全タンパク質の約80%を占める。牛乳に酸を加えてpHを4.6にすると等電点に達し、水に不溶となって沈殿するので、容易に分離することができる。こうして得られるカゼインは、均一なタンパク質ではなく、多種類のタンパク質の混合物である。1930年代にはすでに電気泳動によって三つの成分に分けられ、α(アルファ)-カゼイン(全カゼインの70%)、β(ベータ)-カゼイン(27%)、γ(ガンマ)-カゼイン(3%)とよばれていた。その後、α-カゼインはさらにκ(カッパ)-カゼイン(αz-カゼインともいい、15%)、αs-カゼインなどいくつかの成分からなることが明らかになった。しかし、現在でもカゼインの分画法は確立されているとはいえず、さらに新しい成分が発見される可能性もある。カゼインの化学的組成の特徴は、アミノ酸以外に約1%のリンと、約1%の糖を含んでいることである。分子量は、α-カゼインが2万5000~2万7000、β-カゼインが1万7000~2万とされている。カゼインに含まれるこれらのタンパク質成分どうしは、お互いに付着しやすい性質をもつので、多数のタンパク質分子が集合した会合体となって存在する。
牛乳には、子ウシの胃液に含まれるタンパク質分解酵素レンニン(キモシン)の作用を受けると凝固するという性質がある。この牛乳凝固は、牛乳が胃の中に長時間とどまり、消化酵素の作用を十分に受けるのに都合がよいという生物的意味がある。牛乳をレンニンで凝固させたものをレンネットカゼインとよび、これに発酵その他の加工を施したものがチーズである。牛乳のレンニンの作用による凝固に際しては、κ-カゼインが重要な役割を果たしていると考えられている。レンニンは、κ-カゼインに作用して、そこから糖を含んだ分子量約8000のペプチドを遊離させる。そのことによってカゼインの各成分からなる複合体の性質が変化し、不溶性になると考えられる。なお、凝固がおこるときには、カルシウムイオンが必要である。
人乳には、カゼインは約1%含まれており、全タンパク質の約50%に相当する。牛乳に比べてラクトアルブミンの含量が多い。
カゼインは栄養剤、乳化剤、マッサージ用クリームなどに用いられる。なお、カゼインとホルムアルデヒドからつくられるカゼインプラスチックは、象牙(ぞうげ)に似た光沢をもつほか、加工や着色が容易で、象牙、サンゴ、真珠などの模造品をはじめ、ボタンや洋傘の柄(え)などの製造に用いられる。これらの利用法は、カゼインが乳汁の等電点沈殿で簡単に取り出せるという利点によっている。
[笠井献一]
牛乳はすべての必須アミノ酸(ひっすあみのさん)を含む栄養的にも完全なタンパク質であるが、育児用の調製粉乳の場合は、タンパク質、脂質、微量成分などを、すべて人乳の組成にあわせて成分調整をしている。また、レンニンで凝固したカード(レンネットカゼイン)は、加温・切断によって、収縮・粘着性を帯びる性質があり、それがチーズ製造上の利点になっているが、ピッツァやフォンデュのチーズが糸を引く現象もそれである。
[新沼杏二]
改訂新版 世界大百科事典 「カゼイン」の意味・わかりやすい解説
カゼイン
casein
乳に含まれている主要なタンパク質でリン酸を結合している。牛乳は約2.5%のカゼインを含んでいる(乳中タンパク質の約80%にあたる)。人乳には約0.9%含まれている。すべての必須アミノ酸を適当に含んでいるので栄養的に重要なタンパク質である。pH4.6付近で水に不溶になるので牛乳に酸を加えて沈殿させることにより調製する。
種類
単一のタンパク質ではなく,数種のカゼイン成分の混合物である。各カゼイン成分にはさらに遺伝的変異体が存在している。牛乳中ではカルシウムと結合したカゼインカルシウムとして存在し,さらにリン酸カルシウムと結合して複化合物(ミセル)を生成し,コロイド状態に分散している。主成分であるαS-カゼインはカルシウムにより凝固するが,κ-カゼインが存在すると安定なミセルを形成する。β-カゼインは低温ではカルシウムにより凝固しないが,室温以上では凝固する。この凝固もκ-カゼインにより防止される。κ-カゼインによって他のカゼイン成分のカルシウムによる凝固が防止され,牛乳中で安定なカゼインミセルが形成されている。凝乳酵素レンネットはカゼイン成分中のκ-カゼインに特異的に作用して,そのカゼインミセル安定化作用を失わせ,カゼイン全体を凝固させる。この変化はチーズの製造に利用されている。
製法
酸を用いて沈殿させた酸カゼインとレンネットで凝固させたレンネットカゼインがあり,性質はやや異なる。通常は酸沈殿法が用いられる。新鮮な脱脂乳を35℃に加温し,塩酸を加えてpHをカゼインの等電点(pH4.6)よりやや低い4.2まで下げる。沈殿した米粒の2倍大のカゼイン粒子を集めて水洗したのち,圧搾して脱水する。これを乾燥,粉砕して30~90メッシュの粒度にふるい分ける。比重1.25~1.31の白色,非吸湿性の製品で,水およびアルコールなどの有機溶剤には溶けない。アルカリおよび過剰の酸には可溶である。
用途
食用,飼料用として用いられるほか,工業的には接着剤,紙のコーティングなどに利用されている。
執筆者:吉野 梅夫+宝谷 紘一
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
百科事典マイペディア 「カゼイン」の意味・わかりやすい解説
カゼイン
→関連項目カード(酪農)|再生繊維|刺激療法|乳製品
出典 株式会社平凡社百科事典マイペディアについて 情報
化学辞典 第2版 「カゼイン」の解説
カゼイン
カゼイン
casein
リンタンパク質の一種.牛乳では全タンパク質の80%,人乳では30% を占め,乳タンパク質の主成分で栄養タンパク質.リン酸の大部分はセリンおよびトレオニンのヒドロキシ基とエステル結合により結合している.酸あるいは酸-アルコールによる分画沈殿によって得られる.カゼイン尿素と還元剤共存下のクロマトグラフィーにより,α S1,β,κの3種類のペプチド鎖に分かれる.カゼイン凝固作用をもつ酵素であるレンニンはカゼインからペプチドを遊離するが,それはκ-カゼインのC末端部を含むポリペプチドである.[CAS 9000-71-9]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
栄養・生化学辞典 「カゼイン」の解説
カゼイン
ブリタニカ国際大百科事典 小項目事典 「カゼイン」の意味・わかりやすい解説
カゼイン
casein
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...