関連語
共同通信ニュース用語解説 「多発性骨髄腫」の解説
多発性骨髄腫
血液細胞の一つである形質細胞ががん化して異常に増え、役に立たないタンパク質を大量に作るなどして発症するがんの一種。正常な血液細胞が減少するため、貧血によるだるさや息切れのほか、頭痛や肺炎、骨がもろくなるなどの症状が出る。白血球が減少して免疫機能が低下し、感染症にかかりやすくなったり、血小板が減って、出血の際、血が止まりにくくなったりする。中高年で発症し、男性にやや多い。治療は薬物療法を中心に放射線療法、血液細胞を作り出す造血幹細胞の移植などがある。
更新日:
出典 共同通信社 共同通信ニュース用語解説共同通信ニュース用語解説について 情報
内科学 第10版 「多発性骨髄腫」の解説
多発性骨髄腫(血漿蛋白異常をきたす疾患)
定義・概念
骨髄において形質細胞が単クローン性に悪性増殖している疾患である.M蛋白血症をきたし,高カルシウム血症,腎機能低下,骨痛,骨折,感染症などの臓器障害を起こしやすい.病因は不明である.
疫学・発症率・統計的事項
男性に多く,加齢とともに発症頻度が上昇する.
病態生理
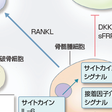
骨髄において単クローン性の形質細胞(骨髄腫細胞)が増加し,それらが産生するM蛋白が血中に増加する(図14-10-24).骨髄腫細胞は細胞接着因子を介して,骨髄ストローマおよびその細胞外マトリックスと接着することで増殖,生存,抗癌薬耐性をきたす.骨髄腫細胞と骨髄ストローマ細胞との相互作用は,両者の直接的接着およびインターロイキン-6(IL-6),インスリン様増殖因子1(IGF-1),血管内皮増殖因子(VEGF),ストローマ細胞由来因子(SDF)-1αなどのサイトカインの誘導による.骨髄腫細胞の増殖や抗癌薬耐性は,Raf,JAK,PI3-kなどの細胞内シグナルの活性化を介する.骨髄腫細胞は,破骨細胞活性化因子であるreceptor activator of nuclear factor-kappa B(RANKL)を産生し,破骨前駆細胞の破骨細胞への分化と破骨細胞の活性化を促進して,骨吸収をもたらす.骨髄腫細胞は,dickkopf1(DKK1)やsecreted Frizzled-related protein(sFRP)-2を分泌し,骨芽細胞の分化を抑制することによって骨病変の修復を遅延させ,破骨細胞の活性化とともに,骨髄腫における骨病変(溶骨性変化)を進展させる.
分類
IMWG診断基準(表14-10-23)では,骨髄腫を下記の6つの病型に分類し,骨髄腫と鑑別すべき病態としてMGUSを定義した.
1)無症候性骨髄腫:
骨髄腫ではあるが,臓器障害(高カルシウム血症,腎機能低下,貧血,骨病変,過粘稠度症候群,アミロイドーシス,年2回をこえる細菌感染)がない状態である.MGUSと同様に治療適応はないが,診断後,中央値23カ月間で症候性骨髄腫に進展するため,3カ月に1回くらいの定期検査が必要である.
2)症候性骨髄腫:
一般的に多発性骨髄腫とよばれる病型で,臓器障害が存在する.MGUS, 無症候性骨髄腫,孤立性骨形質細胞腫, 髄外性形質細胞腫から進展する骨髄腫もこの中に含まれる.治療(後述)の対象となる.
3)非分泌型骨髄腫:
骨髄腫のうちM蛋白を産生するが分泌しない症例.骨髄腫の約3%を占める.免疫固定法で血中および尿中にM蛋白を認めない.経過中にL鎖を検出しなければ,腎障害をきたさない.免疫抗体法などで検査すると,骨髄腫細胞内には免疫グロブリンを同定できる.症候性骨髄腫と同様の臨床像を呈するため,治療(後述)の対象となる.臓器障害があり,免疫グロブリン低値を示す症例では,本病型を疑って検査が必要である.予後は症候性骨髄腫と同様である.
4)孤立性骨形質細胞腫:
X線写真で骨に孤発性病変を認め,生検による病理組織学的検索で形質細胞腫と診断されるが,M蛋白,臓器障害および骨髄における形質細胞の増加を認めないもの.全形質細胞腫瘍の5%未満を占める.病変は脊椎が最も多い.治療は病変部位への放射線照射で,予後は症候性骨髄腫に比べて良好で10年生存率は40~50%である.3/4以上の症例が2~4年間の経過で症候性骨髄腫へ進展する.
5)髄外性形質細胞腫:
骨髄および骨以外の臓器に発症する形質細胞腫のことで,全形質細胞腫の約3%を占める.発生部位は,ほとんどが上気道であるが,消化管などにも発症する.確定診断は病理組織診断である.10年生存率は約70%で症候性骨髄腫と比べて良好であるが,径5 cm以上の腫瘤は症候性骨髄腫に進展しやすく予後不良である.
6)形質細胞白血病:
骨髄腫のうち末梢血中の形質細胞>2000/μLかつ末梢血白血球分画中の形質細胞比率≧20%の症例.発症時から形質細胞白血病(PCL)の病像を呈する原発性PCLと経過中に白血化した二次性PCLとに区分され,それぞれの頻度は60%と40%である.診断時にすでに骨髄外浸潤や臓器障害などが進行した状態であることが多い.治療(後述)は,標準的化学療法よりも大量化学療法が有効である.ボルテゾミブの有効性も報告されている.予後は症候性骨髄腫に比べて不良であり,生存期間中央値は7カ月程度である.
病因
病因は不明である.第二次世界大戦における被爆者に発症頻度が高い.約1/3の症例には前癌状態としてMGUSが認められる.MGUSの形質細胞における染色体不安定性が染色体の数的異常や再構成を引き起こす原因となり,新たなクローンが出現する.p16遺伝子の不活性化,N-RAS/K-RAS遺伝子の突然変異などがMGUSから骨髄腫への進展を促進することが報告されている(Hanamuraら,2006).
臨床症状
骨痛が最も頻度の高い(70%)自覚症状であり,なかでも背部痛・腰痛・肋骨部痛が多く,体動時に自覚することが多い.局所の持続する骨痛は病的骨折を反映する所見である.細菌に対して易感染性となり,肺炎や腎盂腎炎を発症しやすい.約25%の症例が腎不全を発症するが,その原因としては,増加したL鎖,高カルシウム血症,アミロイドの糸球体への沈着,高尿酸血症,繰り返す感染症,頻回のNSAIDsの使用,ヨード系造影剤の使用,ビスホスホネート製剤の投与などが知られている.進行例では,貧血による動悸や息切れも多い.過粘稠度症候群の症状(前述)は,IgM 4.0 g/dL,IgG 5.0 g/dL,IgA 7.0 g/dL以上に到達すると出現しやすい.高カルシウム血症により,うつ状態,混乱などの精神神経症状をきたすことがある.アミロイドが末梢神経に沈着すると手根管症候群やほかの末梢神経障害をきたすことがあるが,運動神経よりも感覚神経が優位に障害される.
検査成績
M蛋白の種類により,IgG型,IgA型,IgD型,IgE型,IgL型(=Bence Jones蛋白(BJP)型)に分類されるが,BJP型以外では血清総蛋白が増加し,血清蛋白電気泳動でMスパイクを認める.BJP型では低ガンマグロブリン血症を認める.尿中にもIgを認め,尿蛋白電気泳動による分画検査でIgを検出する.血清と尿の免疫電気泳動および免疫固定法でM蛋白を検出する.
末梢血液検査では,正球性正色素性貧血,赤血球の連銭形成(rouleaux formation),軽度の白血球減少,血小板減少を認めることが多い.形質細胞白血病では,末梢血中に形質細胞を多数認める.骨髄穿刺検査では,CD138+で形態学的に異型性のある形質細胞を認める(図14-10-25).CD38とCD19との発現を検索すると,単クローン性の形質細胞はCD382+CD19−であることが報告されている(Haradaら,1993).
骨粗鬆症から骨融解病変までさまざまな骨病変を認めるが,骨X線写真では,骨梁の減少,骨融解像,打ち抜き像(punched out lesion)の所見を認める.
赤沈は亢進し,CRPは軽度上昇することが多い.腎機能障害が出現しやすく,その場合は血清Ca値が上昇する.血清β2ミクログロブリン(β2M)の上昇は,骨髄腫細胞量と腎機能障害の両方の程度を反映し,骨髄腫の予後予測のための病期分類(international staging system(ISS))(表14-10-24)の指標として用いられる.
診断
高ガンマグロブリン血症があり,血清中および尿中にM蛋白が認められれば骨髄腫を疑う.骨髄穿刺あるいは髄外腫瘤の生検で,形質細胞の単クローン性増殖を認めれば,骨髄腫と診断する.骨髄腫の診断には,IMWG診断基準(表14-10-23)が最もよく用いられる.形質細胞の単クローン性増殖を証明する方法としては,①IgH鎖遺伝子の再構成パターンをサザンブロット法あるいはPCR法で解析をする方法,②フローサイトメトリーなどを用いて細胞表面抗原を解析する方法(上述のようにCD382+CD19−であれば,単クローン性増殖と判定する)の2つがある.骨髄腫と診断されると,臨床病期(ISS)(表14-10-24)を決定する.
治療・経過・予後
無症候性骨髄腫の症例は,緩慢な経過をたどるため治療の適応ではないが,症候性骨髄腫へ進展する可能性があるため,注意深い観察が必要である.
孤立性骨形質細胞腫と髄外性形質細胞腫に対しては,約40 Gyの局所放射線照射を行うと無病生存期間が延長する可能性がある.
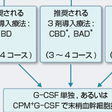
症候性骨髄腫では,骨髄腫の進行をコントロールする目的と合併症による死亡を防ぐ目的で治療を行う.新規の症候性骨髄腫症例に対する初回治療は,症例が自家造血幹細胞移植(AHSCT)を併用した大量化学療法(HDC)の適応か否かにより選択される(図14-10-26).65歳未満で重篤な合併症がなく,心肺機能が正常な症例では,AHSCT併用HDCの適応がある.なお,AHSCTの幹細胞源としては,末梢血幹細胞を用いることがほとんどである.
AHSCT併用HDCの適応がある症例に対しては,造血幹細胞に対して毒性を有するメルファランなどのアルキル化剤の投与は避けるべきである.新規薬剤であるボルテゾミブと副腎皮質ホルモンとの併用投与(BD療法)が初回治療における標準療法である.BD療法を行うと,自家末梢血幹細胞の採取には悪影響を与えず,高い奏効率(>80%)が得られる.ビンクリスチン,ドキソルビシン,デキサメタゾン併用(VAD)療法もBD療法と同様に,高い奏効率(>80%)が得られ,造血幹細胞に対する毒性が低いことから,当該症例の自家末梢血幹細胞採取前の初期治療として行われることが多い.大量デキサメタゾン(HDD)療法も造血幹細胞に対する毒性が低いことから,当該症例の自家末梢血幹細胞採取前の初期治療として用いられる.これらの初回治療を数コース施行した後に,顆粒球コロニー刺激因子(G-CSF)を単独投与あるいはシクロホスファミド投与後に投与して自家末梢血幹細胞を効率的に採取する.その後,大量メルファラン療法を併用した自家末梢血幹細胞移植を施行する.AHSCT併用HDCは,標準的化学療法と比較して完全奏効率が高く(25~40% vs <5%),無増悪生存期間と全生存期間が長いが,標準的化学療法と同様に,ほとんどの症例が治癒しない.
一方,AHSCT併用HDCの適応がない症例に対しては,メルファラン,プレドニゾロン,ボルテゾミブ併用(MPB)療法が初回治療における標準療法であり,メルファラン,プレドニゾロンの併用療法(MP療法)と比較して奏効率(75% vs 35%)と3年生存率(72% vs 59%)が高くなる.当該症例に対するほかの初回治療法としては,シクロホスファミドとプレドニゾロンの併用療法(CP療法),VAD療法,HDD療法,BD療法がある.なお,BD療法はほかの治療法と比べて腎障害を速やかに改善させる可能性が報告されている.
治療が奏効した症例では,速やかに骨痛,高カルシウム血症,貧血が改善し,感染症に罹患し難くなる.M蛋白の減少は,これらの症状の改善よりも遅れて出現する.完全奏効に至らなくても,臨床的な奏効は長期間続くことが多い. どのような地固め・維持療法が全生存期間の延長につながるかは十分に明らかにされていないため,さまざまな臨床試験が行われている.
再発・再燃した場合は,AHSCT併用HDC適応症例では,初回治療で1年間以上の奏効期間が得られた症例は2回目のAHSCT併用HDCを行い,ほかの症例ではレナリドミドやボルテゾミブなどの新規薬剤を用いて救援療法を行う.これらの新規薬剤をデキサメタゾンと併用して投与すると,再発症例の60%が部分奏効し,10~15%が完全奏効する.一方,AHSCT併用HDC非適応症例では,初期治療で6カ月間以上の奏効期間が得られた症例は効果が認められた初期治療を行い,ほかの症例ではレナリドミドやボルテゾミブなどの新規薬剤を用いて救援療法を行う. 救済療法を行った後に進行・増悪した場合は,研究的治療あるいは緩和医療を行う.
骨髄腫症例の生存期間中央値は7~8年間であるが,若年症例では10年間以上生存することがある.おもな死因は骨髄腫の進行,腎不全,敗血症,治療関連骨髄異形成症候群である.
合併症に対する支持療法も抗腫瘍療法と同様に重要である.高カルシウム血症は,ビスホスホネート,副腎皮質ステロイド,水分負荷とナトリウム利尿で治療する.急性腎不全に対しては,腹膜透析よりも血漿交換の方が効果がすぐれている.過粘稠度症候群に対しては,血漿交換を行う.肺炎球菌ワクチンの効果はない.繰り返す重症感染症に対する予防的Ig製剤の投与は有効である.下肢の神経症状,重度の局所痛,膀胱直腸障害が出現した場合は,緊急MRIを撮影し,形質細胞腫による脊髄圧迫部位に対して放射線照射を行う.痛みの強い骨病変に対して,局所放射線照射が有効である.[松永卓也]
■文献
Hanamura I, et al: Frequent gain of chromosome band 1q21 in plasma-cell dyscrasias detected by fluorescence in situ hybridization: incidence increases from MGUS to relapsed myeloma and is related to prognosis and disease progression following tandem stem-cell transplantation. Blood, 108: 1724-1732, 2006.
Harada H, et al: Phenotypic difference of normal plasma cells from mature myeloma cells. Blood, 81: 2658-2663, 1993.
Malpas JS, Bergsagel DE, et al: Myeloma, pp1-581, Oxford University Press, Oxford, 1995.
多発性骨髄腫(造血幹細胞移植の適応の考え方)
a.予後予測因子
1975年に発表されたDurie and Salmon分類が長く用いられてきたが,多数例のデータに基づく予後予測モデルでは客観的指標であるβ2MとAlbの組み合わせによって強力な予後予測分類が可能になることが示された.
b.初発症例に対する造血幹細胞移植の適応
自家移植と化学療法のRCTのメタ解析では無憎悪生存率は改善するものの,全生存率については有意な改善は認められなかった.すなわち自家移植の主要な目的は無憎悪生存率の延長によるQOLの改善ということになる.しかし,ボルテゾミブ,サリドマイド,レナリドミドの併用によって自家移植後の予後も改善している.
c.多発性骨髄腫に対する同種移植
多発性骨髄腫に対する同種移植の移植関連死亡率は30~40%と高く,自家移植の後にミニ移植を行う臨床試験が実施されている.しかし,現時点では多発性骨髄腫に対する初期治療における同種移植の位置づけは明らかになっていない.進行期における同種移植は移植関連死亡率が高いだけでなく,根治が得られる可能性もほとんどない.[神田善伸]
■文献
Koreth J, Schlenk R, et al: Allogeneic stem cell transplantation for acute myeloid leukemia in first complete remission: systematic review and meta-analysis of prospective clinical trials. JAMA, 301: 2349-2361, 2009.
Cutler CS, Lee SJ, et al: A decision analysis of allogeneic bone marrow transplantation for the myelodysplastic syndromes: delayed transplantation for low-risk myelodysplasia is associated with improved outcome. Blood, 104: 579-585, 2004.
Oliansky DM, Czuczman M, et al: The role of cytotoxic therapy with hematopoietic stem cell transplantation in the treatment of diffuse large B cell lymphoma: update of the 2001 evidence-based review. Biol Blood Marrow Transplant, 17: 20-47 e30, 2011.
出典 内科学 第10版内科学 第10版について 情報
家庭医学館 「多発性骨髄腫」の解説
たはつせいこつずいしゅ【多発性骨髄腫 Multiple Myeloma】
からだの健康を守っている免疫(めんえき)の一翼をになう抗体(こうたい)はたんぱく質でできていて、免疫グロブリンと呼ばれています。
免疫グロブリンは、骨髄(こつずい)に存在する形質細胞(けいしつさいぼう)でつくられますが、この形質細胞ががん化して骨髄腫細胞(こつずいしゅさいぼう)と呼ばれる異常な細胞となり、無制限に増殖する病気です。形質細胞のはたらきが低下する一方、正常な血液をつくる骨髄のはたらきも障害されます。
[症状]
50歳以上になってからの発症が多く、腰や背中の痛み、骨の痛みのほか、からだのだるさ、息切れ、動悸(どうき)、顔色が悪いなどの貧血(ひんけつ)の症状が現われ、出血しやすくなります。感染に対する抵抗力も低下して、肺炎などにかかりやすくなります。
骨髄腫細胞には、骨を溶かしてしまう因子が含まれているために、いろいろな骨が破壊され、わずかな外力が加わっても骨折(病的骨折(びょうてきこっせつ))をおこしやすく、骨折でこの病気が発見されることもあります。視力障害、めまい、頭痛などがおこることもあります。
頻度の低い病気のために、医師の治療を受けていてもこの病気と気づかれないことがありますから、疑わしい症状が続くときは、血液専門の医師を紹介してもらいましょう。
[検査と診断]
血液を採取して調べると、血沈(けっちん)(赤沈(せきちん))(「赤沈(赤血球沈降速度/血沈)」)が非常に亢進(こうしん)しているほかに、貧血、白血球(はっけっきゅう)や血小板(けっしょうばん)の減少がみられることがあります。
たんぱく尿が出ていることも多く、尿検査がきっかけで、この病気が発見されることもあります。
骨のX線撮影で「打ち抜き像」と呼ばれる骨の破壊像が見られることや、血清たんぱく中に、異常な免疫グロブリン(免疫グロブリン‐Mたんぱく)の増加がみられることで診断できます。
免疫グロブリン‐Mたんぱくの血中濃度が高くなると、血液の粘りけ(粘稠度(ねんちゅうど))が高まり、血液の循環障害がおこり、眼底の異常、中枢神経や末梢神経(まっしょうしんけい)の異常、心不全(しんふぜん)、腎臓(じんぞう)障害などの症状が現われます(過粘稠度症候群(かねんちゅうどしょうこうぐん))。
[治療]
化学(薬物)療法では、メルファランやシクロホスファミドなどの抗がん剤と副腎皮質(ふくじんひしつ)ホルモンのプレドニゾロンとの長期併用が効果をあげています。また、サリドマイド(保険適用外)も効果があります。
補助療法として、痛みが激しいときは、鎮痛薬(ちんつうやく)を用いますが、ときに、放射線を照射することもあります。また、腰痛にはコルセットを装着することもあります。
最近、根本的な治療法として、骨髄移植(こつずいいしょく)にかわって、造血幹細胞移植(ぞうけつかんさいぼういしょく)が期待されています。これには、造血幹細胞を自分の血液から分離し移植する自己末梢血幹細胞移植(じこまっしょうけつかんさいぼういしょく)(保険適応)や、造血幹細胞が豊富な赤ちゃんの臍帯血(さいたいけつ)を利用する臍帯血移植(さいたいけついしょく)などがあります。
治療が効果をあげているときは、ふつうに生活してもかまいません。多少、骨の痛みがあっても、適度にからだを動かすことや、水分を多くとって尿量を増やすことが、合併症を防ぐためにたいせつです。
ブリタニカ国際大百科事典 小項目事典 「多発性骨髄腫」の意味・わかりやすい解説
多発性骨髄腫
たはつせいこつずいしゅ
multiple myeloma
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
日本大百科全書(ニッポニカ) 「多発性骨髄腫」の意味・わかりやすい解説
多発性骨髄腫
たはつせいこつずいしゅ
→骨髄腫
世界大百科事典(旧版)内の多発性骨髄腫の言及
【骨髄腫】より
…免疫グロブリンを産生・分泌する形質細胞が腫瘍性に増殖する悪性腫瘍。主として骨髄で増殖し,各所の骨が侵されることが多いので,多発性骨髄腫multiple myelomaとも呼ばれ,単クローン性免疫グロブリン(Mタンパク)の出現,骨病変などを特徴とする。腫瘍化した形質細胞(骨髄腫細胞)は骨髄で主として結節状に増殖し,次第に骨皮質を融解・破壊して骨折(病適骨折)を起こす。…
※「多発性骨髄腫」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...