改訂新版 世界大百科事典 「窒素代謝」の意味・わかりやすい解説
窒素代謝 (ちっそたいしゃ)
nitrogen metabolism
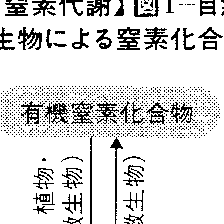
生体による窒素および窒素化合物の同化,異化,排出過程の総称。生体構成元素のうちで窒素は生体に含まれる原子の数では水素,酸素,炭素に次いで多いものである。窒素は種々の生物へ取り込まれ,それぞれ特有の生化学的過程を経て,代謝され体外へ出される。このような過程がつなぎ合わされて自然界の窒素の循環が営まれている(図1)。土壌中の窒素化合物は,雨水によって持ち込まれた硝酸塩やアンモニウム塩以外は,大部分は死んだ生物に由来する。生物遺体の有機窒素化合物は,死後の分解でアミドとアンモニアになる。土壌中の腐敗細菌Bacillus mycoidesなどの微生物は,生物遺体のアミドのほか,動物の排出した尿素,尿酸を分解してアンモニアを生じる。
こうして生じたアンモニアは,土壌中の亜硝酸菌と硝酸菌によりO2を酸化剤として,NO2⁻を経てNO3⁻へと酸化される(硝化作用nitrification,表1)。これらの細菌は,無機窒素化合物をエネルギー源とし,その酸化反応で発生するエネルギーを利用して,炭酸固定を行う(化学合成chemosynthesis)独立栄養生物である。亜硝酸細菌と硝酸細菌は硝化細菌nitrifying bacteriaと総称され,この2群の細菌は生態学的に相伴って生息している。
生体によるNO3⁻の還元は,NO3⁻を窒素源として利用,同化する同化的還元assimilatory nitrate reductionと,生体酸化還元系の最終電子受容体としてNO3⁻を利用する異化的還元dissimilatory nitrate reductionの二つに大別される(表1)。この二つの系の硝酸還元酵素どうし,亜硝酸還元酵素どうしを比べると,それぞれ相異なる酵素であり,二つの系の関係は代謝系進化の研究の興味ある課題となっている。異化的還元の一つとして,O2の代りにNO3⁻を用いて有機化合物を酸化し,そのエネルギーを利用して生育する細菌がある。この反応を硝酸呼吸nitrate respirationという。その際のNO3⁻の還元の度合は細菌の種類により異なり,NO2⁻,N2,またはNH3まで還元するものがある。N2まで還元される場合は,特に脱窒素作用または脱窒denitrificationと呼ばれる。脱窒の場合には,N2のほかにN2O,NOが副次的に形成されることがある。硫黄細菌はH2Sをエネルギー源とし,これをO2により酸化する化学合成生物であるが,その一部のものは嫌気条件下ではO2の代りにNO3⁻やNO2⁻を利用してH2Sを酸化しN2を発生する。これがもう一つの型の脱窒である。これとは逆に微生物のなかには窒素ガスを固定する(窒素固定nitrogen fixation)ものがある。
植物は尿素などの有機窒素化合物を利用することもできるが,一般には硝酸塩やアンモニウム塩などの無機窒素化合物を根から吸収する。多くの植物は硝酸塩のほうをよりよく吸収,利用するが,植物の種類によってはアンモニウム塩のほうをよく利用するものもあり,また若いときはアンモニウム塩をよく利用し,生長が進むと硝酸塩を利用するようになる植物もある。外界から取り入れた窒素化合物を生体の構成物質に変える過程を窒素同化という。植物に吸収されたNO3⁻はまず硝酸レダクターゼの触媒する次の反応によりNO2⁻へ還元される。
NO3⁻+NAD(P)H+H⁺─→NO2⁻+NAD(P)⁺+H2O
同化型の硝酸レダクターゼはSH基,フラビンアデニンジヌクレオチド,ヘム,モリブデンMoを含む複合酵素であり,大部分は葉に存在する。この酵素はNO3⁻,サイトカイニンによる誘導,アンモニアによる生成抑制のほか,種々の生体内物質による活性化,不活性化による調節,フィトクロムによる調節をも受ける。光合成細菌,ラン藻の一部にはフェレドキシンを電子供与体とする同化型の硝酸レダクターゼが知られている。還元の第2の段階で,NO2⁻は亜硝酸レダクターゼの働きで,6電子還元を受けアンモニアとなる。
NO2⁻+6e⁻+6H⁺─→NH3+H2O+OH⁻
同化型の亜硝酸レダクターゼは非ヘム鉄とシロヘムsirohemeを含む酵素であり,緑色細胞では葉緑体に,非緑色細胞では原色素体に局在する。電子供与体は葉緑体の場合はフェレドキシンと考えられているが,非緑色細胞の場合はよくわかっていない。
このようにして生じたアンモニアは,グルタミンまたはカルバモイルリン酸への合成を経て,種々の有機化合物へ取り込まれる(図2)。無機態窒素が同化されてグルタミンやアスパラギンになることは1910年ころから知られていたが,アンモニアが最初に有機化合物になる反応は,グルタミン酸デヒドロゲナーゼ(GDHと略記)による反応と考えられていた。しかし,現在では酵母菌類を除いては,グルタミンシンテターゼ(GSと略記)とグルタミン酸シンターゼ(L-glutamine-2-oxoglutarate aminotransferase。GOGATと略記)の共同の働きでグルタミン酸が合成されると考えられている(図3)。
反応は,
または
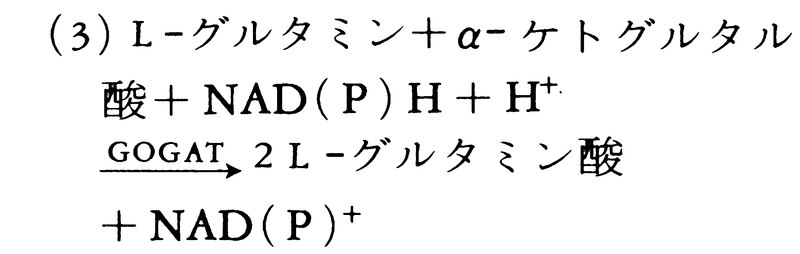
緑色細胞では,GS,GOGATともに葉緑体に局在し,GOGAT反応の電子供与体は還元型フェレドキシンである(反応(2))。非緑色細胞ではNAD(P)Hを補酵素とするGOGATが存在する(反応(3))。GS/GOGAT系は光呼吸においてグリシンから放出されるアンモニアの再同化にも働いている。GDHは多くの場合,グルタミン酸の分解に働いているが,酵母菌類ではGS/GOGAT系はほとんど存在せず,アンモニアの同化はNADPH依存のGDHによって行われる。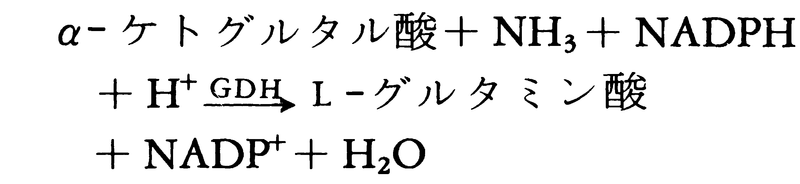
アンモニア同化のもう一つの経路はカルバモイルホスフェートシンターゼによりカルバモイルリン酸を生じるものである。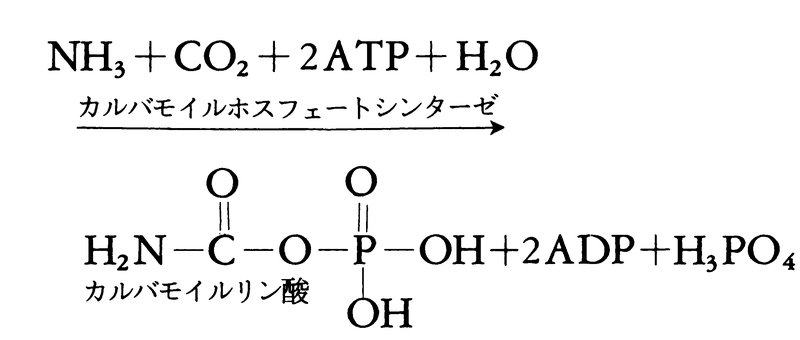
アミノ酸代謝
アミノ酸は生体内でおもに次の3通りの代謝的変化を受ける。
(1)アミノ転移 グルタミン酸型トランスアミナーゼ,アラニン型トランスアミナーゼなどによって,種々のケト酸との間にアミノ基の授受が行われ,それに対応する種々のアミノ酸が合成される。反応は,
このあとさらに炭素骨格の変更,修飾が行われて多くの種類のアミノ酸が合成されていく(図2,表2)。タンパク質の成分にはならない非タンパク性アミノ酸も合成される。これらはタンパク質構成アミノ酸とともにタンパク質以外の窒素化合物の合成の重要な基質となる。グルタミンのほかにもう一つの代表的なアミドであるアスパラギンはアスパラギンシンテターゼ(ASと略記)によってグルタミンから合成される。
細菌の場合は,
アミノ酸合成系では多くの場合,最終産物とみなされるアミノ酸によって,合成経路の最初の反応に対するフィードバック制御が行われ,遊離のアミノ酸が高濃度に蓄積しないしくみになっている。
(2)脱アミノ (a)グルタミン酸はGDHにより酸化的に脱アミノされる。反応は,
(4)の左行反応と(6)の右行反応との組合せで種々のアミノ酸の脱アミノが行われる。種々のアミノ酸からα-ケトグルタル酸へのアミノ転移は細胞質で行われ,生じたグルタミン酸はミトコンドリア内膜を通過して内部へ入り,ここでGDHで脱アミノされるかアスパルテートトランスアミナーゼの働きでオキサロ酢酸にアミノ基を渡し,自身はα-ケトグルタル酸となってクエン酸回路で代謝される。(b)酸化的脱アミノ反応はアミノ酸オキシダーゼという一群のフラビン酵素によっても行われるが反応は異なる。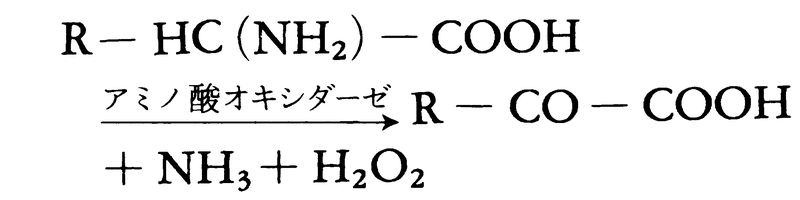
(c)酸化的脱アミノに対し,一群のアンモニアリアーゼによる非酸化的脱アミノ反応がある。フェニルアラニンアンモニアリアーゼはフェニルアラニンからアミノ基を離すことにより,リグニン合成の重要な前駆体であるトランス-ケイ皮酸を供給する。(d)グルタミンやアスパラギンの酸アミド基はそれぞれグルタミナーゼ,アスパラギナーゼ(アミダーゼと総称される)の働きで加水分解により脱アミノされる。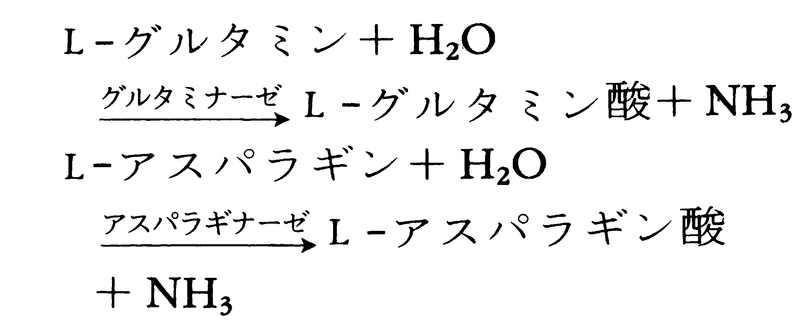
逆にこれらのアミドの合成はそれぞれGS,ASにより行われ,植物では他の窒素化合物の脱アミノで生じたNH3をグルタミン,アスパラギンという無害な形で蓄積する。動物では脱アミノで生じたNH3は尿素回路で処理される。
(3)脱炭酸 いくつかのアミノ酸はそれぞれのデカルボキシラーゼにより脱炭酸されてアミンを生成する。例えば,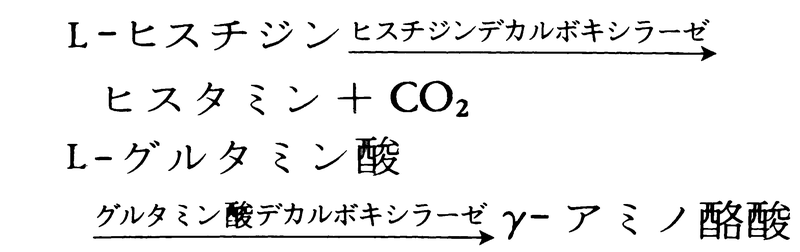
生成された各種アミノ酸はペプチド・タンパク質の合成に用いられるほか,ヌクレオチド,核酸,ポルフィリン,アルカロイド,アミノ糖など多くの有機窒素化合物の合成に用いられる(表3)。カルバモイルリン酸は尿素回路へ入り,アルギニン,オルニチン,尿素を生成するほか,ピリミジン合成の基質として用いられる。タンパク質は,動物でも植物でも,タンパク質分解酵素(プロテアーゼと総称される)によってアミノ酸にまで分解される。糖質,脂質などのエネルギー源が欠乏すると,タンパク質が分解されアミノ酸がエネルギー源として利用される。タンパク質の代謝回転速度はタンパク質の種類によって著しく異なる(表4)。
核酸を構成する各ヌクレオチドはそれぞれ複雑な経路を経て合成される。核酸の分解は,ヌクレオチド,ヌクレオシド,塩基へと順に加水分解され,さらに塩基が分解を受ける。多くの動物ではプリン誘導体の代謝最終産物は尿酸である。一方,核酸の分解により生じた塩基を,元の合成経路とは別の経路でヌクレオチドへと合成し,核酸合成に役だてるサルベージ経路が存在する。
→アミノ酸 →空中窒素固定
執筆者:辻 英夫
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「窒素代謝」の意味・わかりやすい解説
窒素代謝
ちっそたいしゃ
窒素、および窒素を含む化合物が、生体内で変換される過程を総称して窒素代謝という。生物が外界から摂取する窒素の形態は生物によって異なり、大気中の分子状窒素を固定して有機窒素化合物を合成する窒素固定生物、硝酸などの無機窒素化合物を同化する植物および細菌類、有機態の窒素化合物しか利用できない動物および一部の微生物などに分けられる。大気中の分子状窒素を利用できる生物は、地中にすむアゾトバクターやクロストリジウムなどの細菌類、マメ科植物などの根に共生して根粒を形成する根粒菌、および一部の放線菌、藍藻(らんそう)などに限られている。これらの窒素固定生物は、遊離窒素を直接活性化するニトロゲナーゼのほか、還元のための酵素系をもっている。この窒素固定反応にはモリブデンと鉄が不可欠であり、アンモニアが生成物であるが、この反応において安定な中間物質はまだみいだされていない。
植物などのように無機態の窒素化合物を利用する生物は、一般に土壌から硝酸態の窒素を摂取する。これは、土壌中のアンモニアが硝化細菌によって、ただちに硝酸まで酸化されるためである。植物の根から吸収された硝酸塩は、硝酸還元系の酵素によってアンモニアに還元される。アンモニアはグルタミン合成酵素によってグルタミンとなり、ついでグルタミン酸合成酵素によってグルタミン酸となる。このアミノ酸から他のアミノ酸が合成され、さらにタンパク質に合成される。細菌や藻類では、このほかにグルタミン酸デヒドロゲナーゼによってアンモニアからグルタミン酸が生成し、これからアミノ酸、タンパク質が合成される。動物などのように有機態の窒素化合物しか利用できない生物は、食物として吸収したアミノ酸などを素材として生物自体に固有のタンパク質を合成する。このように外界の窒素化合物を生体の構成物質に変える過程を窒素同化という。
一方、生体内の窒素化合物は絶えず代謝され、変換されている。タンパク質はアミノ酸に加水分解され、さらに酸化などの反応によって脱アミノされて分解していく。脱アミノ反応で生成したアンモニアは、植物ではグルタミンやアスパラギンのアミドとなって蓄積されることが多いが、動物ではアンモニアのまま、あるいは尿素や尿酸に変えられてから体外に排出される。細菌のなかには、嫌気的な条件で硝酸を呼吸の電子受容体として硝酸呼吸を行うものや、窒素ガスとして放出する脱窒素作用を行うものもある。また、土壌中に存在する硝化細菌は、好気的条件でアンモニアを硝酸まで酸化して、その際に放出されるエネルギーを用いて炭酸同化を行っている。
[吉田精一]
最新 地学事典 「窒素代謝」の解説
ちっそたいしゃ
窒素代謝
nitrogen metabolism
生物による窒素化合物の同化・異化・排出の総称。生物は硝酸塩・N2をアンモニアに変え,これから主にグルタミン酸を経て,有機窒素化合物を形成,生体の重要成分であるタンパク質・核酸などを合成する。排泄はアンモニア(微生物・下等動物)・尿素(哺乳類など)・尿酸(鳥類・爬虫類)の形で行われる。窒素の地球生化学的循環をつくりだすとともに栄養的に重要。
執筆者:石本 真
出典 平凡社「最新 地学事典」最新 地学事典について 情報
化学辞典 第2版 「窒素代謝」の解説
窒素代謝
チッソタイシャ
nitrogen metabolism
生体における窒素含有物質が関与する代謝反応.[別用語参照]窒素固定
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...