関連語
精選版 日本国語大辞典 「総論」の意味・読み・例文・類語
そう‐ろん【総論】
- 〘 名詞 〙 全体の大要をまとめて論ずること。また、書物の巻頭で、概要を述べた論やその文章。⇔各論。
- [初出の実例]「首四句先
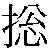 論也」(出典:杜詩続翠抄(1439頃)二)
論也」(出典:杜詩続翠抄(1439頃)二) - [その他の文献]〔宋史‐蘇軾〕
- [初出の実例]「首四句先
内科学 第10版 「総論」の解説
総論(呼吸器系の疾患)
(1)視診
a.呼吸数と呼吸の深さ
呼吸数の評価は胸郭の運動を観察して行う.患者が意識的に頻呼吸や息こらえなどを行うおそれがある場合,胸部や腹部の聴診などの際に,胸郭の運動を観察し呼吸数をカウントする.呼吸が浅くて胸郭の動きが評価しにくい場合には,紙片を鼻孔に当てるかまたは呼吸音を聴診するなどによって測定できる.呼吸数の異常病態について表7-1-1に示す.
呼吸器疾患による低酸素血症(室内気吸入で動脈血PaO2<60 mmHg)を呼吸不全とよぶが,発症経過より急性呼吸不全(acute respiratory failure)と慢性呼吸不全(chronic respiratory failure)に分類される.一般に,呼吸不全では頻呼吸を伴うことが多いが,頻呼吸を伴う呼吸不全は急性であり,頻呼吸を伴わない呼吸不全は慢性を考える.慢性呼吸不全の患者が新たに頻呼吸をきたしたときは,慢性呼吸不全の急性増悪(acute on chronic respiratory failure)を考える.
一方,多くの急性呼吸器疾患では,低酸素血症がなくても,頻呼吸を呈することがある.初期の肺炎などでは肺の聴診でクラックル音(crackles)をいまだ認めないことがあり,浅く速い呼吸が唯一の異常所見であることがある.Kussmaul呼吸は,尿毒症や敗血症などによる代謝性アシドーシスを代償するための規則的な深い呼吸が持続する状態である.
呼吸数の評価を行うときに,あわせて呼吸の深さも評価する.「浅い」呼吸か「深い」呼吸かの評価を行う.1回換気量と呼吸数のいずれかまたは両方が低下した状態を,肺胞低換気(alveolar hypoventilation)とよぶ.一方,急性の浅く速い呼吸は急性肺炎に特徴的な所見である.浅い呼吸はまた,胸膜痛,肋骨痛,術後痛などでも認められる.
b.呼吸のパターン
呼吸のリズムと規則性のことを呼吸のパターンとよぶ.一般に,安静時においては,吸気:呼気時間は1:2である.呼気終了後に休息期があり,それから再び吸気に移る.異常な呼吸のパターンの代表的なものに,Cheyne-Stokes呼吸と失調性呼吸がある.Cheyne-Stokes呼吸とは,無呼吸と過換気のサイクルを周期的に繰り返す呼吸のリズム異常である(図7-1-1).無呼吸状態は,数秒から十数秒間におよぶ.Cheyne-Stokes呼吸を呈することがある疾患を表7-1-2に示す.
失調性呼吸(Biot呼吸)とは,頻呼吸と無呼吸が非周期的に無規則にみられる呼吸のリズム異常のことをいう.脳炎,脳圧亢進などで認められることがある.
呼吸の観察では,呼吸数や深さ,パターンに加えて,患者が努力呼吸を行っているかにも注意する.努力呼吸は呼吸不全や喘息重積発作,COPD急性増悪などの重篤な病態をきたしていることを示唆する.表7-1-3にあげるような項目を認めた場合には,努力呼吸があるものとして迅速な対応をすべきである.鼻翼呼吸と奇異性呼吸は特に重要である(図7-1-2).
c.胸郭の形状
胸郭の形状を観察するときにはできるだけ患者の体勢を直線状にして行う.脊柱の後弯や側弯に注意する.漏斗胸や鳩胸では呼吸不全をきたすことはまれであるが,重度な後弯や側弯では呼吸不全をきたしうる.胸郭の前後径の増大を樽状胸郭(barrel chest)とよぶ.慢性閉塞性肺疾患や胸椎多発性圧迫骨折でみられる.胸郭の形状に加え,胸郭の動きを左右比較しながら観察する.呼吸器疾患で,病変部位が片側のみであれば,胸郭の動きに左右差が認められる.
(2)触診と打診
a.気管の触診
気管の偏位(tracheal deviation)をみるには,まず検者の第2指の指先を患者の胸骨上縁において正中線の目安とし,次にその指先を上方に直線上に進める.気管が正中に触れれば偏位はない.気管牽引(tracheal tug)をみるには,患者の甲状軟骨を検者の第1と第2指の指先でつまんで軽く頭側へ引っ張ってみる.心拍動と一致して気管牽引を感じたら弓部大動脈瘤を示唆する(Oliver徴候).
b.触覚振盪音
触覚振盪音(tactile vocal fremitus)とは,胸壁を通して触診でとらえられる母声音振動のことである.患者に「ひと~~つ」など母音を発声させ,手掌面や手掌尺側部を左右対称部位に当ててその左右差を確認する(図7-1-3).胸水や気胸は触覚振盪音を減弱させる.
c.打診
肺尖部の打診では直接鎖骨を打診するとよい.胸部の打診では,左右対称部位を打診し,その左右差を確認する.検者の左手第3指を胸壁に密着させ,右手第3指で,左手第3指の遠位指節間関節を,明瞭な音が出る程度で最も軽く打つ. 正常の肺は打診上,共鳴音(resonance)である.胸水貯留があれば濁音(dullness)であり,気胸では鼓音(tympany)となる.
(3)聴診
a.呼吸時の雑音
聴診器なしで聞かれる呼吸時の雑音は気道狭窄を示唆する.一般に,雑音の大きさと閉塞の程度は比例するが,ほとんど完全閉塞の状態になると雑音が聞かれなくなる.呼吸時の雑音が聞かれていた努力呼吸状態の患者で,呼吸時の雑音が聞かれなくなったら気道閉塞を疑って適切で迅速な処置を行う.
b.呼吸音
胸壁で通常聞かれる,肺胞呼吸音(alveolar breath sound)は吸気が大きく聞かれる呼吸音である.一方,気管付近の呼吸音,すなわち気管呼吸音(tracheal breath sound)は呼気が大きく聞かれる呼吸音である.気管支拡張症などがある部位では,気管呼吸音がその部分で聞かれる(tubular breath sound).
c.肺性副雑音
健常者では聴かれない音を副雑音(adventitious sound)という.さらに,副雑音は肺性と胸膜摩擦音など非肺性に分かれる.肺性副雑音は,連続性(continuous)と非連続性(discontinuous)とに分けられる.
連続性副雑音(乾性ラ音)は音の高低と音色により,wheezes(楽音様高音)/rhonchi(いびき様低音)と分類される.wheezesは気道の狭窄(閉塞)病変(喘息やCOPDなど)で聞かれる.喘息で聞かれるwheezesではJohnsonの分類による重症度評価を行う(表7-1-4).
stridorは「吸気>呼気」の大きさで,上気道付近に聞かれる,大きな高音性の楽音様副雑音である.stridorは上気道付近の気道狭窄(閉塞)病変を示唆する危険な徴候である.
rhonchiは気道の分泌物(痰)が貯留する病変(気管支炎など)で聞かれる.rhonchiが触診で触れる場合には,rattlingとよばれ,過剰分泌を示唆しており,分泌物(痰)吸引が必要となる.
非連続性副雑音(湿性ラ音)は,cracklesとよばれる.cracklesが聞かれるときには,音質によるfine(質の細かい)/coarse(質の粗い)の分類を行うが,cracklesが聞かれる吸気の時相(phase)によって分類すると(early/late/holo)病態を推定するのに役に立つ(表7-1-5).
d.非肺性副雑音
胸膜炎の患者では,胸膜摩擦音(pleural friction rub)とよばれる,呼吸時に臓側と壁側胸膜による摩擦音が聞かれることがある.下部胸壁で聞かれることが多く,患者が胸膜痛を訴える部位で最もよく聞かれる.
胸水が大量に貯留している場合,患者の体を揺らしたときに(患者に事前の十分な説明が必要である),液体が跳ねるような振水音(succussion splash)が聞かれることがある.縦隔気腫では,胸骨左縁で心臓の拍動に一致して破裂音が聴取されることがあり,これをHamman破裂音(Hamman’s crunch)とよぶ.
(4)全身の診察
呼吸器疾患ではさまざまな全身所見を呈することがあり,肺以外の診察も必須である.頭頸部ではまず,副鼻腔炎の存在(副鼻腔気管支症候群など),顔面紅潮(慢性低酸素血症による二次性多血症),顔面腫脹+側副血行静脈の発達(上大静脈症候群)に注意する.口唇,舌などのチアノーゼ(中心性チアノーゼ)は,低酸素血症で還元型ヘモグロビンが5 g/dL以上の場合にみられる.ヘモグロビンが増加している多血症では,チアノーゼが出現しやすい.
四肢では,ばち指(clubbed fingers:clubbing)に注目する.ばち指はさまざまな疾患で認められるが,呼吸器疾患によるばち指では,四肢のすべてで出現することが特徴である.爪の基部と爪の付け根の皮膚とのなす角が180度をこえた場合にばち指とよぶ(図7-1-4).
ばち指を呈する呼吸器疾患には,肺癌,間質性肺疾患,肺膿瘍,気管支拡張症などがある.骨肥大と関節症を伴うときは,肥大性肺性骨関節症(hypertrophic pulmonary osteoarthropathy)とよばれる.一般に,結核やCOPDではばち指を呈することは少ない.肺結核後遺症やCOPDでばち指を認めた場合には,肺癌や気管支拡張症などの合併を疑う.
アステリキシス(asterixis:flapping)は,両手首にみられる,非律動非同期的な羽ばたき運動であり,さまざまな疾患(尿毒症や肝性脳症)で認められるが,急性高二酸化炭素血症(PaCO2がベースライン値から15 mmHg以上上昇した場合)にも認められる.手のぬくもり(hot hands)と合わせて,CO2ナルコーシスの早期発見に有用な所見である.CO2ナルコーシスが進行すると,眼底でうっ血乳頭が認められる.
また,肺の悪性腫瘍では,神経学的診察が重要であり,重要な神経症候について表7-1-6に示す.
(5)慢性閉塞性肺疾患の診察所見
COPD患者ではさまざまな特徴的な臨床所見を認める.喫煙者(過去の喫煙者を含む)を診察する場合,COPDの所見(表7-1-7)がないかどうか注意を払う.特に,慢性の労作時呼吸困難や湿性咳を訴える患者の診察では必須である(Tokudaら,2007;徳田ら,2011).
2)呼吸器疾患のバイオマーカー
呼吸器の特徴は外界の異物が常時侵入してくるため,それに対応するための強力な免疫能と気道クリーニング能を有していることである.
このような特徴から,感染症やアレルギー性の疾患が多い.日常の臨床で多く遭遇する疾患をおおまかに,①呼吸器感染症(肺炎,気道感染症,肺結核),②喘息,③慢性閉塞性肺疾患(chronic obstructive pulmonary disease:COPD,肺気腫や慢性気管支炎),④肺癌や中皮腫などの悪性腫瘍,⑤びまん性肺疾患(間質性肺炎やびまん性汎細気管支炎など多数の疾患の総称)の5種類に分類すると便利である.
これらの疾患では外来異物に由来する物質や生体反応物質を血液や喀痰中から検出することが可能であり,バイオマーカーと呼称し,診療の参考所見として使用している.
(1)呼吸器感染症のバイオマーカー
a.末梢血白血球
細菌感染症により通常末梢血白血球数と好中球数は増加する.好中球分画の左方移動はさらに鋭敏である.ウイルス感染では,通常末梢血白血球数の減少を認める.
b.血清CRP(C-reactive protein)
CRPは肺炎球菌のC多糖体と反応し結合する蛋白質で急性相反応蛋白の一種である.きわめて感度が高いため,わが国で最も繁用されている臨床検査の1つである.感染症に限らず,炎症性疾患において血中濃度が増加し,軽快すると速やかに検出されなくなる.血中IL-6高値が持続すると肝臓において産生される.
c.赤血球沈降速度(赤沈,erythrocyte sedimentation rate:ESR)
赤沈はCRP同様,感染症など全身の炎症性疾患において亢進する.貧血,血漿アルブミン濃度低下,血漿フィブリノゲンやほかのグロブリン濃度増加があると赤沈は亢進する.播種性血管内凝固症候群(disseminated intravascular coagulation:DIC)ではフィブリノゲン濃度の急激な減少が起こり,亢進していた赤沈速度が正常化し,DIC診断の契機となる.
d.血清プロカルシトニン
血中のプロカルシトニン(procalcitonin)値は細菌感染症によって増加しやすい.その重症化予測やウイルス感染症との鑑別診断に期待されている.
e.血清中抗体価
種々のウイルス性肺炎,マイコプラズマ肺炎,クラミジア肺炎,慢性真菌症(特にアスペルギルスによる菌球症など)では血清中の抗体価やその変動の診断的価値が高い.
f.抗原・菌体成分の検出
インフルエンザウイルスのA型,B型を診断する迅速診断キットがある.検体は咽頭拭い液や鼻汁である.わずか15分前後で診断可能である.発症後7時間以上経っている症例での感度は90%前後である.
真菌のうちクリプトコックス感染症は血液中からクリプトコックス抗原を検出することによってなされることが多い.
肺炎球菌およびレジオネラ肺炎の診断には尿中抗原の検出が有用である.
日和見感染であるサイトメガロウイルス感染症の診断には,末梢血多核白血球に感染したウイルス抗原を免疫化学的に染色し陽性細胞数を数える抗原血症(antigenemia)法がある.
真菌であるPneumocystis jiroveci(以前の名前はP. carinii)感染によるニューモシスチス肺炎やほかの真菌による深在感染症の診断には血清中のβ-d-グルカンの定量が有力である.一方,真菌のうちクリプトコックス感染症の診断にはβ-d-グルカンの定量は有用でないことも知っておく必要がある.
g.インターフェロン-γ遊離試験
結核菌感染者のリンパ球は結核菌体成分に触れるとインターフェロン-γを放出することを利用して結核感染の有無を評価する.
h. DNA診断・PCR診断
肺結核や非結核性抗酸菌症に対して迅速診断や高感度診断の目的でDNA診断やPCR診断が用いられている.ニューモシスチス肺炎の診断にも喀痰や気管支肺胞洗浄液を材料としたPCR診断が有用である.
i.アデノシンデアミナーゼ(adenosine deaminase: ADA)
胸水の原因が不明の場合,胸水中のADA値が高ければ結核性あるいはリンパ腫性胸水を示唆している.
(2)サルコイドーシスのバイオマーカー
サルコイドーシスは肺,眼,心,神経,皮膚,関節などに乾酪性壊死を伴わない慢性肉芽腫を形成する原因不明の疾患であり,血清中のACE(angiotensin converting enzyme,アンジオテンシン変換酵素)が増加することが多い.
(3)間質性肺炎のバイオマーカー
間質性肺炎は肺胞隔壁に主病変が存在する150種以上の疾患の総称である.間質性肺炎のなかで原因不明のものを特発性間質性肺炎(IIP)とよぶ.さらにIIPはIPF(特発性肺線維症),NSIP(非特異型間質性肺炎),COP(特発性器質化肺炎),AIP(急性間質性肺炎),RB-ILD(呼吸細気管支炎関連間質性肺疾患),DIP(剥離性間質性肺炎),LIP(リンパ球性間質性肺炎)に分類される.IIPの診断と活動性の評価には血清マーカーであるKL-6,サーファクタント蛋白(SP)-A,SP-Dが有用である.
1)KL-6:
KL-6(Kohnoら,1989)は,膜貫通型の非分泌型ムチンであるMUC1ムチンに属する200 kDa以上の巨大な分子量をもつ糖蛋白の一種である.線維化が進行している間質性肺炎では血中に増加する.
IPFでは診断補助検査や予後予測因子として有用である.膠原病関連間質性肺炎において,K-6はIPF同様に高い陽性率を示すことが報告されている.COPではKL-6は上昇しないという報告がある一方,約半数の症例で陽性となるという報告もある.放射線肺炎の診断やステロイド治療に対する治療効果判定にも使用されている.
薬剤性肺炎は多くの薬剤により生じることが知られているが,これらの薬剤性肺炎においてもKL-6が上昇することが報告されている.血清KL-6値は予後が悪いタイプの薬剤性肺炎において上昇することが多い.
2)SP-D・SP-A:
SP-D(surfactant protein-D),SP-A(surfactant protein-A)が血液中で上昇する機序はKL-6と同様に肺胞上皮傷害に伴う肺胞-血管透過性の亢進が関与している.SP-D,SP-AはKL-6と同様に予後予測因子としても有用であり,初診時から3年以内に死亡したIPF患者では,生存例と比較してSP-A,SP-D値が有意に高かったことが報告されている.
(4)肺癌のバイオマーカー
肺癌を診断するためには,肺癌細胞や肺癌組織を証明することが必要である.しかし,血清腫瘍マーカーは採血を行うのみで結果を得ることができ,さらにその結果が数値という客観的データで表される利点がある.肺癌は複数の組織型が混在することがあり,しばしば複数の腫瘍マーカーの測定が有用である(大下ら,2005).
1)癌胎児性抗原(carcinoembryonic antigen:CEA):
血清CEA値は癌細胞組織の総体積と関連が高いと考えられている.肺癌全体での陽性率は約50%であり,腺癌では約60%と有用性が高い.特に腫瘍径(T因子),リンパ節転移(N因子)と相関し,病期の進行に伴い陽性率が高くなる.
2)サイトケラチン19フラグメント(cytokeratin 19 fragment:CYFRA21-1):
CYFRA21-1の肺癌全体での陽性率は50~60%で,なかでも非小細胞肺癌(non-small cell lung cancer:NSCLC)における陽性率が高いが,特に扁平上皮癌では60~80%の陽性率を示す.
3)扁平上皮癌関連抗原(squamous cell carcinomarelated antigen:SCC抗原):
子宮頸癌関連抗原TA-4(tumor antigen-4)の亜分画の1つで,わが国で開発されたものである.肺扁平上皮癌における陽性率が高く,特異度も高い.
4)ガストリン放出ペプチド前駆体(pro-gastrin releasing peptide:ProGRP):
小細胞肺癌(small cell lung cancer:SCLC)の増殖因子であるガストリン放出ペプチドの前駆体であり,わが国で開発されたものである.SCLCに対する特異度がきわめて高い.腎不全の約50%の症例で血清ProGRP値は高値を示すので注意が必要である.
5)神経特異的エノラーゼ(neuron specific enolase):
SCLCに対する特異度が高く,臨床病期の進行とともに陽性率・陽性値は高くなる.NSEは神経細胞や赤血球膜にも存在するため,脳転移,脳血管障害や検体の溶血でも高値を呈することがあるため注意が必要である.
(5)中皮腫のバイオマーカー
中皮腫細胞が発現するメゾテリン(mesothelin)関連蛋白は中皮腫患者血清中に検出可能であり,感度83%,特異度95%と良好であり,今後の臨床応用が期待されている(Robinson ら,2005).
(6)呼気中一酸化窒素(NO)
気管支喘息では,呼気中NO値が気道炎症の程度,すなわち,コントロール状態を反映することがわかっている.
3)画像診断
(1)胸部単純X線撮影
単純撮影のハードウエアとソフトウエアの進歩
胸部単純撮影は,人体(被写体)にX線を照射し後方においたフィルムやX線検出器で透過してくるX線を検出し,どの程度人体組織によりX線が吸収されたかを画像化する手法である.かつては,X線を受像するためにX線を受けて発光する増感紙とX線写真用のフィルムを使用するフィルムスクリーン法が用いられていたが,最近では輝尽性蛍光体を使用したイメージングプレートやフラットパネルを利用し受光したX線を直接電気信号に変換しコンピュータを用いて画像化するデジタルX線撮影法(computed radiography:CR)が普及し,ほとんどの大規模な施設ではCRが採用されている.
CRは,はじめからデジタル化された情報であり,画像の観察はモニタを用いフィルムに出力する必要はない.また種々の画像処理により画像をより見やすくしたり,画像間で演算(時期の違う2枚のX線画像を差し引きし,新たに出現した陰影を見やすく表示する)なども容易に行いうる.画像の保管もハードディスクを用いて電子的に行うので,画像の散逸もなく保管に要する費用は少ない.デジタル画像の広範な進歩と普及により,画像処理のソフトウエアやコンピュータを利用した診断支援(異常陰影の自動検出,自動診断など)システムの開発なども急速に進歩しつつある.
a.胸部画像診断における単純撮影の役割,長所,短所
単純撮影の利点は,CTに比較すると,手軽に撮影できることや安価であること,被曝が少ないことなどがある.重積像であることから,病変の全体像や上下方向の進展の特徴,肺容積の変化などが直感的に把握しやすく,何回もの写真を比較して経過を比較観察しやすい.逆に,欠点としては,濃度分解能がCTに比べて悪く,重積像であることから,淡い陰影や小さな病変の検出が不良であることや所見の有無に関しても信頼度が低く,その評価には,経験を要する点などがあげられる.
胸部単純撮影は,胸部画像診断の中で第一に試みられる検査法であり,スクリーニングや経過観察の手法としてきわめて有用である.
b.種々の胸部単純撮影法
ルーチンに用いられる胸部単純撮影は胸部正面像が中心である.正面像は,通常立位,深吸気位で撮影される.スクリーニングの目的のみでは原則として胸部側面像は必要としない.しかし,疾患の種類や胸部正面像の所見次第では,側面像を必要とする.スクリーニングの撮影では,110~120 kVpの準高圧あるいは高圧撮影を行う.高圧撮影では画像のコントラストはやや低下するが,骨の陰影が不明瞭になり肺野の病変は見やすくなるとともに白すぎて評価しにくい肺野(低濃度部)の面積が減少する.また皮膚線量を減らすことができる.またその他の胸部で利用される撮影法としては,斜位撮影や肺尖撮影,側臥位正面撮影,肋骨撮影などがある.
1)正面,側面像(図7-1-7, 図7-1-8):
ルーチンでは,深吸気位,立位で撮影される.胸部単純撮影の基本となる撮影法である.cross table lateral projection
は,臥位での側面撮影で,臥位での気胸の診断などに利用される.
2)肺尖撮影(図7-1-9):
肺尖部は,鎖骨や上位肋骨などの骨陰影に障害されて肺野の陰影が見えにくいため下方からあおって撮影し,鎖骨と肺野の異常陰影の重なりを取る方法である.肺尖部の異常陰影が疑われるときに利用される.
3)側臥位撮影(図7-1-10):
側臥位で正面撮影をする方法で,少量の胸水を検出するのにすぐれる.胸水を疑う側を下にした側臥位で正面を撮影する.気胸の診断では気胸を疑う側を上にした撮影を行うこともある.
4)臥位正面像:
立位をとれない患者では,ポータブル撮影装置により,臥位撮影が行われる.立位と異なり,心陰影はやや大きめに投影されCTRは55%まで正常である.上肺の血管が拡張するなどの,正常立位では異常とされる所見がみられることや少量の胸水や気胸が見にくいなどの点に注意すべきである.
5)呼気位撮影:
呼気時の撮影が有用なのは,気胸,中枢気道の狭窄や閉塞による空気とらえ込み現象を疑う場合あるいはCOPDなどの末梢気道の閉塞による過膨張を疑う場合などである.
6)肋骨撮影:
肋骨病変の評価に利用する.撮影管電圧は低電圧を用いて,正面,両側斜位撮影を行う.
c.正常像
正常の胸部正面像と側面像を示す(図7-1-7, 図7-1-8).心臓を中心とする縦隔陰影は,胸部単純像で中央に位置するので中央陰影とよばれる.中央陰影はおもに心臓と縦隔大血管からなるが,その辺縁の各部分が心臓や大血管のどの部分に相当するか,あるいは肺のどの部分に接するかは十分に理解しておく必要がある(図7-1-11).
肺門近くの主幹部の肺血管や気管支およびその周囲の間質,リンパ節などからなる陰影を肺門陰影という.肺門陰影は,通常左の方が1肋間高く,形や濃度に大きな左右差はない.肺門部より末梢の肺を肺野と称する.肺は多量の空気を含むために透過性は上昇する(黒く見える).その内部に肺紋理とよばれる分岐状の陰影がみられるが,これは肺動静脈によるものである.肺血管は,肺門部近くでは,その走行の角度から肺動脈,肺静脈の鑑別が可能であるが,末梢では肺動脈,肺静脈の区別は困難である.正常では胸壁直下1~2 cmの範囲内では血管陰影は見えない.また立位で撮影された胸部単純像では,下肺の血管陰影は上肺の血管陰影に比べて太いが,左房圧の上昇をきたす場合には,上肺の血管陰影が増強する.肺野の濃度(白さ黒さ)は,ほぼ左右対称である.微妙な左右差を見つけることはわずかな異常陰影を発見する契機にもなる.胸壁の軟部陰影は正常では左右差はなく厚みもほぼ左右対称である.
d.異常所見とその解析
1)X線単純撮影における組織間コントラストとシルエットサイン:
読影にあたって,活用すべき所見にシルエットサインがある.シルエットサインとは,“X線学的に同一の濃度(水と軟部組織など)を示す組織がその境界を実際に接している場合にはその境界が見えなくなる”という原理である.シルエットサインの理解にあたって重要なことは,単純撮影では,組織間コントラストが低いために,人体の組織は4つの濃度(空気(ガス),脂肪,水,骨(重金属))にしか分かれないという事実である.単純撮影像上の濃度は組織の前後の厚みにも依存するが,組織の前後の厚みが同一であれば同じ条件で撮影した場合には軟部組織と水は同一の濃度を呈し,軟部組織内部の状態を単純撮影で評価することはできない.したがって,逆に軟部組織(水)濃度を示す構造の辺縁が明瞭に見えるということは,その構造の濃度が異なる組織(実際にはガス)と実際に境界を接していることを示し(シルエットサイン陰性),正常で見えるべき境界が見えない場合は何らかの病変により空気の濃度が失われたことを示している(シルエットサイン陽性).例をあげれば,胸部正面像で,下行大動脈辺縁が正常で認識できるのは,下行大動脈とこれに接する左肺下葉の空気の濃度差があるためであるが,何らかの病変により左下葉の含気が減少すれば,下行大動脈の輪郭は不鮮明になる(図7-1-12).
2)中央陰影の異常:
中央陰影の異常には,心拡大や大動脈瘤などの心大血管の異常,縦隔腫瘤などがある.通常は中央陰影の輪の局所性の突出がその所見の中心になる.これらの所見を正しく意味づけるのには,中央陰影を構成する各辺縁を構成する構造は何かをよく理解しておくことが必要である(図7-1-11).
3)病変部位の表現:
単純撮影でも2方向撮影があれば,異常陰影の局在部位を解剖学的(右上葉など)に判断しうるが,1方向のみの撮影の場合,正面像における右中葉と右下葉の重なりなど解剖学的位置関係を正確に決定できない場合も少なくない.このような場合は,正面像では,上肺野,中肺野,下肺野などと表現される.正面像では,上肺野と中肺野の境界は第2肋骨前縁の高さ,中肺野と下肺野の境界は第4肋骨の前縁の高さにするのが普通である.
4)病変の性状:
肺野の異常陰影には,病変部の透過性が亢進する場合(黒くなる場合)と透過性が低下する場合(白くなる場合)がある.異常所見を発見した場合は,これを正しい鑑別診断に導くように所見を正しく記載する必要がある.異常陰影を発見した場合は,その位置,大きさ(最長径と最短径),境界の明瞭さ,辺縁の性状(整,不整),内部の状態(均一,不均一),形状,空洞や石灰化の有無などについて記載する.びまん性肺疾患に関しては,画像所見の詳細な解析や軽度の所見の検出には,高分解能CTを必要とする.
5)肺野の明るさの変化:
一側の肺野が反対側に比べて全体に透過性が亢進している状態をunilateral hyperlucent lungと称する.胸壁の疾患,肺胸膜疾患などさまざまな病態で生じるが,日常臨床の中で最も多い原因は,撮影時に軽度に斜位となり撮影された場合である.
6)正常構造の偏位:
無気肺では,肺の局所性の容積減少に伴って正常構造が偏位する.この偏位に気づくことは病変の発見に有用である.右上葉の無気肺では,右肺門部の拳上がみられるなどがその例である.正常構造に偏位があるかどうかの判断を正しく行うには,正常の画像によく慣れておく必要がある.
7)肺血管陰影の異常:
左房圧が上昇すると,上肺の血管陰影が増強し,下肺のそれと同様(equalization),さらに左房圧の上昇が高度になると下肺のそれより太くなる(cephalization).また胸壁直下まで肺血管陰影がみえるなどの肺血管陰影の増強は,左右シャントなどでみられる.逆に肺血管陰影の全般的減少は,Fallot四徴症などの先天性心疾患,局所性の血流減少は肺血栓塞栓症などでみられる.肺高血圧症では,主幹部肺動脈が拡張するのに対して,末梢の肺血管陰影はかえって減弱する.
8)肺門の異常:
肺門陰影の拡大は,主幹部肺血管陰影の拡大,肺門部リンパ節の腫脹,肺門部腫瘤などの場合にみられる.各々典型的な場合には,胸部単純撮影所見から鑑別可能であるものの,非典型的な所見を示す症例や腫瘤の正確な計測には造影CTを要する.
(2)CT, MRI, PETとその読影基礎
a. CT(computed tomography)
ⅰ)胸部画像診断におけるCTの役割
CT装置の技術的進歩を背景に,多臓器の詳細な形態情報が同時に,かつ簡便に得られるCT検査は,現在の胸部疾患の画像診断において中心的な役割を果たしている.特に多列検出器CT(MDCT)の登場と画像再構成コンピュータ技術の進歩によって,従来の横断断層像による精密形態診断法という役割から,病変の精密形態診断ばかりでなくスクリーニングの役割も同時に兼ね備え,さらに種々の再構成画像を生かして三次元的評価ができる画像診断法に変化してきている.もちろん,被検者のX線被曝に留意し,無用な被曝は避けなければならないが,臨床的必要性がある場合には,再構成画像も利用しMDCTの能力を最大限に生かす使い方をすることが大切である.
ⅱ)臨床に用いられる胸部CTの種類
1)通常CT:
胸部病変の全体像を把握するために,深吸気位で肺尖から肺底部までの全体をカバーした連続CT像で,スライス厚は5~8 mmが用いられる.最近のMDCTでは薄いコリメーションを用いて呼吸停止下に全肺を撮像したスキャン生データから種々のスライス厚の画像が再構成可能で,通常CTはその1つとして作成される.スライス厚の異なる画像を得るには再スキャンが必要であったMDCT以前のCTとは異なることに留意が必要である.
胸部CTの画像データは1つであるが,ウインドウレベルとウインドウ幅を変えることによって画像は変化する.日常臨床では,肺野条件と縦隔条件の2種類を用いるのがふつうであるが,骨変化の観察には骨条件を追加する場合がある.
2)高分解能CT (HRCT)(図7-1-13):
CTのもつ空間分解能を最大限に高めた画像で,①薄いスライス厚(1~2 mm),②高分解能アルゴリズム(画像再構成ソフトの1つ),③小さな画像再構成領域(FOV)(通常18 cm前後で片肺をカバー),の3つの条件を満たすものを指すが,③は必ずしも必須条件ではない.
びまん性肺疾患や肺野型肺癌の微細な形態診断が必要な場合に作成され,通常は肺野条件で観察される.MDCT以前は通常CTの撮影後にHRCTが再撮影されていたが,MDCT登場後は,再撮影せずにスキャン生データからHRCT像を再構成するので,被曝は増えない.
3)薄層造影CT:
複雑な軟部組織や血管を含む肺門部や縦隔に生じた病変を詳細に解析するためのCTで,造影剤の急速注入下に撮影された,3 mm以下の薄いスライス厚の連続CT像をいう.MDCTでは造影CTのスキャン生データから胸部全体の薄層造影CT像を作成することが容易である.
4)呼気CT:
CTは通常深吸気位で撮影されるが,閉塞性肺疾患においては,呼気CTを追加することによって,吸気CTではとらえがたいエアトラッピング(air trapping)をCT値の変化が少ない領域として検出可能である.したがって,閉塞性肺疾患のような呼吸機能異常が疑われる患者においては,吸気CTを撮像したあと追加して深呼気位でのスキャンを行う場合がある.
5)種々の再構成画像:
MDCTで得られる薄層連続横断画像データを用いると,任意の断面で再構成した画像(MPR像,図7-1-14)や複数の連続画像の同一座標最大値を集めた最大値投影像(MIP像),三次元的な視野表示をした三次元画像(図7-1-15),気管支鏡と同じ視野になるように再構成したCT気管支鏡などの再構成画像もワークステーションで作成可能で,画質も高い.臨床での必要に応じて横断像で認められた病変の評価がよりわかりやすくなるような再構成画像が追加される.
ⅲ)胸部CTの読影の基礎
1)肺野結節性病変:
肺野結節のCT検査でまず評価しなければならないのは,結節の形態変化と縦隔肺門リンパ節腫脹の有無である.精密形態評価には,結節全体を含む領域で撮像された連続HRCTを用い,リンパ節評価には通常造影CT(もし可能なら薄層造影CT)を用いる.結節の造影効果をCTで評価する場合は,造影の前後で薄層CTを施行し,同一断面でCT値を比較する.
結節の形態の着目点としては,辺縁の性状(整不整,明瞭さ),内部の性状(CT値の程度と均一さ,石灰化の有無,気管支透亮像の有無),周囲気管支や肺動静脈と結節の関係,があげられる.肺癌では辺縁の不整(スピキュラ)や分葉状の発育(ノッチ)がみられる頻度が高く,複数の気管支,肺動静脈が結節に収束し,胸膜の陥入像がみられる(図7-1-13).一方,良性結節では辺縁が明瞭な球状結節や気道分岐に沿った帯状陰影を示す傾向が強い.ただし,最終診断には気管支鏡やCTを用いた生検による組織診断が必要である.
肺癌におけるリンパ節評価では,短径1 cm以上のリンパ節腫脹を転移陽性と判断する基準が一般的であるが,正診率は60~70%であるので,手術適応の判断には組織診断を組み合わせて判定する必要がある. 結節の造影効果から良悪性の鑑別が期待されたが,造影効果そのものでは悪性を判断できないことが明らかになっている.しかし,結節の造影効果がみられない場合には,結核腫などの肉芽腫である可能性が大きい.
2)肺門部病変:
肺門部病変では気管支,肺動静脈の複雑な構造内に病変が存在するので,薄層造影CTを用いて評価を行う.肺塞栓症などの血管病変の診断においても,同様の撮像法を用いる.
肺門部肺癌の評価では,病変の存在部位と病変の広がり,および病変と隣接する縦隔構造,気管支,肺動静脈との関係,の2点について連続画像を観察し,既存構造を確認しながら判断する.必要に応じてMPR画像を用いて三次元的な進展を評価する(図7-1-14).肺塞栓症の診断では,十分に造影された肺動脈内の欠損の有無を診断する.MDCTを用いた高画質の薄層造影CTで診断した場合には,区域から亜区域レベルの肺動脈内の塞栓の有無に関して血管造影に劣らない正診率が得られることが報告されている.したがって,肺塞栓症が疑われる患者においては,薄層造影CTが第一選択の画像検査と考えてよい.
3)びまん性肺疾患:
病変が全肺にびまん性に分布している場合には,通常CTに加えてHRCTを作成する.MDCTで薄いコリメーションを用いる場合には撮影後に任意の部位のHRCT像を同じデータから作成することが可能であるので,改めてHRCTスキャンを行う必要がない.また,肺野病変の評価そのものには造影は不必要である.肺内における病変分布と二次小葉レベルの病変分布を評価する.
a)病変の肺内における分布:上下肺,肺内外層による違いに加えて,腹側背側による違い,区域性か非区域性か,といった分布の特徴をとらえる.細菌性肺炎では区域性分布,誤嚥性肺炎では背側肺に分布する頻度が高く,非感染性炎症疾患では非区域性分布を示す場合が多い.
b)二次小葉レベルの病変分布(図7-1-16)と鑑別診断:HRCTでは二次小葉を構成する構造物の中で,終末細気管支に伴走する肺動脈,小葉辺縁を走行する肺静脈まで描出可能である.これらの構造物をランドマークにすると,二次小葉内の病変分布の評価が可能になる.
ⅰ)気道中心性病変:急性,慢性の気道炎症性疾患は気管支肺動脈束とその周囲肺胞に病変を形成する.病変の進展に伴って,より広範囲の周囲肺胞に及ぶ.早期病変では,HRCT上,気管支肺動脈束と隣接肺野の変化が主体で,小葉辺縁構造(肺静脈,小葉間隔壁,胸膜)は正常である.びまん性汎細気管支炎,肺結核,気管支肺炎などの病変は小葉中心性粒状影が優位であることが多く,マイコプラズマ肺炎や種々の細気管支炎などは気管支肺動脈束腫大が目立つことが多い.
ⅱ)リンパ行性病変:肺胞壁を狭義間質というのに対して,気管支血管周囲結合織,小葉間隔壁,胸膜を広義間質とよぶ.リンパ管を豊富に含む広義間質に沿って進展する病変はHRCTで,気管支肺動脈束と小葉辺縁構造の両者の腫大を生じる.代表疾患として癌性リンパ管症,リンパ増殖性肺疾患,サルコイドーシス,塵肺,肺水腫などがあげられる.
ⅲ)血行性病変:病変が血行性に広がる場合には,肺小葉構造と一定の関係をもたないランダムな分布を示す小粒状影を形成する.悪性腫瘍の血行性転移や粟粒結核が代表的である.
ⅳ)肺胞性病変:HRCTでも肺胞壁の病変と肺胞腔の病変は区別できず,肺胞性病変は基本的に種々の程度の肺野高吸収域として描出される.高吸収域の程度は,軟部組織と空気の比率で決定され,含気が多ければ内部に血管影が残存するすりガラス影,含気が消失すれば浸潤影となる.肺胞性病変には,感染症,肺水腫,非感染性肺炎,肺出血,悪性リンパ腫など多くの病態が含まれ,高吸収域そのものでは,これらの区別はできないが,病歴や臨床所見,病変の分布の特徴を合わせて鑑別診断を進める.たとえば,区域性,連続性の肺野高吸収域は感染症の頻度が高く,非区域性斑状分布は非感染性肺炎で高率にみられる.さらに,構造改変の有無も重要で,構造改変があれば慢性の線維化器質化病変の存在を示唆する所見となる.
4)縦隔病変:
縦隔病変では石灰化や脂肪の有無,造影効果の有無,囊胞成分の性状といった情報が鑑別診断上有用である.したがって,原則として造影前後の通常CTが必要になる.病変が小さい場合,あるいは病変の血流を評価したい場合には,病変部の薄層CTを用いる. 縦隔腫瘤は発生部位に特徴があることがよく知られており,病変の局在(前縦隔,中縦隔,後縦隔)は鑑別診断上重要である.また,辺縁の性状,浸潤性および周囲血管構造との関係は手術の術前情報として重要である.
b. MRI(magnetic resonance imaging)
ⅰ)胸部画像診断におけるMRIの役割
MRI技術の進歩も著しいが,通常の胸部MRIは安静呼吸運動下で撮影されるためにCTと比べ空間分解能が低く,また,肺野は含まれる水素原子数が少ないことに加えて複雑な含気構造をしているために十分な信号が得られない領域でもある.しかし,一方で,軟部組織の濃度分解能はCTよりすぐれる.したがって,MRIが適応となるのは,軟部組織内の微細構造などCTに付加する情報が得られる場合で,縦隔,肺門,胸壁が中心となる. もう1つのMRIの大きな利点は,通常のMRIでは一定の流速以上の流れをもった血管は無信号となるので,単純MRIにおいて信号をもつ軟部組織と区別できる点である.したがって,ヨード造影剤禁忌で造影CTができない患者においては,MRIが第一選択の画像診断となる.
ⅱ)臨床で用いられる胸部MRIの種類
胸部領域のMRIではCTに付加する情報を得ることが目的であるので,胸部全体ではなく,病変部を中心に限られた領域を検査する場合が多い.スキャンは8~10 mmのスライス厚の横断像が基本で,T1強調像とT2強調像を撮像する.通常は心拍動の影響を除外するために心電図同期を併用して撮像することが多い.ただ,心拍数によって繰り返し時間(TR)が規定されるために,心拍数によってはTRが本来のT1強調画像よりも長くなり,画像コントラストが変化することに注意する必要がある.この横断像に加えて,病変の部位,あるいは評価したい血管と病変との関係などを考慮して,冠状断,矢状断などの画像を追加するのが普通である.また,腫瘍性病変の場合には,ガドリニウム造影剤を投与した後にT1強調画像を撮像すると,病変の血流や内部性状,あるいは周囲構造との関係がより明瞭になることが多い.T1,T2強調像に加えて,最近では,種々の脂肪抑制画像,拡散強調画像などの臨床応用がすすめられている.
また,血管を高信号に描出する撮像法を用いて得られた薄層の連続画像から,ワークステーションを利用して,MIP像や三次元画像で表示した血管造影に近い画像(MRA)が得られる.一方,胸壁の病変などでは,撮像範囲が限定されるので,表面コイルを用いることによって,高分解能MR画像が得られる.
ⅲ)胸部MRIの読影の基礎
MRIの形態評価に用いる基準はCTと大きく変わることはない.腫瘍性病変の評価が中心になるが,基本的に複数方向の画像を解析して,病変の存在部位,既存構造との関係をとらえる.リンパ節腫脹判定の基準もCTと同様に短径1 cm以上を用いる.ただ,MRIを評価するときに注意しなければいけないのは,通常のMRIでは大血管は無信号が原則であるが,流速が遅くなったり,乱流が生じると不規則な信号が発生する点である. MRIでは,CTにおけるCT値のような定量的指標はなく,MRIにおける信号強度は相対的なものである.したがって,組織ごとの固有のMR信号強度といったものは存在しないが,T1強調像およびT2強調像での信号強度の組み合わせから,水,出血,脂肪といった組織を推測することができる.特に,縦隔腫瘍ではCTでわからないような内部構造の微細な変化や,出血,脂肪,囊胞の評価が可能で,鑑別に役立つ情報が得られる場合がある(図7-1-17). また,腫瘍性病変の血管浸潤,胸壁や骨への浸潤の評価では,血管や骨構造周囲に存在する脂肪層が保たれているかどうか,血管や骨内部に腫瘍組織の信号がみられるかどうかの評価が重要である.
c.PET(positron emission tomography)
ⅰ)胸部画像診断におけるPETの役割
CTやMRIが主として形態診断法であるのに対して,PETは機能診断法である.PETは陽電子を放出する放射性同位元素で標識された放射性薬剤を患者に投与し,その分布や動態をPET装置でとらえることにより,体内で生じている代謝変化を診断する.現在最もよく使われているのは,18Fで標識したFDG(fluoro-2-deoxyglucose,グルコースの誘導体)を用いた肺癌診断である.18F-FDGはグルコースと同じ経路で細胞内に取り込まれるが,グルコースはグルコース-6-リン酸から解糖系に進むのに対して,18F-FDG-6-リン酸は代謝を受けることなく細胞内にとどまる.したがって,18F-FDGの強い取り込みをとらえることによって,形態ではわからない肺癌などのグルコース代謝の高い病変を検出することができる.
ⅱ)臨床で用いられるPET画像の種類
当初はPET単体の装置で空間分解能の弱点があったが,現在はCT装置を組み合わせたPET-CTが主流であり,CTでの形態情報とPETの代謝情報を融合画像として評価できる.最近,PET-MRI装置が新たに臨床に登場し,臨床応用が始まっている.
ⅲ)肺癌におけるPET読影の基礎
PET導入当初は,肺野結節の良悪性の鑑別における役割が期待されたが,1 cm以下の小結節やすりガラス結節では偽陰性が多いこと,また逆に結核種などの肉芽腫では偽陽性となる場合も多いことから,この目的で検査が行われることは少なくなっている.しかし,リンパ節転移の診断では,明らかにCTでの大きさによる診断よりも正診率が高いことが報告されており,また,PETでは全身の遠隔転移の検索も可能であることから,肺癌が見つかった後の病期診断には不可欠な診断法となっている(図7-1-18).さらに,放射線治療や化学療法後の効果判定においても,残存腫瘍や再発腫瘍の検出にも有用である.
視覚評価においては正常で集積があまりみられない部位に強い取り込みがみられた場合に陽性と判定し,CTを参考にその解剖学的部位を判断する.18F-FDGの強い取り込みはグルコース代謝が亢進していることを意味しているので,病変を疑う根拠になるが,正常でも高い集積を示す部位があることを認識しておく必要がある.脳や心臓は,その代謝の特徴から集積が強く,腎尿路系は排出経路として高集積を示す.その他の生理学的集積部位として,口蓋扁桃,喉頭,肺門リンパ節,胃,腸管,筋肉などがある.
PET-CTでは視覚的評価が中心であるが,取り込みの程度を判断する半定量的な指標として,SUV値を用いる.
4)特殊検査
(1)気管支鏡検査
気管支鏡検査は,呼吸器疾患の病態解析・確定診断のため,肺につながる肺外気管支と肺内にある肺内気管支から気管支内腔を観察し,気管支を介して病変の細胞・組織を回収し,また気道病変に対し気管支腔内から治療を行う検査である(表7-1-8).消化器内視鏡という用語に対応するべく,“気管支鏡”から“呼吸器内視鏡”という呼称が用いられるようになってきている.池田茂人の軟性気管支鏡の開発に始まり,国内の内視鏡を開発する企業の努力により,日本は気管支鏡検査の臨床・研究において世界のトップを走ってきている.
形状からの気管支鏡の分類では,硬性で直線状の光学視管をもちステント留置などの治療に用いることの多い硬性気管支鏡と,気管支鏡検査の大半を占める診断目的には軟性の挿入部をもつ軟性気管支鏡を用いることがある.用いる光などでの分類では,白色光を用いた通常の気管支鏡,自家蛍光気管支鏡,超音波気管支鏡などがある.軟性気管支鏡は,開発当初から1990年代初頭までは,グラスファイバーを束ねたファイバースコープであったが,以後小型化したCCDを使用したビデオスコープが登場し現在では広く普及している.
診断または治療において気管支鏡検査が必要であれば適応となるが,気管支鏡検査においても,検査結果の重要性が検査のリスクを上回る場合に検査を予定するべきである.
気管支鏡検査の禁忌には,著しい心肺機能低下,著しい全身衰弱,出血が止まりにくい状態,高度な酸素化障害などがある.合併症としては,気道内出血,気胸,リドカイン中毒・ショック,低酸素血症,不整脈などがあり,注意を要する.合併症を回避するためにも,気管支鏡検査前に既往症,全身状態,血圧,血液・生化学検査,心電図,動脈血液ガス分析,肺機能検査,感染症の有無などを調べておくことが肝要である.また,検査中のパルスオキシメーター,血圧,心電図をモニターしながら,厳重な観察を行うべきである.
気管支鏡検査の準備では,画像診断から気道内病変の有無の検討,使用すべき気管支鏡の種類,末梢病変へ到達するための気管支ルートの同定,経気管支吸引針生検を行うべきリンパ節の決定などを行っておく.前処置では検査約3時間前より禁飲食,必要に応じて硫酸アトロピンの筋注(重症の不整脈,心不全,排尿障害,緑内障などでは禁忌),必要に応じ鎮静薬を併用する.リドカイン過敏症のないことを確かめ,咽頭喉頭にリドカインで局所麻酔を開始する.気管支内にも噴霧するリドカインも含め,リドカインの検査中総投与量は5 mg/kg以内に収まるようにし,特にリドカイン中毒になりやすい小柄な女性,高齢者,肝腎機能障害者に注意が必要である.リドカイン中毒の症状には意識障害(呼びかけへの反応低下),振戦,痙攣などがあり,呼吸の確保が大切で気管内挿管が必要になることもある.鎮静薬を使用下ではリドカイン中毒の初期症状である意識障害がわかりにくく,注意を要する.
通常の気管支鏡検査で用いる気管支鏡の外径は5~6 mm程度であり,区域気管支から亜区域気管支までの観察が可能である.最近普及してきている外径4 mmの気管支鏡では,可視できる気管支の範囲は1~2分岐程度,より末梢に拡がる.
適応の大部分を占める診断目的の気管支鏡検査では,肺癌を中心とする腫瘍性病変,肺炎,抗酸菌などによる呼吸器感染症疾患などを対象としている.腫瘍性病変に対する気管支鏡検査では,気管支鏡で回収した細胞・組織から細胞・組織学的診断を行うことが最も大切であり,多発病変の有無,気道内病変の進展の程度などを観察し,手術適応・術式の判断,病期診断などを行う.気管支鏡で可視できる病変に対しては,観察の後,直視下生検,擦過細胞診,気管支洗浄などを行う.気管支鏡で可視できない病変に対しては,挿入できる部位まで気管支鏡を誘導し,X線透視下に生検鉗子を病巣に到達させ,経気管支生検,擦過細胞診,洗浄を行う(図7-1-19).病巣に気管支が入っていない病変,小型病変,すりガラス影などの末梢病変の場合,気管支鏡で細胞・組織学的診断を得ることができないことがあり,CTガイド下生検,開胸・胸腔鏡下の切除が検討されることもある.
びまん性肺疾患や呼吸器感染症の気管支鏡診断に,気管支肺胞洗浄(bronchoalveolar lavage:BAL)が用いられることがある.BALは,気管支鏡の先端を亜区域支などに楔入し,生理食塩水の注入・回収を繰り返し,末梢肺胞領域に存在する細胞成分や微生物を回収する方法である.生理食塩水の注入量は75~150 mL程度であり,わが国では1回50 mLを3回注入することが多い.陰影の局在が限局していれば,その区域から行うが,中葉,舌区を含めてびまん性に陰影が存在する場合には注入した生理食塩水が回収しやすい中葉,舌区で行う.生食の注入開始時に気管支内に漏れていないかどうか,患者の咳の有無,呼吸状態に注意を払う.生食の回収は注射器を手でゆっくり引いて行うようにする.強く引きすぎるとかえって気管支内腔がつぶれ回収が悪くなり,出血も混じるようになるので注意する.洗浄液の塗沫標本を作製し細胞診,抗酸菌などの確認と,細菌,真菌培養,リンパ球サブセットなどを提出する.
(2)自家蛍光気管支鏡
重喫煙者,喀痰細胞診異常,気管支扁平上皮癌の既往のある場合などで,気管支鏡検査で前癌病変,上皮内癌,上皮内浸潤が発見されることがある.通常使用する白色光では,前癌病変や上皮内癌などの丈が低く色調に変化がない病変は発見が困難である.自家蛍光気管支鏡は,正常気管支表面に青色波長領域の励起光を照射することで緑色波長領域の自家蛍光が生じる.気道上皮が厚くなっている前癌病変や上皮内癌などでは気管支鏡に帰ってくる自家蛍光が病変の領域で減弱しており,正常気管支とのコントラストから前癌病変,上皮内癌,上皮内浸潤などを発見することができる(図7-1-20).
(3)中枢気道に対する気管支腔内超音波断層法
扁平上皮癌を中心とする腫瘍性病変での気管支壁深達度診断は,光線力学的治療(PDT)を代表とする気管支内視鏡治療の適応や手術適応などを決定するうえで大切な所見であり,気管支腔内超音波断層法(endobronchial ultrasonography:EBUS)で深達度診断を行うことがある.また,気道壁を中心とする疾患の病態解析,ステント留置などの呼吸器インターベンションを予定する場合で,留置部位の気道壁内の軟骨の状態,気道内径の計測などにEBUSを用いる.
臨床例において気管から亜区域枝までの気管支では,プローブ自体をバルーンシースに挿入した後バルーンシース先端のバルーンを2~4 mLの生食で膨張させ,気管支内腔面との間の空気を排除し行う.20 MHzのラジアル型細径超音波プローブでは肺外気管支の軟骨部・肺内気管支では,5層構造を示し,肺外気管支の膜様部は,3層構造を示す(Kurimotoら,1999)(図7-1-21)ことがわかっており,病変部での層構造の変化から深達度診断を行う.
(4)超音波ガイド下経気管支吸引針生検(endobronchial ultrasound guided transbronchial needle aspiration:EBUS-TBNA)
convex型超音波探触子を気管支鏡先端に装備した超音波気管支鏡が開発される前には,TBNAはCTなどで対象病変の位置を予想しながら,ガイドなしに針を気管支壁外の病変に穿刺していた.2004年にconvex型超音波気管支鏡が開発され,対象病変の位置を確認し刺入していく針をリアルタイムに観察することが可能になった(図7-1-22).肺癌の縦隔・肺門リンパ節転移診断,良性疾患特にサルコイドーシスの診断ではEBUS-TBNAについて多くの報告があり,現在縦隔鏡検査からEBUS-TBNAに置き換わりつつある.
(5)ガイドシースを用いた気管支腔内超音波断層法(EBUS using a guide sheath:EBUS-GS)
本法は,ラジアル型細径超音波プローブのまわりにガイドシース(guide sheath:GS)を被せて肺末梢病変までもっていき,EBUSで病変を描出できたことで病変に到達したことを確認後,超音波プローブのみを抜去し,残したGSに生検鉗子を挿入し生検する手技である(Kurimotoら,2004)(図7-1-23).含気のある正常肺は超音波の反射が生じるため,EBUSでは観察できないが,細径プローブを気管支に挿入し病変部の近傍までいき,細径プローブの探触子が病変に接すると,病変を明瞭に描出することができる.海外では肺末梢病変の細胞・組織学的診断の多くは,CTガイド下経皮針生検が行われることが多いが,EBUS,気管支ナビゲーションの使用が可能になり海外でも普及してきている.
(6)気管支ナビゲーション
近年,コンピューターの進歩で気管支鏡検査前にCT画像から仮想気管支内視鏡(virtual bronchoscopy)を作成し,肺末梢病変につながる気管支の枝の同定(気管支のナビゲーション)を行うことが可能になり,臨床現場で使用されるようになって(図7-1-24)国内外で急速に普及してきている.また,自動車のナビゲーションと同様に仰臥位の患者の背中の下から磁場を発生させ,気管支内の鉗子先端の位置を仮想画像の中で確認しながら病巣に近づく方法も開発され,海外ではいくつかの報告(Gildeaら,2006)がある.
(7)経皮的超音波検査
体表からの経皮的な超音波検査では,肋骨,肩甲骨などが邪魔になることがあるものの,胸水,血胸,臓側胸膜直下の無気肺・病変などは明瞭に描出される.臨床においては,胸水に対する胸腔穿刺,胸腔ドレナージを施行する時に穿刺部位の確認のため,超音波検査は不可欠の検査手技である.臓側胸膜直下の病変では,経皮的に超音波ガイド下肺生検も可能である.
(8)気管支内視鏡治療
肺癌を中心に増加してきた呼吸器疾患の中で気道を中心とした病変では,気管支鏡治療は効力を発し,特に呼吸を維持するためには気道の開存を確保することは必要である.気管支内視鏡治療には,肺門部早期肺癌に対する光線力学的治療,気道狭窄に対するステント治療などがある.
a.肺門部早期肺癌に対する光線力学的治療
光線力学的治療(photodynamic therapy:PDT)は,腫瘍親和性のある光感受性物質の投与後,腫瘍組織にレーザーを照射することにより光化学反応を引き起こし,腫瘍組織を変性壊死させる治療法である.腫瘍組織にレーザーを照射することで,光感受性物質が一時的に励起され,再び基底状態に戻る際に癌組織内の三重項酸素から一重項酸素(活性酸素)が発生し癌組織を選択的に変性・壊死させる.保険適応は,早期肺門型肺癌以外に,表在性食道癌,表在性胃癌,子宮頸部初期癌および異形成がある.肺癌に対する適応である中心型早期癌では,気管支鏡で腫瘍の末梢側辺縁が確認できる直径1 cm以下の小さな腫瘍で,気管支壁浸潤が軟骨層の内側にとどまるものが最も治療効果が高いとされている.亜区域支より末梢側に浸潤のある腫瘍で末梢側の浸潤範囲の確認ができない場合,また軟骨層をこえている場合では,レーザーが十分に届かない可能性があり治療効果が不確実になるので注意を要する.
b.気道狭窄に対するステント治療
気管狭窄に対するステント留置は気流制限による呼吸困難を訴える患者の症状を劇的に改善し,QOLを向上させる有用な治療手段である.最近,欧米では呼吸器インターベンション(interventional pulmonology)として注目されている.臨床的には気道ステント留置の適応は,①腫瘍の進行性局所増大により気道の確保が難しく,その他の治療法が適応でない場合(たとえば頻回にレーザー治療などが必要な場合に最終手段として行われるもの),②不安定な気道状態を呈するもの(披裂,気管気管支瘻や気管気管支軟化症なども含む),③狭窄度50%以上で呼吸困難などの呼吸器症状を有するもの,などである.さらに医学倫理的な条件としては,①推定生存期間が4週間以上見込まれるもの,②ステント留置によりあきらかに気流制限改善などの肺機能的な改善が予測できるもの,③医学経済面でコストベネフィットが期待できるもの,などである.
中枢の気道閉塞は,肺癌,食道癌,種々の癌の縦隔リンパ節転移,転移性気管内腫瘍などにより起こる.気管支内腔腫瘍進展性閉塞,気道壁外圧排性閉塞と混合性閉塞がある.気道壁外圧排性閉塞はステント留置の適応だが,気管支内腔腫瘍進展性閉塞ではNd-YAGレーザー,アルゴンプラズマ凝固法,高周波治療,凍結治療,バルーン拡張や化学療法/放射線治療で内腔の開存が不十分である場合,また再閉塞が予想されるときにステント留置を考える.
気道ステントの種類はシリコンステントと,ステンレスやナイチノールなどの自己拡張性金属ステントがある.さらに新しいハイブリットステントとくに最近フルカバータイプができ,金属疲労が少なく壊れにくく取り出しも可能である.シリコンステントの留置において,自発呼吸を残した全身麻酔下で硬性気管支鏡を用いる手技は臨床的に安全で確実であり,ゴールドスタンダードと考えられる.従来の金属ステントは気管支ファイバーで留置することは簡単だが,一度留置すると回収および再留置は困難であり,肉芽形成による再閉塞や金属疲労で壊れるという欠点があるため適応が限られている.
5)肺機能による評価
(1)スパイロメトリー(spirometry)
吸気と呼気からなる呼吸運動を評価する.吸気では横隔膜と肋間筋が収縮することによって横隔膜が腹側に移動し,胸郭が拡張する.この結果,胸腔内は陰圧となり肺は拡張し空気が肺内に流入する.呼気時には筋肉が弛緩するので呼気終了時には拡張した胸郭は吸気開始の状態にもどるとともに胸腔内圧は上昇し陽圧に傾くので肺内の空気は押し出され呼出される.スパイロメトリーはこのような呼吸運動を評価する機能検査である.
a.方法
胸郭の運動を妨げないように着衣をゆるめ,最大吸気位から最大呼気位まで間断なく呼気努力を行う.まず,安静に換気し,ついで最大吸気位まで最大限の吸気努力をした後に最大限呼出するが,このときにはゆっくり呼出し速度は意識しない.ついで,努力性肺活量(forced vital capacity:FVC)の検査では最大吸気位から最大呼気位までの呼気を可能な限り素早く呼出する.1〜2回の練習の後,3回実施し努力性肺活量と1秒間に呼出される量(1秒量,forced expiratory volume:FEV1)の最も大きい値を採用する.
b.肺気量分画と努力呼気曲線(図7-1-25)
スパイロメトリーによって測定可能な肺気量分画は,安静換気による1回換気量(tidal volume:TV)と肺活量(vital capacity:VC),努力性呼気検査時に測定される努力性肺活量と1秒量である.
努力呼気曲線は最大吸気位からできるかぎり速く最大呼気位まで呼出したときの呼気量をスパイロメトリー上に記録した曲線である.縦軸に呼気量を横軸に時間をとり,努力性肺活量,1秒量,1秒量の努力性肺活量に対する割合である1秒率(FEV1%=FEV1/FVC×100,GaenslerのFEV1%)を求める.TiffeneauのFEV1%はFEV1/VC×100 である.
c.肺気量分画と努力呼気曲線の評価
拘束性換気障害と閉塞性換気障害を評価する.
肺の換気能力はスパイロメトリーで測定される値,%肺活量と1秒率で評価される.肺活量は性別,年齢,体格,体位によって異なるので,実測肺活量と予測肺活量との割合で算出される%肺活量で評価する.%肺活量(%VC)=実測肺活量(VC)/ 予測肺活量(VC predicted)×100
予測肺活量は性別・身長・年齢から健常者として予測される肺活量の平均値である.Baldwinの式で求める.
男性:(27.63−0.112×年齢)×身長(cm)
女性:(21.78−0.101×年齢)×身長(cm)
%VCとFEV1の値から以下のように分類する.
正常:%VC≧80%,FEV1%≧70%
拘束性換気障害: %VC<80%,FEV1%≧70%
閉塞性換気障害: %VC≧80%,FEV1%<70%
混合性換気障害: %VC<80%,FEV1%<70%
ⅰ)拘束性換気障害
拘束性換気障害は,肺の弾性収縮力上昇あるいは胸郭の弾性収縮力上昇による肺の拡張性が障害された場合,横隔膜神経障害や呼吸筋障害による呼吸筋の収縮力が障害され肺の拡張性が障害された場合にみられる.
肺間質の炎症あるいは線維化:過敏性肺炎,特発性肺線維症,じん肺,膠原病に伴う間質性肺炎・肺線維症,など. 肺実質に病変:肺水腫,など. 胸郭の疾患:胸郭形成,脊椎側弯症,など 神経・筋肉疾患:横隔膜神経麻痺,重症筋無力症,筋萎縮性側索硬化症,など
ⅱ)閉塞性換気障害(図7-1-26)
閉塞性換気障害は,気道の狭窄や閉塞で気流が制限された場合にみられる.
慢性閉塞性肺疾患(chronic obstructive pulmonary disease:COPD),気管支喘息,びまん性汎細気管支炎,など.
COPDで気流閉塞が進行すると残気量が増加し全肺気量が増加する.さらに,残気量が増加すると肺活量が低下し混合性換気障害を示すが,根本は閉塞性換気障害である.
d.フローボリューム曲線とその評価(図7-1-27)
フローボリューム曲線(flow-volume curve:F-V曲線)は,横軸に肺気量(ボリューム,L),縦軸に各肺気量における呼出速度(フロー,L/秒),をとり,最大努力呼出時の呼気量と気流速度の関係を示す.
縦軸は各肺気量位での最大呼出速度(V・max)を示し,実際に測定したF-V曲線の縦軸は各肺気量位での最大呼出速度の値である.肺活量の75%以上の肺気量位の最大呼出速度は呼出努力に依存するが,75%以下では努力とは無関係で気道内径や虚脱しやすさと関係する.全肺気量から残気量までの50%肺気量位の呼出速度をV・50,25%肺気量位の呼出速度をV・25という.
正常ではF-V曲線は,ピークフローから呼気終末までほぼ直線的に呼出速度が減少する.
閉塞性換気障害:閉塞性換気障害の中でCOPD,特に気腫型のCOPDでは肺気量が増大しF-V曲線が左方に偏位し,曲線の形も凹状を示す.腫瘍・炎症・瘢痕などによる気道狭窄ではF-V曲線は台形を示す.
拘束性換気障害:肺線維症では肺気量が減少しF-V曲線が右に偏位し弾性収縮力増大による呼出速度が増すので曲線は上方に凸となる.
(2)残気量,機能的残気量と全肺気量(図7-1-28)
残気量(residual volume:RV)は最大呼気位で肺内に残存する気量,機能的残気量(functional residual capacity:FRC)は安静呼気位で肺内に残存する気量である.機能的残気量は安静呼気位で胸郭が拡張しようとする力と肺が収縮しようとする力が均衡されている肺気量である.スパイロメトリーでは測定できず,体プレチスモグラフ法(body plethysmography)あるいはガス希釈法で測定する.全肺気量(total lung capacity: TLC)は最大吸気位の肺気量である.
残気量の増大:特に呼気時に気流制限を認める(air trapping)COPDでは,吸気が完全に呼出できないので増加する.神経筋疾患では呼吸筋力低下のために十分に呼出ができず増加する. 残気量の減少:肺線維症では肺気量全体が減少し残気量も減少する.
機能的残気量も同様な原因で変化する.
全肺気量の増大:静肺弾性収縮力の低下(静肺コンプライアンスの増加)を認めるCOPD.
全肺気量の減少:静肺弾性収縮力の増加(静肺コンプライアンスの低下)を認める肺線維症や神経筋肉疾患.
(3)コンプライアンスとその評価(図7-1-29)
肺・胸郭の弾性収縮力(硬さ・縮みやすさ)は,弾性収縮力の逆数であるコンプライアンスで表される.弾性収縮力が縮みやすさを表すのに対してコンプライアンスは伸びやすさを表す.
コンプライアンスは胸郭コンプライアンス(thoracic compliance:CTOR)と肺コンプライアンス(lung compliance:CL)に分けられる.また,気流のない状態で測定する静肺コンプライアンス(static lung compliance:Cst)とある状態で測定する動的コンプライアンス(dynamic compliance:Cdyna)がある.通常は静肺コンプライアンスを測定する.
静肺コンプライアンスは気流のない状態で,肺の容積変化(ΔV)とそれに要した胸腔内圧変化(ΔP)から計算される.
静肺コンプライアンス=肺の容積変化(⊿V) / 胸腔内圧変化(⊿P) (L/cmH2O)
静肺コンプライアンスは,肺内外の圧差(口腔内圧−胸腔内圧)と肺気量変化から求めた肺圧量曲線から求める.臨床的には胸腔内圧は食道にバルーンを挿入して測定される食道内圧を用いる.静肺コンプライアンスの正常値は0.15〜0.30 L/cmH2O程度である.また,最大食道内圧(Pesomax)は弾性収縮力によって規定される.正常値は20〜25 cmH2O程度である.
弾性収縮力低下(静肺コンプライアンス上昇):COPDでは肺胞破壊のために上昇する.最大食道内圧は低下する.
弾性収縮力上昇(静肺コンプライアンス低下):肺線維症,胸膜肥厚.また,最大食道内圧は上昇する.
(4)呼吸抵抗,気道抵抗
気道抵抗(airway resistance)は,口腔と肺胞との間にある気道の粘性抵抗で,呼吸抵抗(respiratory resistance)は気道,肺組織および胸郭の抵抗の総和である.気道抵抗は気道狭窄,肺切除,などで上昇する.
(5)肺拡散能
肺胞に達した大気に含まれるガスと毛細血管中のガスの交換は受動的,物理的な拡散によって行われる.二酸化炭素は酸素と比べて溶解性が高く約20倍拡散しやすいので,実際に問題になるのは酸素である.一酸化炭素を用いた肺拡散能が測定される(DLCO).拡散障害は,肺胞と毛細血管が接する面積の減少,肺胞と毛細血管の距離の増大でみられる.
拡散面積の減少:COPD,肺切除
拡散距離の増大:肺線維症 ,間質性肺炎,肺水腫
(6)動脈血ガス分析,酸塩基平衡
動脈血ガス分析では,pH,酸素分圧(PaO2),二酸化炭素分圧(PaCO2),炭酸水素イオン濃度(HCO3−)を知る.血液中の酸素は,血漿中に物理的に溶解する溶解酸素と,ヘモグロビン(Hb)と結合する結合酸素がある.酸素飽和度(SpO2)は酸素に結合しているHbの割合を示す.PaCO2は有効肺胞換気量で規定され肺胞低換気で上昇し,過換気で低下する.動脈血酸素分圧(PaO2)による酸素化は,大気中の酸素濃度,肺胞換気量,拡散能,換気・血流不均等,シャント,などで規定される.
動脈血中のpHは7.40±0.05の範囲に維持されるように調節されている.酸塩基平衡を評価するには,基本的に動脈血pHとPaCO2で行うが,Henderson-Hasselbach式によって算出されるHCO3−を用いる方法がある.
pH=6.1+log([HCO3-] / [β×PaO2])
(βはCO2の血漿に対する溶解度で通常0.03 mEq/L・torr)
pHの低下はアシドーシス,上昇はアルカローシスの存在を示す.pHの変動が肺の換気に由来する場合には呼吸性アシドーシスあるいはアルカローシス,呼吸ではなく腎機能などの代謝に由来する場合には代謝性アシドーシスあるいはアルカローシスとよぶ.
呼吸性アルカローシス:過換気によるPaCO2の低下
呼吸性アシドーシス:低換気によるPaCO2の上昇の喪失
代謝性アルカローシス:嘔吐や下痢によるHCO3−の喪失など
代謝性アシドーシス:糖尿病や腎不全によるケトン産生など
6)呼吸器疾患の分子生物学
(1)呼吸器疾患における分子生物学の意義
a.呼吸器疾患の現在と未来
現在,呼吸器領域疾患の社会的重要性は急増しつつある.気管支喘息,慢性閉塞性肺疾患や肺癌などの患者数,死亡者数は年々増加しつつあり,増勢に歯止めがかからない状況にある.世界的にも,WHOによる予測では,2020年の死亡要因の第3位が慢性閉塞性肺疾患(COPD),第4位が下部呼吸器感染症(肺炎など),第5位が肺癌,さらに第7位が結核と予想されるなど,呼吸器領域疾患による死亡者数の急増が予見されている.たとえば米国においては,過去40年間で,虚血性心疾患や脳血管障害による死亡数が著明に減少しているのに対し,慢性閉塞性肺疾患による死亡数は倍増の勢いにあり,今後も増加傾向が続くと予想されている.わが国においても,今後,さらに肺癌や慢性閉塞性肺疾患などの呼吸器疾患が急増することが予想されている.
また,新興・再興感染症も緊急の課題である.2003年に全世界に蔓延した重症急性呼吸症候群 (severe acute respiratory syndrome:SARS)や,今後の世界的流行・発生が懸念される鳥インフルエンザや新型インフルエンザなど,重大な新興感染症のほとんどは呼吸器を標的臓器とし,呼吸不全により宿主であるヒトを死に至らしめる.一方,再興感染症としての肺結核も,多剤耐性菌感染や高齢者結核などを中心に,その重要性が再認識されつつある.
このような状況にあって,分子生物学の応用による呼吸器疾患病態解明や治療薬新規開発がまさに切望されており,急速な研究進展が期待されている.
b.呼吸器疾患の分子病態生理
呼吸器内科学は,肺・気管支・胸壁など呼吸にかかわる臓器・器官を対象とする学問領域であり,呼吸器系のもつ生理学的な意義は,ガス交換による酸素化およびホメオスターシス維持にある.肺は,容積としては人体最大の臓器であり,また気相・液相・固相のすべてが密接にかかわる場であるという特徴がある.そのためか,肺・気管支を構成する細胞成分は約40種類以上ときわめて多岐にわたり,その複雑さがまた,感染・免疫・アレルギー・腫瘍など多彩な疾患が発症する素地ともなっている.一方,全身の臓器における生理機能は,加齢とともに低下するが,なかでも呼吸器は,加齢・老化による影響を最も顕著に呈する臓器の1つである.その原因としては,①呼吸器は,出生直後より絶えず外気と接触し,有害物質にさらされるリスクが高いこと,②呼吸運動という物理的負荷による機械的変化・変性が生ずること,などがあげられる.実際に,肺炎,肺癌,COPD,肺線維症などおもな呼吸器疾患は,高齢者に好発する傾向にある.
このように呼吸器病学領域は,感染症,炎症,免疫から腫瘍に至るまできわめて広範な分野にかかわる学問領域であるが,分子生物学はその基盤となるべき位置を占めている.そして,現時点における呼吸器疾患の分子病態解明の成果こそが,未来の呼吸器疾患臨床に繋がるものと期待される.
(2)炎症性呼吸器疾患の分子機序
a.気管支喘息
i)気管支喘息の分子病態
気管支喘息はきわめて多数の因子から病像が形成されており,その発症機序についてはいまだ解明されていないことも多い.気管支喘息の病態的・生理学的特徴として,慢性的な気道炎症・気道過敏性・可逆的な気流制限の3つがあげられる.気道炎症・気道過敏性があいまって気流制限が生じ,気管支喘息の症状が発生する.また,炎症が繰り返して起こった結果,上皮化生(杯細胞化)・線維増生・平滑筋肥厚・粘膜下腺過形成などが生じ,気道壁リモデリングが進展する.これによって喘息症状の重症化・不可逆化が進むと考えられる.
気道過敏性の機序はこれまで不明の部分が多かったが,喘息特有の気道炎症に起因していることが明らかになってきた.一方,炎症が完全に鎮まっても気道過敏性は健常人より高い状態が続くことが多いことから,炎症に起因しない気道過敏性の存在も考えられており,研究が進められている. 気道炎症の機序は活性化T細胞・好酸球・好塩基球・肥満細胞などの炎症細胞と,上皮細胞・線維芽細胞などの気道構成細胞が放出する炎症メディエーター・サイトカインなどの生理活性物質が相互反応を繰り返す炎症カスケードであると考えられている.この炎症カスケードにかかわる生理活性物質として,表7-1-9のような候補物質が想定されている.
しかしながら,気管支喘息の発症機序については未解明の部分が多く,その解明には関連遺伝子の探索を含めた研究が必須と考えられる.一方,近年,遺伝子改変マウスが次々と開発されており,疾患関連遺伝子の解明に有用であることが報告されている.気管支喘息の発症分子機序の解明についても,実験動物としての遺伝子改変マウスを用いた研究が重要であることが考えられる.
ⅱ)気管支喘息と脂質性メディエーター
気管支喘息は,気道平滑筋収縮,血管透過性亢進,血管拡張などによる気管支収縮を主体とする病態であり,種々の化学物質が複雑に関与していると考えられるが,近年,特にトロンボキサン,ロイコトリエンなどの脂質性メディエーターが重要な発症因子とされ,有効な治療標的となりつつある.脂質性メディエーターであるプロスタグランジン,トロンボキサン,ロイコトリエンなどはエイコサノイドと総称され,アラキドン酸を起点とする代謝経路の代謝産物である.アラキドン酸カスケードの代謝産物であるエイコサノイドは,ごく微量で多彩な生理活性作用を呈するのが特徴である.呼吸器系においても,エイコサノイドはきわめて重要な生理的意義を有することが示唆されている.
アラキドン酸は,炭素数20よりなる構造をもち,生体ではリン脂質から細胞質型ホスホリパーゼA2(cytosolic phospholipase A2:cPLA2)によって切り出される.この際に,同時にリゾPAF (Lyso-PAF)が生成され,リゾPAFから血小板活性化因子 (platelet-activating factor:PAF)が作られる.アラキドン酸は,図7-1-30に示すように,アラキドン酸カスケードとよばれる代謝経路を経てさまざまなエイコサノイドを生成する.その2つの大きな経路が,シクロオキシゲナーゼ(cyclooxygenase:COX)系および,5-リポキシゲナーゼ(5-lipoxygenase:5-LO)系である.プロスタグランジン,トロンボキサンはシクロオキシゲナーゼ系の代謝物であり,ロイコトリエンは5-リポキシゲナーゼ系の代謝物である.
PAFは,リン脂質性のメディエーターで,気管支平滑筋の収縮,サイトカインの産生刺激,神経伝達物質合成促進などの作用を示し,従来より気管支喘息発症メカニズムにおける重要な起因物質と想定されている.PAF受容体遺伝子の構造は,アフリカツメガエルの卵母細胞を用いたcDNAの発現クローニングにより,Honda らにより解明された.本クローンは全長約3 kbで1026 bpの翻訳領域をもち,ペプチド配列はアミノ酸342個よりなっていることが明らかにされた.またPAF受容体遺伝子を過剰発現もしくは欠損した遺伝子改変マウス(トランスジェニックマウス,ノックアウトマウス)が開発され,PAFに関する研究は急速に進展しつつある.
PAFは,好中球,好酸球,単球などで多量に産生される.PAFは以下の経路により合成される.まず第一に,リン脂質を基質としてcPLA2によりリゾPAFが生成され,さらに,アセチル転移酵素の作用によりPAFが作られる.産生されたPAFは,アセチルヒドララーゼにより速やかに分解される.PAFはリガンドとしてPAF受容体に結合することにより,その作用を発揮する.
従来より,日本人の4%にPAF分解酵素(アセチルヒドララーゼ)欠損症例が認められ,しかも,小児において酵素欠損と重症喘息に関連が認められることが報告されている.このアセチルヒドララーゼ欠損は,第6染色体,第9エクソンの点突然変異によるものであることが報告され,しかも,アセチルヒドララーゼ完全欠損はホモ型で出現すること(4%),部分欠損はヘテロ型で日本人の27%に存在することが示唆された.一方,北米の108例の検体の検討では,すべて野性型で,アセチルヒドララーゼ欠損は認めていない.この報告は,わが国におけるPAFと喘息の関連を明らかにする際,非常に重要なものと思われる.同時に,わが国と欧米各国の喘息有病率を考慮すると,アセチルヒドララーゼ欠損のみで,喘息発症を説明するのは困難であり,喘息発症メカニズムと遺伝的背景の複雑さを示すものとも考えられる.
発生工学の分野では,IshiiらがPAF受容体遺伝子を過剰発現するトランスジェニックマウス (PAF receptor overexpression transgenic mouse, 以下 PAFR-Tg マウス) を作製し報告している.本マウスは,特に気管・気管支においてPAF受容体遺伝子を過剰発現させることが解明されつつあり,PAF投与により著明な気道収縮を呈した.また,気管支喘息の特徴である気道過敏性とPAF受容体遺伝子過剰発現との関係を検討したところ,PAFR-Tgマウスにおいて,メサコリン気道過敏性が認められた.喘息におけるPAFの意義については,気道・肺胞系におけるPAF受容体の分布,ロイコトリエンなどほかのメディエーターとの相互作用が重要であることが示唆されたが,いまだ不明の点が多い.たとえば,PAFは,細胞増殖を司る細胞調節因子であり,気管支喘息に認められる気管支平滑筋増殖に関与している可能性が示唆されている.
上述のように,PAF,プロスタグランジン,トロンボキサン,ロイコトリエンなどは,多彩な生理活性作用を有するメディエーターであり,気管支喘息など呼吸器系炎症性疾患の発症メカニズムに寄与している可能性がきわめて高い. 特に,アラキドン酸カスケードの起点となる酵素であるcPLA2は,治療薬開発のターゲットとして有望であることが期待される.このcPLA2遺伝子を破壊したノックアウトマウス (cPLA2-KOマウス) が,Uozumiらにより報告された.このcPLA2-KOマウスは,エイコサノイドおよびPAFをほとんど産生せず,感作後の抗原暴露時に出現するべき気道過敏性が消失していることが示された.本マウスは,出生時,形態的奇形を呈しておらず,発育・成長においてもコントロールの野生型マウスと比べまったく差を認めていない.すなわち,cPLA2の遺伝子-酵素系を完全に抑制し,アラキドン酸カスケードの産生を阻害しても,生体の発生・発育に重大な支障をきたさない可能性を呈示する.この知見は,治療薬の開発・実用化の見通しに寄与すると考えられる.
b.間質性肺炎
特発性間質性肺炎は,特定疾患に指定されている難病である.病理学的には肺胞壁における炎症性細胞浸潤,線維芽細胞増生,コラーゲン沈着を呈する.また病態生理学的には,肺胞気と肺毛細血管の間のガス交換障害により,進行性の呼吸不全をきたすのが特徴である.特発性間質性肺炎に対して根本的に有効な治療薬剤は開発されておらず,治療としては保存的治療(酸素療法)が行われている.外科的には肺移植の選択肢もあるが,実施はきわめて困難であるのが実情である.間質性肺炎の発症分子機構は不明であるが,肺胞壁における炎症促進機序が基盤に存在しており,炎症性メディエーターなどの関与が推察されている.
間質性肺炎は,肺胞壁における炎症性細胞浸潤,線維芽細胞増生を基本病態とすることより,従来よりサイトカインの関与が推察されてきた.中でも,特に,TGF-β,TNF-α,IL-1,IL-6などは,炎症性サイトカインとして間質性肺炎への関与が示唆されている.最近では,間質性肺炎症例の集団を用いた遺伝子多型(gene polymorphism)の解析により,間質性肺炎発症に関与する候補遺伝子を探索する手法が研究に用いられつつある.
TGF-βについて,スペインのXaubetらは間質性肺炎症例群と健常群を比較し,TGF-β1のcodon 10および25を解析したところ,両群に有意な差は認められなかったが,30カ月間の経過観察で,codon 10 のPro allele の存在が間質性肺炎症例のA-aDO2 の増大に相関すると報告している.
TNF-α,IL-6については,英国のPantelidis らが間質性肺炎症例群と健常群を比較検討しており,TNF-αについては両群に有意な差は認められていない.一方,IL-6 のintron 4GG の存在は,観察開始時において間質性肺炎症例群で有意に高頻度であり,さらに,間質性肺炎症例の肺拡散能の低下に相関するという.一方,IL-1 について,Hutyrovaらが同様の検討を行ったところ,遺伝子多型性に有意差を認めなかったことを報告している.このように間質性肺炎に関与するサイトカイン遺伝子の研究が海外を中心に進められているが,特に遺伝子多型解析研究では集団の大きさが重要とされている.今後の研究では,大規模な集団を解析できるような体制づくりも要点になると考えられる.
間質性肺炎には高率で肺癌を合併することが知られており,間質性肺炎の死亡要因ともなっている.その原因は従来不明であったが,近年,癌遺伝子(oncogene)の関与が注目されつつある.特に,癌抑制遺伝子p53は,その遺伝子変異によって腫瘍発生を誘起することが報告されている.間質性肺炎に併発した肺癌症例において,p53の変異が多発していることが,わが国のTakahashiら,およびKawasakiらのグループによって報告されている.なお,Takahashiらは,Ⅱ型肺胞上皮細胞におけるras蛋白出現,および肺組織におけるK-ras遺伝子変異も,間質性肺炎症例の腫瘍発生にかかわる可能性を提起している. また間質性肺炎においても,エイコサノイドが関与する可能性が推察されるが,現時点において,エイコサノイド関連遺伝子を対象とした遺伝子多型解析研究は報告されていない.一方,動物モデルでは,ノックアウトマウスを用いた分子生物学研究により肺線維症成立機序におけるエイコサノイドの役割が検討されている.
ブレオマイシンは,悪性腫瘍(特に精巣腫瘍など)に対する化学療法薬として臨床的に使用されているが,重大な副作用として薬剤性の肺線維症をきたすことが知られている.このことより肺線維症の動物実験モデルを作製する手法として,ブレオマイシン投与が頻用されている.Nagaseらによれば,野生型マウスに,ブレオマイシンを気管内投与したところ,生理学的な肺の硬化,肺線維症に合致する病理組織所見(肺胞壁の肥厚,炎症性細胞浸潤,コラーゲン沈着)が認められた(図7-1-31).また,気管支肺胞洗浄液中のトロンボキサン,ロイコトリエンが増加していた.一方,同様にブレオマイシンを投与されたcPLA2-KOマウスでは,生理学的にも病理組織学的にも肺線維症様の諸症状が著しく軽減していた.気管支肺胞洗浄液中のトロンボキサン,ロイコトリエンは,ほとんど検出されなかった.以上の所見より,cPLA2が肺線維症の発症機序において大きな役割を果たしている可能性が示唆された.
間質性肺炎は,難治性,致死性という点において,社会的にもきわめて重大な疾患であり,治療薬の開発が切実に待たれている.間質性肺炎の発症にかかわる遺伝子を明らかにするため,遺伝子多型解析や遺伝子ノックアウトマウスを用いたアプローチなど,さまざまな研究が行われつつある.今後,間質性肺炎の発症機序にかかわる遺伝子が解明されることにより,間質性肺炎に対する有効な治療法・治療薬の開発および実用化が期待される.
c.ARDS(acute respiratory distress syndrome, 急性呼吸促迫症候群)
ARDSは,発症後短時間で肺水腫,低酸素血症を呈する急性呼吸不全であり,頻度の高い誘発原因として敗血症,胃液誤嚥(嚥下性肺炎),外傷などがあげられる.最近では,SARSやインフルエンザの直接死因としても注目されている.ARDSは,報告後30年以上を経た現在もなお死亡率が40~70%にも達する予後不良の疾患である.現在のところ,その治療は,人工呼吸管理,感染症対策といった対症療法が主体であり,有効性が実証された薬剤はない.
ARDSの発症機序には,サイトカインなど種々の炎症関連物質が複雑に関与している可能性が報告されている.しかしながら,その分子機構はいまだ明らかではない.現在,ARDSの有効な治療法,治療薬の開発および実用化を目的として,さまざまな研究アプローチがなされており,研究面では有望と思われる分子機序が報告されつつある.たとえば,PAF受容体ノックアウトマウスおよびcPLA2ノックアウトマウスを用いて,敗血症(LPS投与)および胃液吸引(塩酸気管内投与)モデルを検討したところ,いずれのモデルにおいてもノックアウトマウスでは肺水腫,呼吸不全が抑制され,生存率が改善することが観察された.この観察結果より,ARDS分子機序におけるPAFおよびcPLA2の関与が示され,新治療法への展望が見込まれる.また,ヘムオキシゲナーゼ1のノックアウトマウスを用いた虚血性肺損傷モデルでは,一酸化炭素(CO)吸入が有効であるとの報告がなされている.
また2005年には,アンジオテンシン変換酵素(angiotensin-converting enzyme:ACE)2のノックアウトマウスを用いた検討により,画期的な知見が得られた.ACE2は,アンジオテンシンⅡを不活性化することによって,レニン-アンジオテンシン系を抑制する酵素である.Imaiらは,ACE2が重度の急性肺損傷に対して防御的な役割を担うことを明らかにし,さらにACE2がSARSウイルスのin vivoにおける受容体であることを報告している.これらの知見は,ACE2をはじめとしたレニン-アンジオテンシン系の制御が,ARDSの治療標的となり得ることを示唆するもので,今後の展開が注目される.
(3)肺癌の分子機序
a.肺癌と遺伝子
肺癌発症には,複数の遺伝子異常が契機となることが報告されつつある.細胞の癌化には,癌遺伝子,癌抑制遺伝子,DNA修復酵素遺伝子などが密接にかかわり,その遺伝子異常によって腫瘍発生を誘起することが想定されている.たとえば,癌遺伝子ではK-ras遺伝子変異が,非小細胞肺癌で好発していることが報告されている.一方,癌抑制遺伝子p53は,遺伝子発現制御,DNA修復促進や異常細胞のアポトーシスにかかわり,癌発症の抑制に大きく寄与している.すなわち,p53遺伝子の変異が生じると,DNA傷害が多発・蓄積した異常細胞が増え,癌化につながることが考えられる.また,2007年には非小細胞肺癌においてEML4-ALK融合遺伝子が認められる症例がManoらによって報告され,大きく注目されている.ALK融合遺伝子陽性の非小細胞肺癌に対しては,分子標的薬が開発され臨床現場で使用されている. 肺癌発症にかかわることが知られる代表的な遺伝子異常を表7-1-10にまとめる.
また最近注目されている癌抑制遺伝子として,TSLC1があげられる.非小細胞肺癌では,第11染色体q23領域のヘテロ接合性の消失が高頻度に認められ,癌抑制遺伝子の存在が示唆されてきた.Murakamiらは,ヒト肺癌細胞A549に11q23由来のYACクローンを移入し,腫瘍原性の抑制を指標として新規に癌抑制遺伝子TSLC1を同定した.TSLC1はNCAMと相同性を示す膜蛋白質をコードし,細胞接着に関与すると思われる.その発現はリンパ球以外のあらゆる臓器で認められたが,種々の腫瘍細胞の約半数で欠如している.原発性肺癌でも約40%にTSLC1不活性化が認められている(表7-1-10).
(4)遺伝性呼吸器疾患
a.遺伝子異常による呼吸器疾患
気管支喘息,肺癌などの主要な呼吸器疾患では,従来より発症に遺伝的な要素があることが指摘されている.しかしながら現時点では,これらの疾患は,単一の遺伝子異常ではなく,複数の遺伝子異常の集積により発症することが想定されている. これに対して,単一の責任遺伝子の異常によって発症が説明される呼吸器疾患も報告されている.代表的なものとして,α1アンチトリプシン欠損による若年性COPD(Z型α1アンチトリプシン,Glu342Lysの変異で,欧米白人に比較的多く1~2%の頻度),Hermansky-Pudlak 症候群(HPS1遺伝子異常,プエルトリコでは1800人に1人,肺線維症,アルビニズム,セロイド様物質沈着,血小板機能異常を呈する),囊胞性線維症(cystic fibrosis:CF)などがある. 特に囊胞性線維症の遺伝子発見は,呼吸器疾患のみならず分子生物学のあり方に大きな影響を与えた.囊胞性線維症は,白人において出産の1/2000の頻度で認められる常染色体劣性の遺伝性疾患で,呼吸器感染症(特にバイオフィルムの形成が特徴)や膵外分泌能低下をきたし,予後は不良である.CF遺伝子のキャリアは白人の約5%と推測されている.すでに,Tsuiらによって第7染色体の長腕にCF遺伝子が存在していることが判明していたが,Collinsや Tsuiらのトロント大学研究グループは,このCF遺伝子の同定を目指し,1989年,ついに成功した.CF遺伝子は,約6500 ヌクレオチドよりなり,1480アミノ酸残基のポリペプチドをコードしていた.そしてこのCF遺伝子産生物を,CF transmembrane conductance regulator (CFTR)と命名した.次に,CF患者の遺伝子を検討したところ,多くの患者において,508番目のアミノ酸であるフェニルアラニン(phenylalanine:F)を欠失させる変異が生じていることが発見された.遺伝子の塩基配列では,3塩基が欠失しており,この表現型(ΔF508) がCF患者の病態を生じさせるものと推定された.本研究は,「遺伝子研究」が直接,疾患の原因解明に結びつくことを社会的にも認知させる契機になった.また本研究では,染色体上の予想される部位からCF遺伝子を探し出すという手法が用いられているが,大変な難作業であったという.この後,ヒト染色体のすべての塩基配列を解読するという壮大なプロジェクト,すなわちヒトゲノム解読プロジェクトが開始された.
(5)ポストゲノム時代の呼吸器疾患
a.分子生物学の応用と呼吸器疾患
ヒトに続いてマウスのゲノムが解読され,分子生物学はポストゲノム時代に入った.また,肺癌治療薬ゲフィチニブ,インフルエンザ治療薬オセルタミビルのような分子標的薬は,分子生物学によって同定された分子に対して,コンピューターでのドラッグデザインにより開発された最新科学の結晶である.このような分子生物学の知見は呼吸器疾患にも新たな局面を与えてきている.たとえば1塩基多型(single nucleotide polymorphism:SNP)とよばれる個体差を表すゲノム上の小さな違いについては,最近の知見の集積により呼吸器疾患と関連するものが次第に明らかにされつつある.これらの情報を集学的・統合的に解析することで,肺癌,COPD,肺線維症,気管支喘息のように定義されている疾患群を分子生物学的に細分類し,適切な治療を行うことで死亡率の改善や疾病コントロール状況の好転が期待できるであろう.また,siRNAなど分子生物学上の最新手法の開発・応用などにより,近い将来,呼吸器疾患を対象とする分子標的薬の開発が期待される.[徳田安春・河野修興・酒井文和・村田喜代史・栗本典昭・宮澤輝臣・橋本 修・長瀬隆英]
■文献
Norisue Y, Tokuda Y, et al: Phasic characteristics of inspiratory crackles of bacterial and atypical pneumonia. Postgraduate Medical Journal, 84(994): 432-436, 2008.
Tokuda Y, Miyagi S: Physical diagnosis of chronic obstructive pulmonary disease. Internal Medicine, 46: 1885-1891, 2007.
徳田安春,宮城征四郎:COPDの臨床所見:特集COPDの病態と臨床的特徴:日本臨牀,69: 1770-1774, 2011.
Kohno N, Kyoizumi S, et al: New serum indicator of interstitial pneumonitis activity: sialylated carhydrate antigen KL-6. Chest, 96
:68-73, 1989.大下慎一郎, 河野修興:肺癌の診断 腫瘍マーカー. 外科治療, 93: 391-395, 2005.
Robinson BWS, Creaney J, et al: Soluble mesothelin-related protein-a blood test for mesothelioma. Lung Cancer, 49S1: S109-111, 2005.
Goodman RL: Felson’s Principles of Chest Roentgenology Text with CD-ROM, 3rd ed (Goodman, Felson’s Principles of Chest Roentgenology), Saunders, 2009.
酒井文和:CTから学ぶ胸部単純撮影,克誠堂出版, 東京,2007.
日下部きよ子編:がん診療のためのPET/CT. 金原出版,東京,2006.
村田喜代史: 胸部(呼吸器・縦隔),標準放射線医学,第7版(西谷 弘,他編),pp153-248,医学書院,東京,2011.
村田喜代史,他編: 胸部のCT,第3版,MEDSi, 東京,2011.
Gildea TR, Mazzone PJ, et al: Electromagnetic navigation diagnostic bronchoscopy: a prospective study. Am J Respir Crit Care Med, 174: 982-989, 2006.
Kurimoto N, Murayama M, et al: Assessment of usefulness of endobronchial ultrasonography in determination of depth of tracheobronchial tumor invasion, CHEST, 115: 1500-1506, 1999.
Kurimoto N, Miyazawa T, et al: Endobronchial ultrasonography using a guide sheath increases the ability to diagnose peripheral pulmonary lesions endoscopically. Chest, 126, 959-965, 2004.

表7-1-1

表7-1-2

表7-1-3

表7-1-4

表7-1-5

表7-1-6

表7-1-7

表7-1-8

表7-1-9

表7-1-10
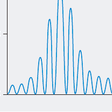
図7-1-1
図7-1-5
図7-1-6
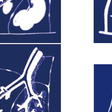
図7-1-16
図7-1-19
図7-1-23
図7-1-24
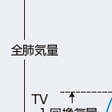
図7-1-25
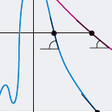
図7-1-26
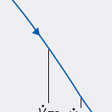
図7-1-27
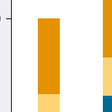
図7-1-28
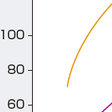
図7-1-29
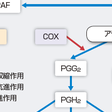
図7-1-30
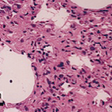
図7-1-31
総論(脱髄疾患)
脱髄疾患は大きく分けて中枢神経系の脱髄疾患と末梢神経系の脱髄疾患(Guillain-Barré症候群など)があるが,この項目では後者は述べない【⇨15-19】.おもな中枢神経系脱髄疾患を分類して表15-9-1に示す.これらの脱髄疾患のなかでも,患者数の多さ,病因解明の難解さ,治療の重要さや社会的な問題性などの観点から,多発性硬化症(multiple sclerosis:MS)がその代表的疾患である.多発性硬化症に類似はしているが,臨床病理学的に特異な視神経脊髄炎(neuromyelitis optica)やBaló病があり,これらは広く多発性硬化症疾患群という疾患スペクトラムに属するものとの考えがある.しかし,別項で述べるように視神経脊髄炎は疾患特異的な血清アクアポリン4抗体が発見され,アストロサイト(星状細胞)の傷害が主要病変との指摘もあり,今後疾患分類が変わる可能性がある.これらの疾患を病変分布と臨床経過によってわかりやすく模式的に示したのが図15-9-2である.[糸山泰人]
■文献
Compston A, et al eds: McAlpine’s Multiple Sclerosis, 4th ed, Churchill Livingstone Elsevier, Philadelphia, 2006.
糸山泰人:変わりつつある疾患の概念-視神経脊髄型多発性硬化症(OSMS)と視神経炎(NMO)-.Annual Review神経,2008: 238-245, 2008.
Misu T, Fujihara K, et al: Loss of aquaporin 4 in lesions of neuromyelitis optica: distinction from multiple sclerosis. Brain, 130: 1224-1234, 2007.
Vinken PJ, Bruyn GW, et al eds: Handbook of Clinical Neurology: Demyelinating Disease 47, Elsevier Science Publishers, Amsterdam, 1985.
総論(薬物中毒・依存症)
中毒(poisoning)という概念は,「毒物(化学物質のなかで生物系に有害反応を引き起こしてその機能を大幅に損傷させ,ときには死を招くことさえあるもの)によって引き起こされる有害な事象」と定義することができる.中毒は急性中毒と慢性中毒に分類されるが,医療の場で緊急の診断・治療を要するのは急性中毒である.厚生労働省人口動態統計によれば,中毒による死亡件数は年間6000~7000件である.起因別頻度をみると,一酸化炭素およびガス類による中毒が全体の約70%を占めており,次に医薬品,農薬と続く.
社会的にはよく用いられる「アルコール中毒」「覚醒剤中毒」という表現は,厳密には「依存症(dependence)」という言葉に置き換えるべきであり,医療従事者は両者を区別して取り扱う必要がある.依存症とは「生体と薬物の相互作用から生ずる精神状態および身体症状で,薬物の精神効果を再び体験したいとか,あるいは薬物の投薬中止によって生ずる苦痛状態を取り除くために,薬物を強迫的に欲求すること」(WHO,1969)と定義され,その状態や程度により,精神依存と身体依存に分類される.麻薬,覚醒剤以外に依存性を有する薬物の多くは向精神薬に分類される.依存症は慢性中毒や薬物乱用(drug abuse)に関連しており,その離脱や社会復帰のためには長期間の治療や支援が必要となる.[福本真理子]
■文献
福本真理子:アセトアミノフェン中毒の治療にノモグラムは有用か.中毒研究,23: 111-115,2010.
上條吉人:臨床中毒学(相馬一亥監修),pp1-38,医学書院,東京,2009.
Kearney TE: Therapeutic Drugs and Antidotes. In : Poisoning & Drug Overdose, 4th ed (Olson KR ed), pp404-509, McGraw-Hill, New York, 2004.
出典 内科学 第10版内科学 第10版について 情報
普及版 字通 「総論」の読み・字形・画数・意味
【総論】そうろん
字通「総」の項目を見る。
出典 平凡社「普及版 字通」普及版 字通について 情報
関連語をあわせて調べる
1 花の咲くのを知らせる風。初春から初夏にかけて吹く風をいう。2 ⇒二十四番花信風...