翻訳|pyridine
精選版 日本国語大辞典 「ピリジン」の意味・読み・例文・類語
ピリジン
日本大百科全書(ニッポニカ) 「ピリジン」の意味・わかりやすい解説
ピリジン
ぴりじん
pyridine
6員環内に窒素原子1個を含む複素環式化合物の代表的なものの一つ。ベンゼンC6H6の一つの炭素原子を窒素で置き換えた構造であるので、ベンゼンと同じように共鳴がおこり、芳香族性をもつことが知られている。
コールタール中に0.2%ぐらい含まれている。ピリジンが塩基性をもっていて酸に溶ける性質を利用して、コールタールを希硫酸と処理して分離していた。
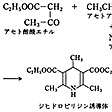
実験室的な合成法としては、ドイツの化学者A・R・ハンチによるピリジン合成が知られている。この合成法では、β(ベータ)-ケトエステルまたはβ-ジケトンをアルデヒドおよびアンモニアと縮合させてピリジン環を構築する()。工業的には、現在は、シリカ‐アルミナ触媒により高温でホルムアルデヒド、アセトアルデヒド、アンモニアを反応させるアルデヒド法、またはアクリルアルデヒドとアンモニアの反応によるアクロレイン法により合成されている。
無色の悪臭をもつ液体。弱い塩基性をもっているので、強酸には塩をつくって溶ける。水、エタノール(エチルアルコール)、エーテルのいずれとも任意の割合で混じり合う。ピリジン環は比較的安定で、付加反応を示さないばかりか、置換反応もおこしにくい。ニトロ化反応に対してはベンゼンよりさらに不活性であり、混酸(硫酸と硝酸の混合物)とは常温では反応せず、高温にすると反応して3-ニトロピリジンを与えるが、収率はよくない。この例でもわかるように、陽イオンによる求電子置換反応は窒素に対してメタの位置におこる。ピリジンを過酸化水素水(オキシドール)で酸化すると、窒素上に酸素がついたピリジン N-オキシドになる。除草剤や医薬品の合成原料、ゴムや塗料関係の溶剤、分析試薬としても使用される()。
ピリジンの同族体であるピコリン、ルチジンなどの塩基もコールタール中に含まれていて、これらを総称してピリジン塩基とよぶ。
[廣田 穰・末沢裕子 2015年7月21日]
改訂新版 世界大百科事典 「ピリジン」の意味・わかりやすい解説
ピリジン
pyridine
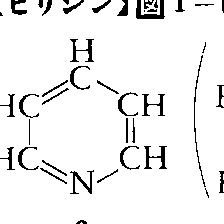
ベンゼンの-CH=単位一つを窒素原子で置換した構造をもつ化合物。イギリスのアンダーソンThomas Andersonは,1846年にコールタールからピリジンの同族体であるピコリン(メチルピリジン)を初めて単離し,その後まもなくピリジンそのものを骨油から単離した。当初その構造が確定せず,図1-bのように書かれていたが,69年イギリスのJ.デュワーによって図1-aの構造をもつことが示された。ベンゼンの場合と同様,炭素,水素を省略して図1-cのように書くのが普通である。図1-dのような書き方はピペリジンと混同しやすいので避けるべきである。ピリジン環に対する置換基の位置番号のつけ方には2通りある。数字を用いるときには窒素を1とし,ギリシア文字を用いるときは窒素に隣接した炭素をαとし,以下図2のように続ける。
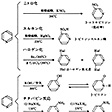
ピリジンは不快な臭気をもつ無色の液体で,融点-41.8℃,沸点115.50℃。水とは自由に混合する。コールタールから得られるほか,その同族体はチチバビンchichibabinのピリジン合成(式1),ハンチHantzschのピリジン合成(式2)などで合成される。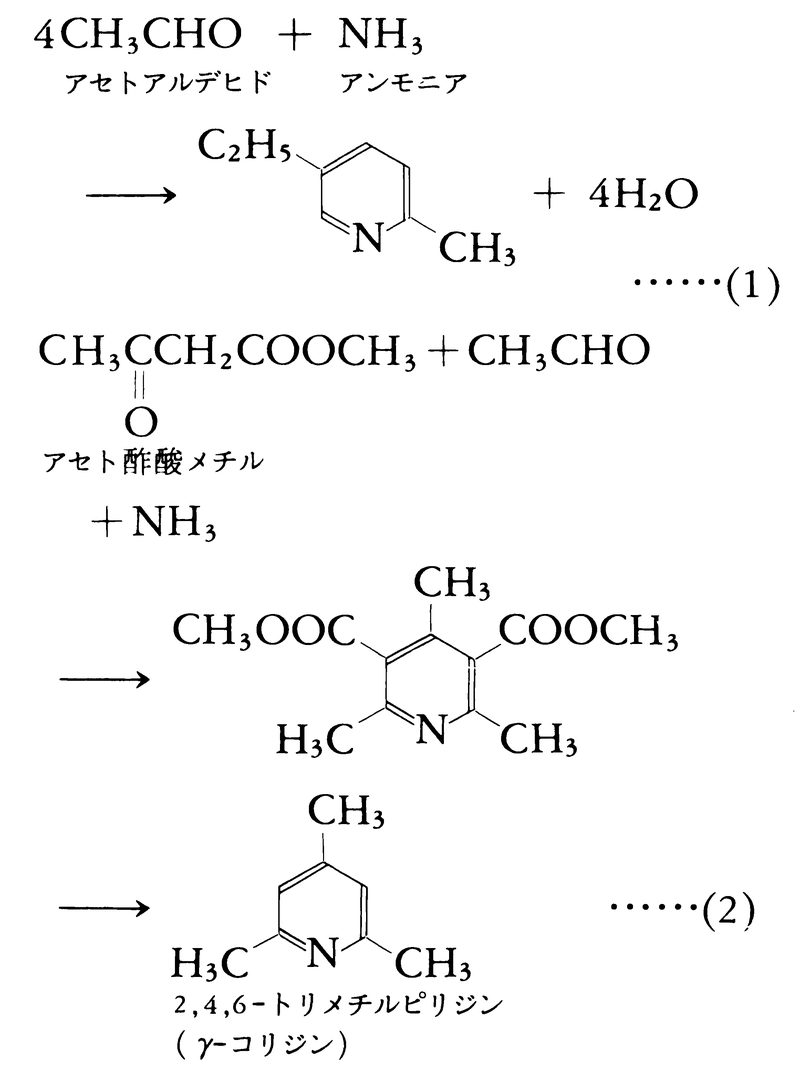
ピリジンは代表的な芳香族複素環式化合物であり,その共鳴安定化は二つのケクレ形限界構造式と三つの双極イオン形限界構造式の寄与によって説明される。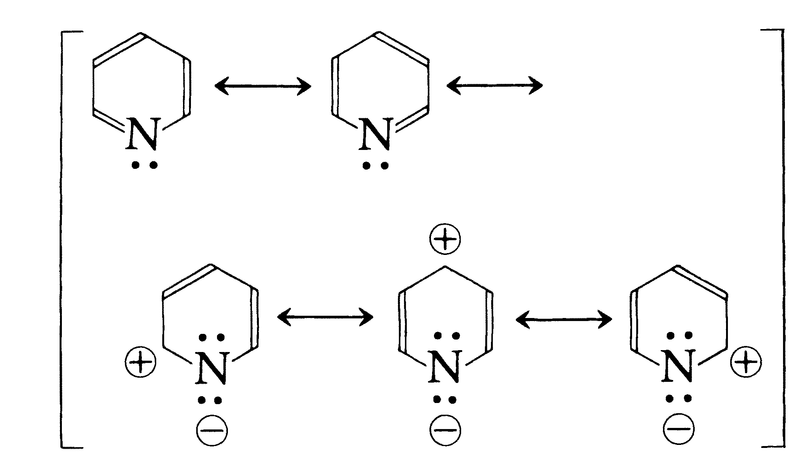
ピリジンは,窒素原子上の非共有電子対のため弱い塩基性を示し,塩をつくるので,強酸が生じる反応において除酸剤として用いられる。また第一ハロゲン化アルキルとの反応によってN-アルキルピリジニウム塩を生じる。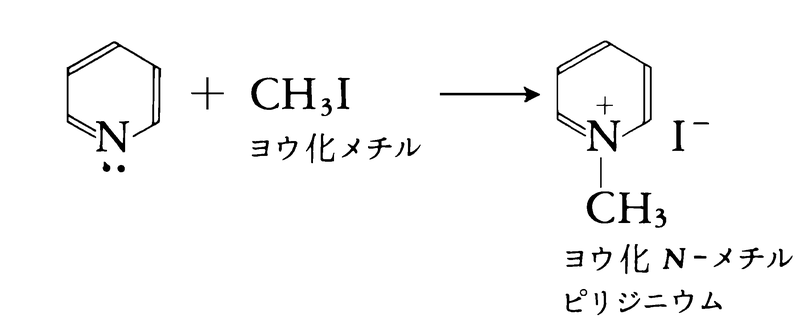
ピリジン自身は求電子置換反応を受けがたく,発煙硝酸を用いても常温ではニトロ化されないが,高温ではニトロ化が起こり3-ニトロピリジンを低収率ながら生じる。ピリジン環にアルキル基,アミノ基が置換すると求電子置換反応が起こりやすくなる。過酸化水素などの過酸化物で酸化するとN-オキシドとなり,いくぶん求電子置換反応が起こりやすくなる。
ピリジンは,塩基性溶剤として化学工業で広く用いられるほか,三酸化クロムなどを用いる酸化反応の溶媒として,有機合成で広く用いられている。
執筆者:竹内 敬人
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「ピリジン」の解説
ピリジン
ピリジン
pyridine
C5H5N(79.10).アザベンゼンともいう.コールタール中に,その多数の同族体とともに,0.2% 前後含まれている.骨油,タバコの煙のなかにも少量含まれる.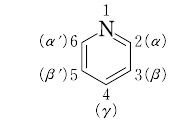 無色,特有の臭いと苦味をもつ液体.融点-42 ℃,沸点115.5 ℃.
無色,特有の臭いと苦味をもつ液体.融点-42 ℃,沸点115.5 ℃.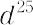 0.9779.
0.9779.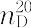 1.5102.きわめて弱い塩基で,強酸と塩をつくる.pKa 5.19(25 ℃,水溶液).吸湿性で水,エタノール,エーテル,そのほかの有機溶媒に易溶,また多くの有機化合物をよく溶かす.芳香族性をもつ安定な化合物で,硝酸や酸化クロム(Ⅵ)によって酸化されない.求電子置換はベンゼンの場合より起こりにくく,非常にはげしい条件でニトロ化,スルホン化,およびハロゲン置換を受ける.置換反応は主として3位(β位)で起こる.過酸化水素または過酸で酸化すればN-オキシドを生じる.ナトリウムアマルガムで還元すると飽和化合物としてピペリジンを生じる.第三級アミンの性質をもち,ハロゲン化アルキル(RX)を作用させるとハロゲン化アルキルピリジニウム[C5H5NR]+ X-を生じるが,それを高温に熱すればアルキル基が2位または4位に転移する.ピリジンは求核置換を受けやすい.たとえば,アルキルリチウムまたはアリールリチウムを作用させると,2位にアルキルまたはアリール置換が起こる.同族体の合成には,ハンチ法やチチバビン法がある.ピリジンは化学工業において,塩基性溶剤として重要である(ゴム,塗料工業).中枢神経を抑制し,皮膚および気管を刺激する.LD50 891 mg/kg(ラット,経口).[CAS 110-86-1]
1.5102.きわめて弱い塩基で,強酸と塩をつくる.pKa 5.19(25 ℃,水溶液).吸湿性で水,エタノール,エーテル,そのほかの有機溶媒に易溶,また多くの有機化合物をよく溶かす.芳香族性をもつ安定な化合物で,硝酸や酸化クロム(Ⅵ)によって酸化されない.求電子置換はベンゼンの場合より起こりにくく,非常にはげしい条件でニトロ化,スルホン化,およびハロゲン置換を受ける.置換反応は主として3位(β位)で起こる.過酸化水素または過酸で酸化すればN-オキシドを生じる.ナトリウムアマルガムで還元すると飽和化合物としてピペリジンを生じる.第三級アミンの性質をもち,ハロゲン化アルキル(RX)を作用させるとハロゲン化アルキルピリジニウム[C5H5NR]+ X-を生じるが,それを高温に熱すればアルキル基が2位または4位に転移する.ピリジンは求核置換を受けやすい.たとえば,アルキルリチウムまたはアリールリチウムを作用させると,2位にアルキルまたはアリール置換が起こる.同族体の合成には,ハンチ法やチチバビン法がある.ピリジンは化学工業において,塩基性溶剤として重要である(ゴム,塗料工業).中枢神経を抑制し,皮膚および気管を刺激する.LD50 891 mg/kg(ラット,経口).[CAS 110-86-1]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「ピリジン」の意味・わかりやすい解説
ピリジン
pyridine
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
百科事典マイペディア 「ピリジン」の意味・わかりやすい解説
ピリジン
出典 株式会社平凡社百科事典マイペディアについて 情報
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...



 )1.50920
)1.50920