ヨウ(沃)素酸 (ようそさん)
iodic acid
化学式HIO3。ヨウ素およびヨウ化物イオンを酸化する際につねに見いだされる5価のヨウ素の化合物で,1813年にJ.L.ゲイ・リュサックとH.デービーが同時に発見した。五酸化二ヨウ素I2O5を水に溶かすか,ヨウ素を25%程度の濃厚な過塩素酸あるいは発煙硝酸と加熱したり,または塩素水で酸化して得られる。ヨウ素酸バリウムと硫酸の複分解によっても得られる。特異の臭気を有する無色の結晶で,吸湿性はない。固体のヨウ素酸の生成熱は237.5kJ/molとかなり大きく,比較的安定な物質である。α形とβ形の2種があり,ともに斜方晶系で,β形のほうがα形より結晶軸の軸比が大きい。IO3⁻は三角錐構造をとり,I-O結合距離は1.80~1.89Å,∠O-I-O結合角は96°40′~101°25′。加熱すると70℃で水の一部を失って3I2O5・H2O(HI3O8に相当する)に変化し,さらに,200℃で完全に脱水してI2O5となる。水溶液は無色で,-14℃が氷とHIO3との氷晶点。この点では72.8gのHIO3が100gの溶液中に溶解している。エチルアルコールに微溶,エーテルには不溶。水溶液はやや強い酸で,解離定数K=0.156dm3/mol(25℃)。濃厚な溶液中では(HIO3)n(n=2~3)として存在するという報告もある。強い酸化力があり,光により徐々に分解され,酸素を放ってヨウ化物となるのである。硫黄は封管中でヨウ素酸水溶液と加熱すれば硫酸となり,赤リン,黄リンはともに激しく反応して,ホスホン酸を生じヨウ素を遊離する。多くの金属と反応するが,スズ,鉛,白金とは反応しない。塩酸は塩素を発生しヨウ素を遊離するが,同時に一塩化ヨウ素を生ずる。ヨウ化水素酸とヨウ素酸とは,反応してヨウ素を遊離する。
HIO3+5HI─→3I2+3H2O
過酸化水素との反応ではヨウ素を遊離するが,そのヨウ素は再び過剰の過酸化水素と反応してヨウ素酸となる。亜硫酸とは複雑な反応機構を通って硫酸にまで酸化する。硝酸酸性水溶液中で水銀(Ⅱ)と鉛の分析試薬に用いられる。
ヨウ素酸塩MIIO3には多くのものが知られている。一般に無色の結晶。1価の金属塩のうちナトリウム塩NaIO3は5水和物で,他は無水和物,2価の塩は水銀塩が無水和物で,他は1~4水和物として得られる。塩素酸塩,臭素酸塩より安定であるが,炭素あるいは有機物を混ぜて熱すると爆発する。ヨウ素酸カリウムは分析用試薬として重要である。
執筆者:大瀧 仁志
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
Sponserd by 
ヨウ素酸
ようそさん
iodic acid
ヨウ素のオキソ酸の一つ。ヨウ素を発煙硝酸または塩素酸水溶液と加温してつくる。あるいは五酸化二ヨウ素I2O5を水に溶かしてつくる。特異臭のある無色の結晶。加熱すると、約70℃から脱水が始まり、110℃で融解してHI3O8(比重4.734)となり、220℃で五酸化二ヨウ素I2O5になる。光で徐々に分解する。吸湿性はない。水100グラムに310グラム溶ける(16℃)。水溶液は酸性で、強い酸化剤である。ヨウ素酸塩MIIO3は、アルカリ金属やアルカリ土類金属の水酸化物溶液にヨウ素を加えて熱するか、塩素酸塩水溶液にヨウ素を反応させてつくる。一価金属塩はナトリウム塩(五水和物)のほかは無水塩で、二価金属塩には無水塩、一水和物、二水和物、四水和物がある。塩素酸塩や臭素酸塩より安定であるが、酸化力が強く、炭素、有機物と混ぜて熱すると爆発する。ヨウ化水素を酸化してヨウ素と水にする。
HIO3+5HI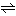 3I2+3H2O
3I2+3H2O
水溶液は硝酸銀、塩化バリウム、酢酸鉛で無色の沈殿を生じる。ヨウ素酸カリウムKIO3の標準液を用いる酸化滴定はヨウ素酸塩滴定とよばれ、ヨウ化物、亜ヒ酸塩、タリウム(Ⅰ)塩、ヒドラジンなどの定量に用いられる。
ヨウ素のオキソ酸にはその他、過ヨウ素酸、オルト過ヨウ素酸、次亜ヨウ素酸などがある。オルト過ヨウ素酸は化学式H5IO6。オルト過ヨウ素酸バリウムBa3H4(IO6)2の水溶液に濃硝酸を加えてつくる。無色の単斜晶系の結晶。潮解性。水、エタノール(エチルアルコール)によく溶け、水100グラムに112グラム(25℃)溶ける。五塩基酸であるが強酸ではない。熱すると約132℃で融解し、水を失って過ヨウ素酸HIO4となる。過ヨウ素酸はメタ過ヨウ素酸ともよばれ、無色の固体。吸湿性。熱すると110℃で昇華し、138℃でI2O5となる。過ヨウ素酸塩には、オルト酸塩MI5IO6、メタ酸塩MIIO4のほか二メソ酸塩MI4I2O9、メソ酸塩MI3IO5、二オルト酸塩MI8I2O11など複雑な組成のものが多い。ヨウ素酸塩のアルカリ性溶液を、塩素または電解により酸化してつくる。一般にオルト酸塩がメタ酸塩より安定である。
次亜ヨウ素酸HIOは水溶液としてのみ存在する。ヨウ素の水溶液を酸化水銀(Ⅱ)と振って得られる。弱酸。次亜ヨウ素酸塩は遊離の酸よりやや安定であるが、水溶液としてだけ知られ、酸化力、漂白作用が強い。
[守永健一・中原勝儼]
出典 小学館 日本大百科全書(ニッポニカ)日本大百科全書(ニッポニカ)について 情報 | 凡例
Sponserd by 
ヨウ素酸
ヨウソサン
iodic acid
HIO3.ヨウ素のオキソ酸には,IⅠのモノオキソヨウ素(Ⅰ)酸 HIO,IⅤのヨウ素酸HIO3,IⅦの過ヨウ素酸HIO4,およびオルト過ヨウ素酸や各種イソポリ酸などがあるが,単にヨウ素酸といった場合には,IUPAC,学術用語ともに,HIO3に限定される.HIⅤ O3(175.91)はI2O5と水との反応や,I2 を発煙硝酸などと加熱酸化,濃縮して沈殿させるか,Ba(IO3)2とH2SO4との反応から得られる.α,β形の二変態がある.分解点110 ℃.70 ℃ で水を失って,HI3O3になり,200 ℃ でI2O5になる.水に易溶だが,潮解性はない.エタノールに微溶,エーテルに不溶.強い酸(Ka 約0.169(25 ℃))で,強い酸化力をもつ.医療用(収れん剤,殺菌消毒剤など),分析試薬に用いられる.[CAS 7782-68-5:HIO3]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
Sponserd by 
ヨウ素酸
ヨウそさん
iodic acid
化学式 HIO3 。五酸化二ヨウ素を水で溶解するか,ヨウ素を硝酸,過塩素酸または過酸化水素によって酸化すると得られる無色の斜方晶系結晶。光に当ると黒変する。比重 4.63,融点 110℃ (分解) 。吸湿性はないが水に易溶。熱によって分解し,アンヒドロヨウ素酸 HIO3・I2O5 となるが,この変化は 70℃で始り,220℃で完全となる。この酸は安定で,消毒剤,収斂剤などとして使用される。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
Sponserd by 
世界大百科事典(旧版)内のヨウ素酸の言及
【ヨウ素(沃素)】より
…気体が紫色を呈することから,ギリシア語のiōdēs(すみれ色)にちなんで命名された。天然には,海藻,海産動物中におもに有機化合物として存在するほか,チリ硝石中にヨウ素酸塩として含まれる。脊椎動物の甲状腺にチロキシンとして存在し,生理学的に重要な役割を果たしている。…
※「ヨウ素酸」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
Sponserd by 


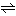 3I2+3H2O
3I2+3H2O