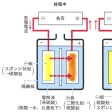
精選版 日本国語大辞典 「鉛蓄電池」の意味・読み・例文・類語
なまり‐ちくでんち【鉛蓄電池】
日本大百科全書(ニッポニカ) 「鉛蓄電池」の意味・わかりやすい解説
鉛蓄電池
なまりちくでんち
lead acid battery
lead storage battery
lead accumulator
正極活物質に多孔性二酸化鉛PbO2、負極活物質にスポンジ状鉛Pb、電解液には33~37%程度の硫酸H2SO4水溶液を用いる代表的な蓄電池。1859年にフランスのプランテRaimond Louis Gaston Planté(1834―1889)により発明され、多くの改良が加えられてきた長い歴史をもつ。
鉛蓄電池が放電すると、正極では
PbO2+SO42-+4H3O++2e-
―→PbSO4+6H2O
また負極では
Pb+SO42-―→PbSO4+2e-
の反応が進み、鉛蓄電池全体では
PbO2+Pb+2SO42-+4H3O+
―→2PbSO4+6H2O
で示される。充電反応はこれらの逆である。起電力は硫酸濃度が濃いほど大きくなるが、通常の濃度では約2.1ボルトで、水溶液を電解液とする蓄電池のなかではもっとも高い。また公称電圧は2.0ボルトで、出力密度は300W/kg前後、エネルギー密度は30~40Wh/kgである。両極ともに電解液の硫酸と反応するので、放電電気量に比例して硫酸濃度(比重)が低下し、充電時に上昇する。したがって硫酸濃度(比重)から充放電状態を知ることができる。
ペースト式極板を用いる方式では、集電体を兼ねる極板の格子グリッド材料に、通常2~6%のアンチモンを含む鉛合金が用いられている。また鉛カルシウム合金シートに切れ目を入れて引き延ばし、格子状とするエキスパンド格子が実用化されている。これらの格子グリッドにペースト状二酸化鉛粉末あるいはペースト状鉛粉末を充填(じゅうてん)してそれぞれ正極または負極とする。そして表面にガラスマットを当てて活物質の脱落を防ぎ、硫酸電解液中で隔離板を介して正極と負極を対置する。このような構造の単電池を数個、並列あるいは直列に接続して、合成樹脂製の電槽に収納する。正極にクラッド式(チューブ式)極板を用いる場合には、ガラス繊維製の多孔性チューブに鉛合金芯金を挿入し、その空隙(くうげき)に活物質の二酸化鉛ペーストを充填して枠体に配列する。構造的に二酸化鉛が脱落しにくく耐久性に優れているため、充放電サイクル寿命を長くすることができる。負極にはつねにペースト式が用いられるが、充放電を繰り返すとスポンジ状鉛が収縮・緻密(ちみつ)化して容量が低下するので、それを防止するためにリグニン系物質や硫酸バリウムなどの防縮剤が少量添加されている。
鉛蓄電池は、漏液による周辺機器の腐食を避けるために密封構造とし、ベント形では充電時の酸霧の逸散や水の消耗を抑える目的で蓄電池の上部に排気栓が設けられている。またシール形(密閉形)では充電時に正極から発生する酸素を負極で反応吸収させ、負極を化学的に放電状態として水素の発生を抑え、補水を必要としない機能をもたせる。さらに定められた内圧を超えると作動する安全弁(制御弁)を備えていて、メンテナンスフリーとなっている。また触媒栓式シール形では、触媒と防爆フィルターにより充電時に発生する水素と酸素を反応させて水に戻すとともに、酸霧の放散や外部火種による内部可燃ガスの引火爆発を防ぐようくふうされている。自動車始動用鉛蓄電池では、70℃を越えるような厳しい環境下での信頼性が技術的に未熟であるため、現状ではシール形は普及していないが、将来的にはシール形になるものと考えられる。
2002年(平成14)における日本の鉛蓄電池の生産シェアは蓄電池総生産額の28%で、やや増加の傾向にある。高出力で移動可能であり、安定した品質、高い信頼性や経済性を有する鉛蓄電池が自動車のエンジン始動用やフォークリフトなどの動力用電源に用いられているほか、据置用が非常用電源、予備電源、電力貯蔵用、太陽電池発電システム用などに、また小容量の小形シール鉛蓄電池が、二輪自動車用や無停電電源装置など多方面で使用されており、そのうち自動車始動用が62%を占める。
[浅野 満]
『高村勉・佐藤祐一著『ユーザーのための電池読本』(1988・コロナ社)』▽『池田宏之助著『電池の進化とエレクトロニクス――薄く・小さく・高性能』(1992・工業調査会)』▽『池田宏之助編著、武島源二・梅尾良之著『「図解」電池のはなし』(1996・日本実業出版社)』▽『小久見善八監修『最新二次電池材料の技術』普及版(1999・シーエムシー)』▽『日本電池株式会社編『最新実用二次電池 その選び方と使い方』(1999・日刊工業新聞社)』▽『小久見善八編著『電気化学』(2000・オーム社)』
改訂新版 世界大百科事典 「鉛蓄電池」の意味・わかりやすい解説
鉛蓄電池 (なまりちくでんち)
lead accumulator
lead storage battery
最も広く実用に供されている二次電池で,陽極活物質は二酸化鉛PbO2,陰極活物質は鉛Pb,電解液は比重1.2の希硫酸H2SO4で構成される。1860年フランスのプランテG.Plantéの考案によるもので,実用化できるよう改造されたのは1879年である。100年余の歴史をもつが,新素材の開発により,コンパクト化,高性能化,保守の簡素化が図られている。充放電の反応は,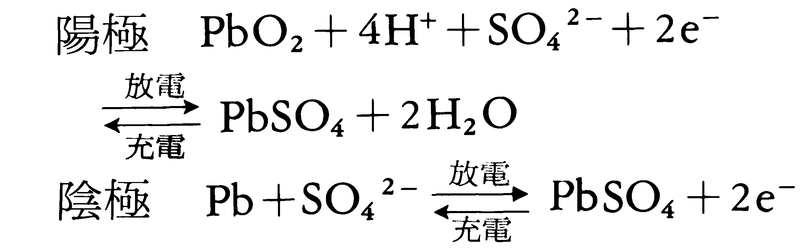
で,全反応は次式にまとめられる。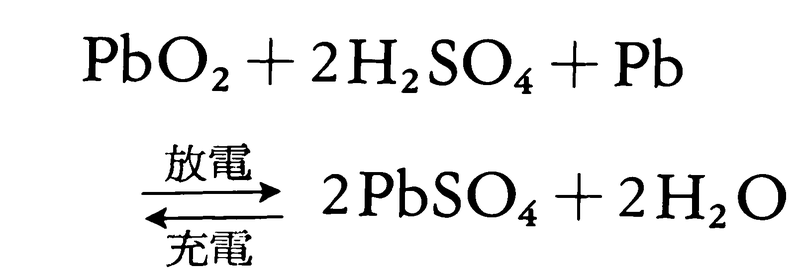
起電力は常温で比重1.2の希硫酸で約2.05Vである。この式からわかるように,放電とともに硫酸濃度は低下する。放電しすぎたり,充電しないで放置しておくと,電気不導体の硫酸鉛PbSO4の大結晶が極板上に析出して,充電不可能となる。この現象をサルフェーションsulfationという。充放電を繰り返しながら使用する注意が必要である。
鉛蓄電池の極板にはペースト式とクラッド式の二つがある。ペースト式極板は,活物質の微粉を希硫酸で練ってつくったペーストを,硬鉛の格子に塗りこんで乾燥した後,化成(電解酸化あるいは還元)と呼ぶ処理によって活物質をPbあるいはPbO2の形に仕上げたもので,軽量小型で大きな容量が得られ,高率放電特性にすぐれていて,陽極板,陰極板の両方に用いられる。クラッド式極板は,ガラス繊維あるいは合成繊維を編んでつくったチューブの中に鉛合金の芯金を入れ,すき間を活物質で充てんしたものを多数並列して,化成してつくられる。クラッド式極板は,じょうぶで深い充放電に対し長寿命であり,陽極板としてだけ用いられる。電池は陽極板と陰極板の間にガラス繊維製あるいは合成樹脂製のセパレーターを挟んで多数重ね,合成樹脂製の容器に入れてつくられる。自動車や船舶などのエンジン始動用電源や非常時の電源などに多用されており,さらに電気自動車駆動源や電力貯蔵用電池などへの改良が進められている。小型密閉式のものも携帯用として実用化されている。
執筆者:笛木 和雄
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「鉛蓄電池」の解説
鉛蓄電池
ナマリチクデンチ
lead acid battery
負極にはPb,正極活物質にPbO2を用い,電解質として硫酸を使用する蓄電池.1859年,フランスのR. Plantéにより発明された.その後,あらたな蓄電池が開発されたが,製造コストが安く,高電流に対しても耐えるため,依然として鉛蓄電池は車その他に用いられている.電池反応は,
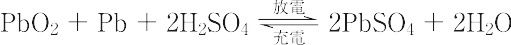
で,放電により両極活物質は,ともにPbSO4に変化する.硫酸は比重約1.25のものを使用するが,放電により消費され,約1.10に低下する.電極活物質は通常ペースト状に練って,格子形の硬鉛極板に充填して使用する.とくに正極活物資は充・放電による体積変化がいちじるしく,活物質が脱落しやすい.また,充・放電の繰り返しによりPbSO4が結晶化(sulfation)し,利用率の低下が起こる.公称電圧は2 V である.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「鉛蓄電池」の意味・わかりやすい解説
鉛蓄電池【なまりちくでんち】
→関連項目電気自動車
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「鉛蓄電池」の意味・わかりやすい解説
鉛蓄電池
なまりちくでんち
lead acid battery
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...