精選版 日本国語大辞典 「水素電極」の意味・読み・例文・類語
すいそ‐でんきょく【水素電極】
化学辞典 第2版 「水素電極」の解説
水素電極
スイソデンキョク
hydrogen electrode
2H+ + 2e- = H2
の電極反応の可逆電極電位を安定に示す電極.通常,H+ 濃度の高い溶液に白金黒付き白金電極を浸し,H2 ガスを通じて飽和させたもので,その可逆電位Eは次式で表される.
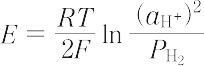
ここで,aH+ は H+ の活量,Fはファラデー定数,Rは気体定数,Tは絶対温度,PH2 は水素分圧である.とくに
PH2 = 1 atm,aH+ = 1
(通常,1.18 mol L-1 のHCl溶液が用いられる)の水素電極は標準水素電極とよばれ,規約により電位0の基準となっている.水素電極電位は電極金属の種類には無関係であるが,実際には水素電極電位より貴な電位をもち,しかも水素過電圧の小さい金属でないと安定な電位は得られない.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
日本大百科全書(ニッポニカ) 「水素電極」の意味・わかりやすい解説
水素電極
すいそでんきょく
hydrogen electrode
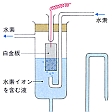
基準電極の一つで、白金電極の下半分を一定濃度の酸に浸し、上半分を水素の気体に接触させてつくったもの。普通、ガラス容器に水素イオンを含む液を入れ、この中によく白金黒(白金の黒色粉末)をつけた白金板を半分挿入し、容器の下部から水素ガスを送って液中に泡として出てくるようにする。このとき水素の圧力をPH2とすると、水素は解離して白金上に吸着し、この吸着水素原子は液中の水素イオン(活動度aH+)と白金の触媒作用により速やかに平衡となる。つまり、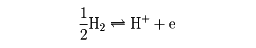
の平衡が成り立ち、25℃でその電位Eは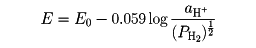
となる。PH2=1(気圧),aH+=1としたときを標準水素電極standard hydrogen electrodeといい、その電位EすなわちE0は温度に無関係に0ボルトと約束する。
[戸田源治郎]
改訂新版 世界大百科事典 「水素電極」の意味・わかりやすい解説
水素電極 (すいそでんきょく)
hydrogen electrode
気体電極の一種で,水素イオンを含む溶液中に,化学的に不活性な電極を挿入し,その表面に水素ガスを通気・接触させた電極系。原理的には図のような構造で,不活性電極としては,2H⁺+2e⁻⇄H2の電極反応(e⁻は電子を表す)が円滑に進行するようなもの(たとえば,白金黒をめっきした白金)を用いる。この電極の平衡電極電位は,溶液のpHや,通気する水素ガスの分圧の関数である。とくに,溶液中の水素イオンの活量が1で,通気する水素ガスの分圧が1気圧のときの水素電極を標準水素電極standard hydrogen electrodeという。これは最も標準的な基準電極として使われており,その平衡電極電位を,便宜上,すべての温度でゼロと仮定することが多い。標準水素電極を基準として測った他の電極の電極電位を,水素電極尺度hydrogen scaleによる値という。
→気体電極
執筆者:玉虫 伶太
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
ブリタニカ国際大百科事典 小項目事典 「水素電極」の意味・わかりやすい解説
水素電極
すいそでんきょく
hydrogen electrode
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「水素電極」の解説
水素電極
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...