共同通信ニュース用語解説 「ヒ素」の解説
ヒ素
有害で、特に化合物は毒性の強いものが多い。毒劇物取締法で毒物に指定されている。地上に広く存在し、木材防腐剤や殺虫剤、半導体製造などに使用される。人体への急性症状は吐き気や下痢などで、ショック症状から死に至ることもある。
更新日:
出典 共同通信社 共同通信ニュース用語解説共同通信ニュース用語解説について 情報
翻訳|arsenic
有害で、特に化合物は毒性の強いものが多い。毒劇物取締法で毒物に指定されている。地上に広く存在し、木材防腐剤や殺虫剤、半導体製造などに使用される。人体への急性症状は吐き気や下痢などで、ショック症状から死に至ることもある。
更新日:
出典 共同通信社 共同通信ニュース用語解説共同通信ニュース用語解説について 情報
周期表第ⅤB族,窒素族に属する元素。かなり古くから知られていた元素で,前4世紀ころすでにアリストテレスが顔料に用いられた雄黄As2S3について記載している。化合物,単体ともに錬金術者に興味がもたれ,とくに銅をヒ素の硫化物(雄黄)で処理すると白色で一見銀のようにすることができることから,金属変換の要素として重要視された。また,ギリシア時代にすでに治療薬として使われた記録もあり,一般には毒薬として広く使われた。
ヒ素は遊離状態でも産するが,大部分は硫化物として広く存在する。雄黄,鶏冠石,硫ヒ鉄鉱,硫ヒ銅鉱等である。銅,鉛,亜鉛,スズなどの硫化鉱石に伴って産することが多い。したがって,これらの硫化鉱から得る金属中にヒ素が不純物として混入してくるのが普通である。単斜ヒ素鉱,金属ヒ化物(FeAs2,CoAs2,NiAs2)としても存在している。
昇華性で,2種あるいは3種の変態が知られている。ヒ素蒸気から360℃以上で析出させると,安定形の灰色金属光沢をもつ金属ヒ素(灰色ヒ素,α-ヒ素)が得られる。三方晶系,菱面体の結晶。比重5.73。融点817℃(28気圧)。615℃で昇華する。室温では空気中で安定である。400℃に熱すると白い炎をあげて燃え三酸化二ヒ素As2O3を生ずる。水に不溶。塩酸には侵されないが,濃硝酸あるいは温かい希硝酸には酸化され亜ヒ酸H3AsO3,ヒ酸H3AsO4を生ずる。熱すると多くの金属と反応してヒ化物を生ずる。金属性が最も大きく,導電性を示す。ヒ素蒸気を液体窒素などで急冷すると黄色ヒ素(γ-ヒ素)が得られる。立方晶系。比重2.0。非常に揮発しやすく,手であたためても昇華するくらいである。二硫化炭素に溶けてAs4に相当する分子量を示す。室温で日光照射すると,すぐに灰色ヒ素(α-ヒ素)に転移する。ヒ素蒸気を300℃以下で蒸着するとガラス質の黒色ヒ素(β-ヒ素)を生ずるという。これは少量のヒ素を検出するためのマーシュテストと呼ばれる水素化ヒ素AsH3(アルシン)の熱分解によりガラス管内面に生ずるヒ素鏡と同じもので,その詳細についてはまだよくわかっていない。ガス状態では四面体の4頂点をヒ素原子が占めるAs4分子であり(原子間距離2.44Å),800℃以上ではAs2に解離する。
工業的には,硫化鉱石や銅などの製錬の際に発生するヒ素酸化物が濃縮して含まれている煙灰を,焙焼(ばいしよう)して粗製のAs2O3として得ている。これをさらに昇華精製すると純度99%程度のAs2O3となるので,炭素で還元蒸留を行い金属ヒ素(99.5~99.9%)とする。高純度ヒ素(99.9999%)は主としてAs2O3からつくられる。As2O3を塩酸に溶かし,濃硫酸で脱水,蒸留して塩化ヒ素AsCl3とし,精製したのち加水分解して再びAs2O3として乾燥,800℃で水素による還元で単体ヒ素をつくる。これをさらに水素気流中で昇華精製したり,気相ゾーンメルティングによって精製する。
As2O3としてガラスの脱泡,消泡剤,触媒,農薬などに用いられる。またAs2O3は古来種々の形で医薬品に用いられ,秦佐八郎らが606号の名で開発したサルバルサンもこの製剤であった。現在でもAs2O3は薬局方に所収され,歯髄失活薬などにされる。合金材料として,鉛-アンチモン系合金に硬さを増すために少量添加したり,耐熱性向上のために銅に添加される場合もある。高純度ヒ素がつくられるようになってから,化合物半導体としての用途が開けつつある。シリコンに代わるものとしてIC基板に用いることが有望視されている。またオプトエレクトロニクスの分野でも多方面に使用されている。たとえばガリウムヒ素光電極面は近赤外領域の光に対して最も高能率に光電子を放出するので,光電子増倍管などに多く用いられている。インジウム,ガリウム,リン,アルミニウム,ヒ素などからつくられる半導体を用いた発光ダイオード(LED)は,電子機器の信号灯や光ファイバーを用いた比較的短距離の光通信システムに用途を広げている。
執筆者:漆山 秋雄+後藤 佐吉
ヒ素化合物には有毒なものが多く,古くから殺鼠剤や毒薬として用いられた。水素化ヒ素は猛毒であり,三酸化二ヒ素,塩化物などがこれに次ぐ。しかし金属ヒ素やガラスに含まれる三酸化二ヒ素は水に溶解しないので,毒性は弱い。これらヒ素化合物は消化管や気道,皮膚を通して吸収され,主として尿中に,また大便や毛髪,脱落する皮膚を通して排出される。吸収されたヒ素化合物は肝臓,腎臓,消化管,脾臓,皮膚,骨などにとり込まれる。原形質毒で,とり込まれた局所で組織の壊死を起こし,種々の中毒症状を現す。ヒ素中毒には急性中毒と慢性中毒があり,前者では胃痛,嘔吐,下痢,腎臓障害による無尿症,皮膚炎,粘膜の炎症などが現れ,重症では,循環障害や痙攣(けいれん),麻痺などで死ぬ。後者では,皮膚の色素沈着,つめ,毛髪の欠損,皮膚癌,多発性神経炎,貧血,肝臓障害などがみられる。
ヒ素を含む粉塵に暴露されたヒ素鉱山やヒ素化合物の製造工場などの作業者にヒ素中毒症が発生し,ヒ素まけ,亜ヒまけなどと呼ばれる皮膚炎を起こし,黒皮症,ボーエン病,皮膚癌,肺癌などが発症する。〈亜ヒ焼き〉と呼ばれる亜ヒ酸(三酸化二ヒ素)製造所の排煙,排水が周辺の環境を汚染し,作業者や住民に慢性ヒ素中毒症を起こした事例として,宮崎県土呂久鉱害や島根県笹ヶ谷鉱害が知られている。また,ヒ素化合物製造工場の排水によって汚染した井戸水によって住民にヒ素中毒が発生した事例もある。1955年,西日本一帯の乳児にヒ素中毒が多発し,患児約1万2000人,うち死亡131人の大惨事となった森永ヒ素ミルク中毒事件は,粉乳に安定剤として入れた第二リン酸ソーダ(リン酸水素二ナトリウム)に含まれていた不純物のヒ素が原因であった。本事件は大きな社会的反響を呼び,〈食品衛生法〉改正の契機となった。〈水質汚濁防止法〉によりヒ素の環境基準は0.01mg/l以下,排出基準は0.1mg/l以下と定められている。
執筆者:中島 泰知
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
周期表第15族に属し、窒素族元素の一つ。ヒ素の化合物は洋の東西を問わず古くから知られ、天然に産出する鶏冠(けいかん)石や雄黄(ゆうおう)(石黄(せきおう))については紀元前400年ころまでに、その薬理作用などがアリストテレスによって記載されているが、ヒ素が単体として遊離されたのは13世紀の神学者アルベルトゥス・マグヌスによる。錬金術の盛んな16世紀にはヒ素がいろいろな金属と結合し、銅に塗ると銀のようにみえることなどから、金属変換の重要な要素と考えられた。名称はギリシア語の雄黄arsenikonに由来する。日本語では江戸時代の蘭学者である宇田川榕庵(ようあん)の『舎密開宗(せいみかいそう)』に「亜爾攝尼究母(アルセニキユム)、砒(ひ)」と記されている。砒は砒石、砒霜(酸化ヒ素)からきたものである。明治以降は砒素が用いられている。
[守永健一・中原勝儼]
天然に遊離して産出することもあるが、雄黄(石黄)As2S3、鶏冠石As4S4、硫砒(りゅうひ)鉄鉱FeAsSなど、おもに硫化鉱物として存在する。そのほかにヒ華、単斜ヒ華などの酸化物やヒ化物などの鉱物が知られる。銅または鉛の製錬に際し副産物として得られる。硫化鉱を焙焼(ばいしょう)して三酸化二ヒ素As2O3とし、加熱昇華させて精製したのち、木炭で還元すると金属を得る。純度の高いものは、いったん塩化ヒ素とし、これを蒸留して精製してから、水素で還元してつくったヒ素を温度勾配(こうばい)をつけて電気炉中で昇華精製する。純度99.99999%以上のものが得られる。
[守永健一・中原勝儼]
灰色ヒ素、黄色ヒ素(立方晶系、比重1.97)および黒色ヒ素(無定形、比重4.73)の3変態が知られる。四面体形四原子分子As4を含む黄色ヒ素はヒ素の蒸気を急冷してつくられる。しかし、すぐに金属光沢をもつ普通のヒ素すなわち灰色ヒ素または金属ヒ素とよばれる安定形に変わる。黄色ヒ素の構造は白リンと同じで、金属ヒ素は黒リンに似た構造をもち、いくらか導電性がある。空気中で熱すると三酸化二ヒ素を生じ、ハロゲンとも容易に反応する。濃硫酸・硝酸に溶けて亜ヒ酸、濃硝酸に溶けてヒ酸となる。酸素があると塩酸にも溶けて塩化ヒ素(Ⅲ)をつくる。アルシン(ヒ化水素)AsH3を熱分解すると黒色ヒ素を生じる。
[守永健一・中原勝儼]
合金添加剤に用いられる。銅に少量加えると耐熱性を増し、鉛に加えると硬さを増すなどの特徴をもち、主として鉛‐アンチモン系の軸受合金などに添加される。最近は高純度ヒ素の用途が開けつつある。ヒ化ガリウムGaAs、ヒ化インジウムInAsなどの化合物半導体として、また半導体への添加剤として用いる。とくにGaAsは赤色あるいは赤外発光ダイオード、マイクロ波素子、集積回路、半導体レーザー、太陽電池などに用いられる。ヒ素の硫化物、高純度ヒ素の単結晶は赤外線をよく通すので赤外線写真用レンズ、フィルターなどに用いられる。
[守永健一・中原勝儼]
単体ヒ素には毒性がない(あるいは弱い)と考えられているが、ヒ素の化合物は有毒で農薬用に使われるが、生物への蓄積を恐れて他のものに置き換えられつつある。三酸化二ヒ素はガラスの透明度をあげたり脱色したりする目的で少量添加される。ヒ素化合物には強い毒性をもつものが多い。
[守永健一・中原勝儼]
ヒ素(灰色ヒ素)
元素記号 As
原子番号 33
原子量 74.9216
融点 817℃(28気圧)
沸点 ―
比重 5.73
結晶系 三方
昇華点 613℃
元素存在度 宇宙 7.2(第36位)
(Si106個当りの原子数)
地殻 1.8ppm(第51位)
海水 3.7μg/dm3
As.原子番号33の元素.電子配置[Ar]3d104s24p3の周期表15族非金属元素.原子量74.92160(2).安定核種が質量数75の同位体のみの単核種元素.ほかに60~92の放射性同位体がある.紀元前から硫化物などとして知られており,単体は13世紀の錬金術師Albertus Magnusがヒ素鉱物中に金属が含まれていることを認めていたが,1649年にJ. Schröderが酸化物を木炭で還元して,単体の分離にはじめて成功した.硫化物鉱物石黄の黄金色を表すアラビア語al-zarnikhがギリシアに入ってαρσενικον(arsenikon)となり,さらにラテン語名arsenicumにかわって,現在の英語の元素名arsenicとなった.宇田川榕菴は天保8年(1837年)に出版した「舎密開宗」で,亜爾攝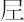 究母(アルセニキュム)砒としている.
究母(アルセニキュム)砒としている.
天然には,単体はまれに産出されるが,鶏冠石AsS,石黄As2S3,硫ヒ鉄鉱FeAsSなどが代表的な鉱物で,自然界に広く分布している.地殻中の存在度1.0 ppm.いん石(コンドライト)中にも ppm けたで存在する.非鉄金属製造で硫化鉱を処理するときに生じる煙灰中から回収し,加熱昇華で分離し,炭素で還元する.3種の同素体がある.室温で安定な灰色の金属ヒ素(α相)は三方晶系で,黒リンと同様の層状構造をしている.密度5.78 g cm-3(20 ℃).第一イオン化エネルギー946.5 kJ mol-1(9.81 eV).六配位の AsⅢおよび AsⅤのイオン半径はそれぞれ0.058,0.046 nm.加熱すると616 ℃ で昇華する.蒸気組成は四面体型 As4 で,急冷すると蒸気は凝縮して,密度4.70 g cm-3(20 ℃),六方晶系の黄色ヒ素になるが,不安定で,光や放置,加熱で灰色の金属性ヒ素にかわる.転移の中間形が無定形の黒色ヒ素(β相)で,密度は4.6~5.2 g cm-3.ヒ素は酸化数3,5で化合物をつくる.水,希酸,アルカリ溶液には不溶,硝酸,濃硫酸にはH3AsⅢ O3やH3AsⅤ O4となって溶ける.乾燥した空気中で安定であるが,加熱すると燃えてAs2O3になる.空気を断って,硫黄Sやハロゲン X2 と加熱すると,それぞれAs2S3,AsX3(F2 ではAsF5)が生成する.多くの金属とは高温で直接反応し,ヒ化物を生じる.多くの有機ヒ素化合物があるが,重要なものにアルシン酸R2AsⅤO(OH),アルソン酸RAsⅤO(OH)2(R:アルキル基,アリル基,ヘテロ環状基)とそれらの塩がある.
メチルアルシン酸,ジメチルアルシン酸,フェニルアルソン酸,ジフェニルアルシン酸は農薬(除草剤),医薬品に使用される.ジフェニルシアノアルシン,ジフェニルクロロアルシンはおう吐剤(旧日本軍化学兵器).超高純度ヒ素は化合物半導体として需要最大のヒ化ガリウムGaAs製造に用いられる.亜ヒ酸塩,ヒ酸塩は殺虫剤(農薬),防腐剤,なめし剤,なせんなどに使用される.そのほか,殺鼠剤,防蟻(ぎ)剤,除草剤,塗料,ガラス消泡剤に使用される.液晶ディスプレイガラス用がわが国の需要の大半を占めていたが,環境への配慮から無ヒ素化が進んでいる.合金への添加剤として,銅,鉛に添加すると硬さや耐食性が向上するので鉛蓄電池極板に使用される.毒性が強く,ヒ素,ヒ素化合物およびこれを含有する製剤は毒物劇物取締法の毒物に指定されている.PRTR法・特定第一種物質・発がん性クラス1,経口クラス2,作業環境クラス1.急性毒性の強さはアルシンAsH3がもっとも強く,亜ヒ酸塩がこれにつぐ.ヒ素化合物の致死量は1.5 mg/kg 体重(酸化ヒ素).急性中毒症状は,腹痛,おう吐,下痢,筋肉痛など.亜ヒ酸塩は労働安全衛生法の特定化学物質.「ヒ素及びヒ素化合物」は水道法水質基準値ヒ素の量に関して0.01 mg/L 以下,水質汚濁防止法有害物質で排水基準値ヒ素の量に関して0.1 mg/L 以下,土壌汚染対策法特定有害物質で,基準値は同じくヒ素の量に関して土壌含有量150 mg/kg 以下である.[CAS 7440-38-2]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
出典 株式会社平凡社百科事典マイペディアについて 情報
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...