改訂新版 世界大百科事典 「炭酸バリウム」の意味・わかりやすい解説
炭酸バリウム (たんさんバリウム)
barium carbonate
化学式BaCO3。天然には毒重石として産出する。工業的には,重晶石BaSO4を炭素とともに約800℃に熱して硫化バリウムBaSとし,その抽出液を熱しながら二酸化炭素を通じて沈殿させる。
BaSO4+2C─→BaS+2CO2
BaS+CO2+H2O─→BaCO3+H2S
3種の結晶形のものが知られているが,ふつうのものは無色,斜方晶系の結晶で,Ba2⁺,CO32⁻の両イオンが硝酸カリウム中のK⁺,NO3⁻の両イオンとまったく同様に配列している。比重4.43,水に対する溶解度2.2mg/100g(18℃)。全体の性質は炭酸カルシウムに似ているが,それよりずっと熱分解しにくく,約1400℃で分解して酸化バリウムBaOとなる。
BaCO3─→BaO+CO2
これは,Ba2⁺がCa2⁺よりずっと大きなイオンなので,CO32⁻イオンとの相互作用が弱く,これをCO2とO2⁻に分解させがたいためである。バリウムの塩類,光学ガラスなどの原料となる。有毒である。
執筆者:曽根 興三
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「炭酸バリウム」の意味・わかりやすい解説
炭酸バリウム
たんさんばりうむ
barium carbonate
炭酸のバリウム塩。天然には毒重石(どくじゅうせき)として産する。水酸化バリウムの水溶液に二酸化炭素を通じるか、バリウム塩の水溶液に炭酸アルカリを加えると沈殿してくる。工業的には、重晶石BaSO4を600~800℃で炭素で還元して硫化バリウムとし、その熱水溶液に二酸化炭素を通じて製造する。普通は無色の斜方晶系の結晶であるが、ほかに非晶質と六方晶系結晶の二変態がある。水にはほとんど溶けない。酸によって分解して二酸化炭素を発生する。二酸化炭素を含む水には炭酸水素バリウムとなって溶ける。炭酸カルシウムに比べ熱分解しにくい。バリウム塩やクリスタルガラス、光学ガラスの原料となるほか、陶磁器やほうろうのうわぐすり、金属熱処理の浸炭剤、殺虫剤や殺鼠(さっそ)剤に用いられる。有毒。
[鳥居泰男]
炭酸バリウム(データノート)
たんさんばりうむでーたのーと
炭酸バリウム
BaCO3
式量 197.3
融点 1740℃(CO2高圧下)
沸点 ―
比重 γ;4.43
結晶系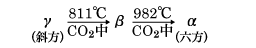
屈折率 (n)γ;1.529(c軸に平行)
溶解度 2.2mg/100g(水18℃)
化学辞典 第2版 「炭酸バリウム」の解説
炭酸バリウム
タンサンバリウム
barium carbonate
BaCO3(197.34).天然には毒重石として産出する.バリウム塩水溶液に炭酸アルカリを加えるか,水酸化バリウム水溶液に二酸化炭素を通じると得られる.α,β,γ形の三変態がある.普通は斜方晶系のγ形だが,高圧二酸化炭素中811 ℃ で非晶質のβ形に,982 ℃ で六方晶系のα形に転移する.融点1740 ℃(90 atm).密度4.43 g cm-3.空気中で加熱すると1450 ℃ で分解する.水に難溶.バリウム塩,光学ガラス,ブラウン管,電子材料,蛍光体,うわぐすり,塗料などの原料,殺そ剤などに用いられる.有毒.[CAS 513-77-9]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「炭酸バリウム」の意味・わかりやすい解説
炭酸バリウム
たんさんバリウム
barium carbonate
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...

