精選版 日本国語大辞典 「熱化学方程式」の意味・読み・例文・類語
ねつかがく‐ほうていしきネツクヮガクハウテイシキ【熱化学方程式】
日本大百科全書(ニッポニカ) 「熱化学方程式」の意味・わかりやすい解説
熱化学方程式
ねつかがくほうていしき
thermochemical equation
化学方程式に反応に伴う熱の出入量(反応熱)を付け加えて表した反応式をいう。反応熱は発熱の場合には正の符号、吸熱の場合には負の符号で示す。たとえば、一酸化炭素を空気中または酸素中で燃やすと発熱するが、これの熱化学方程式は、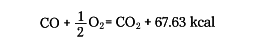
である。あるいは、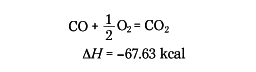
としてエンタルピー(熱含量)変化ΔHで表すこともある。この場合は系の吸熱を正とするので、発熱量は負の値になる。つまり一つの系を基準として考えるので増加する場合を正、減少する場合を負にとる。反応熱は反応物や生成物の状態(固相か液相か気相か)によって熱量が異なるから、必要ならばこれを付記する。たとえば、
H2(気)+Cl2(気)=2HCl(気)+44kcal
また、反応の温度を付記する場合もある。たとえば、
NaCl(固)+2H2O
=NaCl(溶液)+1.26kcal(25℃)
のように表す。
[戸田源治郎・中原勝儼]
化学辞典 第2版 「熱化学方程式」の解説
熱化学方程式
ネツカガクホウテイシキ
thermochemical equation
化学反応に伴う熱の放出・吸収を示す式.その熱量が反応に関与する各物質の物理的状態によって大きく異なるので,通常の化学方程式に加えて各物質の物理的状態を示す.たとえば,
C(s) + O2(g) = CO2(g),ΔH = -393.5 kJ mol-1
は12.01 g の固体炭素(黒鉛)と32 g の気体の酸素が完全に反応して,44.01 g の気体の二酸化炭素が定圧の条件下で生成されるときのエンタルピー減少量が393.5 kJ,すなわち,発熱反応であることを示している.反応熱を化学方程式の右辺に記すことも多い.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「熱化学方程式」の意味・わかりやすい解説
熱化学方程式【ねつかがくほうていしき】
→関連項目生成熱
出典 株式会社平凡社百科事典マイペディアについて 情報
改訂新版 世界大百科事典 「熱化学方程式」の意味・わかりやすい解説
熱化学方程式 (ねつかがくほうていしき)
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
世界大百科事典(旧版)内の熱化学方程式の言及
【化学反応】より
…反応熱に符号をつけ,反応系に加える熱を正,反応系から除く熱を負とすれば,発熱反応の場合は負,吸熱反応の場合は正となる。反応熱の大きさを化学反応式に書き加え等号で結んだのが熱化学方程式である。たとえば25℃,1気圧で, N2(g)+3H2(g)=2NH3(g)+91.80kJ化学記号の後のgは気相を意味する。…
【化学方程式】より
… 2Na+2H2O=H2+2NaOHこの式から46.0gのナトリウム(原子量23.0)は水と反応して1molの水素,すなわち0℃,1気圧のもとでは22.4lの水素を発生することがわかる。反応に伴う熱の出入りをも表した方程式を熱化学方程式という。たとえば,エチルアルコールC2H6O1molが燃焼して1368kJ(327kcal)の熱を発生し,二酸化炭素CO22molと液体の水H2O3molができるとき, C2H6O(液体)+3O2(気体)=2CO2(気体)+3H2O(液体); ⊿H=-1368kJ/molと記す。…
【反応熱】より
…熱力学的には両者は互いに変換される。化学方程式の後に反応熱を併記したものは熱化学方程式と呼ばれる。化学結合の再編成によって物質系のもつ内部エネルギーU(定容下)またはエンタルピーH(定圧下)の増減が熱の出入りとなって表れる。…
※「熱化学方程式」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

