精選版 日本国語大辞典 「ニトリル」の意味・読み・例文・類語
ニトリル
日本大百科全書(ニッポニカ) 「ニトリル」の意味・わかりやすい解説
ニトリル
にとりる
nitryl
nitrile
化学物質の一般名。無機化学でニトリル(nitryl)とよばれているものと、有機化学でニトリル(nitrile)とよばれているものがあるが、これらは英語名が異なることからわかるように、まったくの別物で、日本語に訳したときに同じ訳名になってしまったものである。有機化学のニトリルをカルボニトリル(carbonitrile)とよべば両者を混同することはない。
[廣田 穰 2015年3月19日]
無機化学
無機化学の分野では、NO2の原子団をニトリルとよんでいる。したがって以前はNO2+で表される1価陽イオンはニトリルイオンとよばれていた。現在、IUPAC命名法ではこの陽イオンを「ニトリルイオン」とよぶのは不適当とされ、「ジオキシド窒素イオン」と命名されている。しかし、フリーラジカルや置換基の名前としては「ニトリル」が残っている。
ハロゲン化ニトリルNO2X(Xはフッ素F、塩素Cl、臭素Br)は共有結合性の無色の気体で、フッ化ニトリルは沸点零下72.4℃、塩化ニトリルは沸点零下15℃であり、100℃では二酸化窒素と塩素とに分解する。そのほか(NO2)ClO4、(NO2)BF4、(NO2)PF6などが知られており、これらはイオン性の結晶である。また、五酸化二窒素N2O5も同様に(NO2)+(NO3)-であることが知られている。一般に加水分解によって硝酸を生ずる。
(NO2)ClO4+H2O
―→HNO3+HClO4
[加治有恒・廣田 穰 2015年3月19日]
有機化学
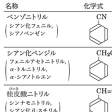
有機化学ではNO2+をニトロニウムイオンといい、通常はニトリルイオンとはいわない。炭素骨格Rにシアノ基-C≡Nが結合した化合物R-C≡Nをニトリルnitrileまたはカルボニトリルcarbonitrileとよぶ。芳香族ニトリル(、)と脂肪族ニトリル(、)に大別される。
[加治有恒・廣田 穰 2015年3月19日]
命名法
おもな命名法に次のようなものがある。
(1)ニトリルR-C≡Nを加水分解するとカルボン酸を生ずるので、ニトリルをカルボン酸の誘導体とみなして、炭素数が等しいカルボン酸の慣用名の語尾-oic acidのかわりにオニトリル-onitrileをつけて命名する。オは前の子音字と続けて読む。たとえば、酢酸acetic acid(CH3COOH)のニトリルはアセトニトリルacetonitrile(CH3C≡N)であり、アクリル酸acrylic acidのニトリルはアクリロニトリルacrylonitrileとよばれる。
ニトリルのIUPAC名は、同数の炭素原子をもつ炭化水素名の語尾にニトリル(-nitrile)をつけるとできる。たとえば、CH3CH2CH2CNの名前は、同数の炭素原子をもつ炭化水素CH3CH2CH2CH3の名前「ブタンbutane」の語尾に「ニトリルnitrile」をつけて、ブタンニトリルbutanenitrile(英語では1語)になる。
(2)環状カルボン酸などで命名の基礎となるカルボン酸名の語尾が‐カルボン酸-carboxylic acidで終わっているときには、これを‐カルボニトリル-carbonitrileとかえて命名する。たとえば、シクロヘキサンカルボン酸に対応するニトリルはシクロヘキサンカルボニトリルである。
(3)ニトリルは炭化水素残基のシアン化物ともみなせるので、炭化水素基名の前にシアン化をつける。たとえば、アセトニトリルはシアン化メチル、アクリロニトリルはシアン化ビニルともよばれる。
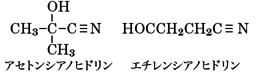
(4)ケトンやアルデヒドにシアン化水素を付加させると得られるα(アルファ)-ヒドロキシニトリルおよびアルケンオキシドとシアン化水素の付加物であるβ(ベータ)-ヒドロキシニトリルは、シアノヒドリン(シアンヒドリン)とよばれる。アセトンのそれはアセトンシアノヒドリン、エチレンオキシドのそれはエチレンシアノヒドリンとよばれる。
[加治有恒・廣田 穰 2015年3月19日]
性質
ニトリルR-CNは、イソニトリルR-NCと異性体の関係にあるが、性質や反応性はまったく異なる。酸により加水分解すると、ニトリルは比較的遅く反応して、アミドを経てカルボン酸になるが、イソニトリルは速やかに分解して、ホルムアミドを経て第一アミンになる。ニトリルは弱い臭気をもつ安定な化合物でそれほど強い毒性はないが、イソニトリルは特異の悪臭をもつ有毒な化合物であるので、両者は容易に区別できる。ただし、アクリロニトリルのような共役不飽和ニトリルは呼吸酵素との反応性が高く有毒である。
芳香族ニトリルは、第一アミンをジアゾ化した後、シアン化銅(Ⅰ)を作用させると得られる。
C6H5NH2+HNO2―→C6H5N2+
C6H5N2++CuCN―→C6H5CN
脂肪族ニトリル(シアン化アルキル)は、ヨウ化アルキルとシアン化カリウムをエタノール(エチルアルコール)水溶液またはジメチルホルムアミド中で加熱すると得られる。また、一般に有機酸アミドと五酸化二リンとを加熱すると得られる。
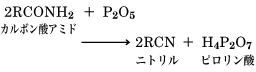
工業的にはアルケンとアンモニアと酸素を高温で反応させてつくる。
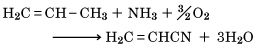
ニトリルをエタノール中でナトリウムと反応させるとアミンが得られる。また、乾燥塩化水素を反応させると塩化イミドイルが得られ、これは有機合成の有用な中間体である。
[加治有恒・廣田 穰 2015年3月19日]
改訂新版 世界大百科事典 「ニトリル」の意味・わかりやすい解説
ニトリル
nitrile
炭化水素基にシアン基-C≡Nが結合した化合物の総称で,シアン化物ともいう。一般式R-C≡N。イソニトリルR-N=Cとは異性体の関係にある。命名法のおもなものとしては次の三つがある。(1)ニトリルをカルボン酸の誘導体とみなし,炭素数が等しいカルボン酸の慣用名の酸語尾-ic acidの代りに-onitrileをつけ,これを音訳する。(2)環状カルボン酸などで-carboxylic acidと呼ばれるときには-carbonitrileとする。(3)ニトリルを炭化水素のシアン化物とみなし,炭化水素基名の前に〈シアン化〉をつける。たとえばCH3CNは,(1)に従えばアセトニトリル(acetic acid→acetonitrile),(3)に従えばシアン化メチルと呼ばれる。
低分子量のニトリルは,特異な臭いをもつ無色の液体で,炭素数が多くなると水に溶けにくくなる。アクリロニトリルCH2=CHCNのように有毒なものもあるが,ニトリルの毒性はさほど強くない。無機酸または無機塩基を触媒として加水分解すると,酸アミドを経由してカルボン酸とアンモニアを生じる。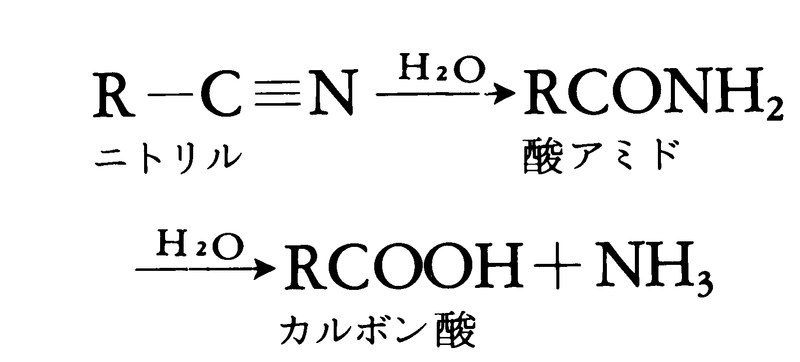
また,水素化アルミニウムリチウムや水素化ホウ素ナトリウムで還元すると第一アミンを生成する。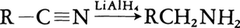
ニトリルの合成法のうち一般的なものを次に記す。
(1)カルボン酸アミドの脱水 脱水剤としては五酸化リンP2O5,塩化チオニルSOCl2等が用いられる。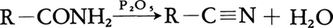
(2)ハロゲン化アルキルの置換反応 この方法は脂肪族ニトリルの合成に用いられる。
R-X+KCN─→R-C≡N+KX
(3)ザントマイヤー反応 この方法は芳香族ニトリルの合成に用いられる。
2Ar-N2⁺X⁻+Cu2(CN)2─→2Ar-CN+2N2+Cu2X2
(4)アセチレンへのシアン化水素の付加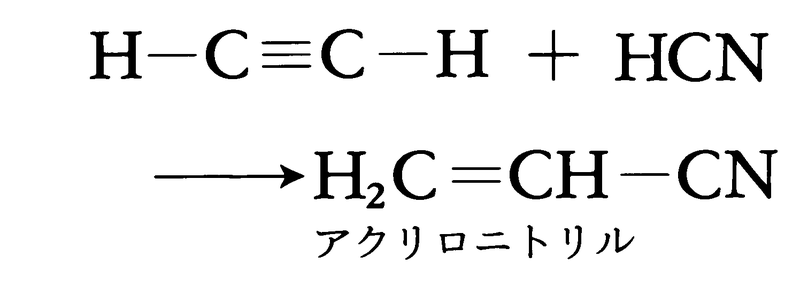
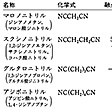
低分子量の脂肪族ニトリルは溶剤として用いられるが,一般にニトリルは有機合成中間体としての用途が広い。ジカルボン酸の誘導体で分子内に2個のシアン基をもつ化合物のうちマロノニトリルNCCH2CNは活性メチレンをもつ化合物として有機合成にしばしば用いられており,アジポニトリルNC(CH2)4CNはナイロン66の原料として多量に使われている。また,分子内に多数個のシアン基をもつ化合物のうち,テトラシアノエチレンやテトラシアノキノジメタンは,シアン基が大きな電子吸引性をもつことから,電荷移動錯体合成の際の電子受容体として使われており,有機半導体の合成に一役買っている。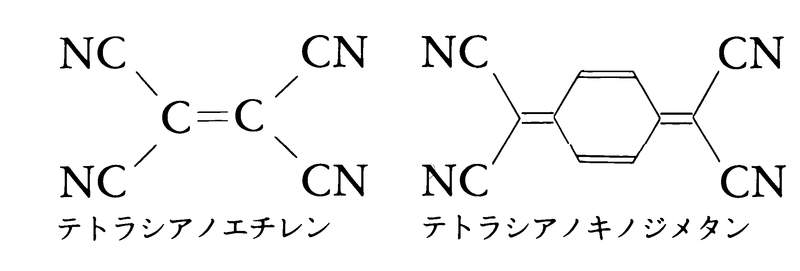
執筆者:井畑 敏一
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「ニトリル」の解説
ニトリル
ニトリル
nitrile
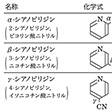
【Ⅰ】ニトリル(nitrile).シアノ基-C≡Nが炭化水素基Rと結合した有機化合物RCNの総称.炭化水素の末端の H3 を≡Nで置換したものと考え,炭化水素名に“ニトリル”をつけて命名する(ヘキサンニトリルCH3(CH2)4CNなど).環式化合物のH原子をCNで置換したものと考え,母体化合物名に“カルボニトリル”をつけて命名する(図の構造をもつ,4-ピリジンカルボニトリルなど).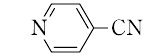 通俗名をもつカルボン酸から誘導されたニトリルは,そのカルボン酸の英語名の語尾-icまたは-oicを-onitrile(オニトリル)にかえて命名する(アセトニトリル,ベンゾニトリルなど).また,炭化水素基のシアン化物としても命名される(シアン化メチルCH3CN,シアン化ベンジルC6H5CH2CNなど).脂肪族ニトリルはハロゲン化アルキルまたは硫酸ジアルキルにシアン化アルカリを作用させると得られる.芳香族ニトリルは第一級アミンをジアゾ化した後,シアン化銅(Ⅰ)を作用させると得られる(ザントマイヤー反応).また,カルボン酸のアンモニウム塩またはアミドを五酸化リンなどで脱水しても得られる.一般に,特有の臭いをもつ無色の液体または固体.赤外スペクトルには,2260~2240 cm-1 に特性吸収を示す.酸またはアルカリで加水分解され,酸アミドを経てカルボン酸になる.還元されて第一級アミンとなる.【Ⅱ】陽イオンまたは陽イオン性原子団NO2に対する国際的な名称nitrylの音訳である.しかし,日本語では有機化合物のニトリル(nitrile)との混同を避けるため,ニトロイル(nitroyl)(ニトロイル化合物)を用いる.なお,ニトロキシル(nitroxyl),およびイオン性のニトロイル化合物への名称ニトロニウム(nitronium)は,いずれも望ましくないとされるが,日本語での“ニトリル”とともに一部で通用している.
通俗名をもつカルボン酸から誘導されたニトリルは,そのカルボン酸の英語名の語尾-icまたは-oicを-onitrile(オニトリル)にかえて命名する(アセトニトリル,ベンゾニトリルなど).また,炭化水素基のシアン化物としても命名される(シアン化メチルCH3CN,シアン化ベンジルC6H5CH2CNなど).脂肪族ニトリルはハロゲン化アルキルまたは硫酸ジアルキルにシアン化アルカリを作用させると得られる.芳香族ニトリルは第一級アミンをジアゾ化した後,シアン化銅(Ⅰ)を作用させると得られる(ザントマイヤー反応).また,カルボン酸のアンモニウム塩またはアミドを五酸化リンなどで脱水しても得られる.一般に,特有の臭いをもつ無色の液体または固体.赤外スペクトルには,2260~2240 cm-1 に特性吸収を示す.酸またはアルカリで加水分解され,酸アミドを経てカルボン酸になる.還元されて第一級アミンとなる.【Ⅱ】陽イオンまたは陽イオン性原子団NO2に対する国際的な名称nitrylの音訳である.しかし,日本語では有機化合物のニトリル(nitrile)との混同を避けるため,ニトロイル(nitroyl)(ニトロイル化合物)を用いる.なお,ニトロキシル(nitroxyl),およびイオン性のニトロイル化合物への名称ニトロニウム(nitronium)は,いずれも望ましくないとされるが,日本語での“ニトリル”とともに一部で通用している.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「ニトリル」の意味・わかりやすい解説
ニトリル
→関連項目イソニトリル
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「ニトリル」の意味・わかりやすい解説
ニトリル
nitrile
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「ニトリル」の解説
ニトリル
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...