改訂新版 世界大百科事典 「幾何異性」の意味・わかりやすい解説
幾何異性 (きかいせい)
geometrical isomerism
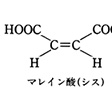
もともとは炭素-炭素二重結合に結合する置換基の位置の関係によって生じる異性。現在では炭素以外の原子を含む二重結合や環式化合物に結合する置換基,錯体での配位子の位置などの関係によって生じる異性をもさす。1874年ファント・ホフは炭素原子の正四面体構造を論じた論文で,分子内に自由回転できない二重結合をもち,しかも二重結合している炭素にいずれも同じ置換基が結合しているとき,二つの原子(団)が二重結合の同じ側にくる場合と反対側にくる場合があることを指摘した。この種の異性体の最初の例は,J.A.ウィスリツェヌスが87年に報告したフマル酸とマレイン酸であった。マレイン酸は加熱すると容易に水を失って無水マレイン酸になるのに対して,フマル酸は強熱しない限り水を失わず,そのうえ脱水生成物は無水マレイン酸であることから,二つのカルボキシル基が二重結合の同じ側にくるものをシスcis型,反対側にくるものをトランスtrans型と呼ぶようになった。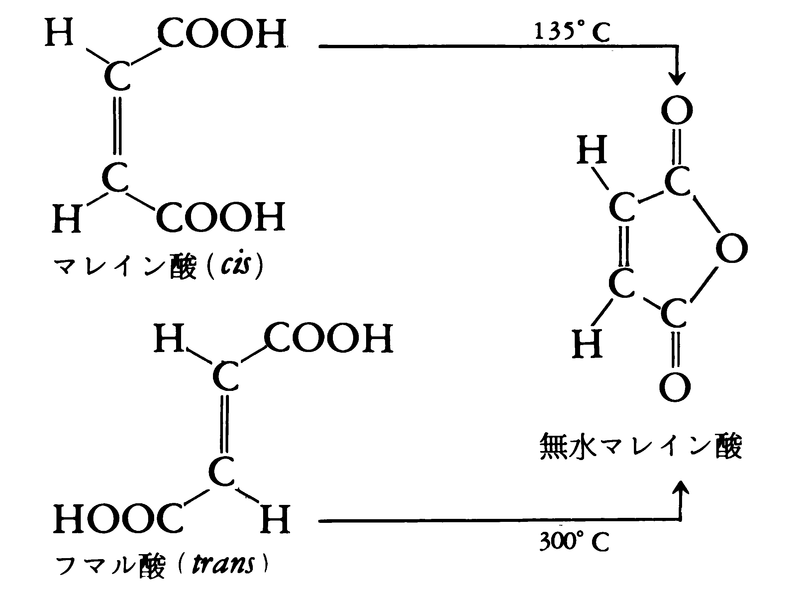
幾何異性体ないしシス-トランス異性体は光学異性体と異なり,異性体間の物理的・化学的性質に著しい差がある場合が多いため,両者を分離することは比較的容易である。一般にトランス型に比べてシス型が不安定であるが,これは同じ側にある二つの置換基の間の立体障害によるものである。
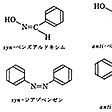
幾何異性は炭素-炭素二重結合だけではなく,炭素-窒素あるいは窒素-窒素二重結合をもつ化合物(たとえばオキシムやアゾ化合物)にも認められることが19世紀末までにわかってきた。シスアゾベンゼンは(トランス)アゾベンゼンに比べてかなり不安定であり,容易にトランス体に異性化する。一方,トランス体を光照射するとシス体となる。オキシムやアゾ化合物では,シス型にはシンsyn-,トランス型にはアンチanti-の表記が使われている。
種々の構造をもつアルケン(たとえば4種の異なる原子(団)が結合したエチレン)が得られるようになると,シスまたはトランスで幾何異性体を命名することが困難になってきた。現行のIUPACの立体化学命名法によると,二重結合に結合した2個の原子(団)に順位規則に従ってそれぞれ優先順位をつけ,順位の高い原子(団)が同じ側の異性体をZ(zusammenの略で〈いっしょに〉の意),反対側の異性体をE(entgegenの略で〈に対して〉の意)と命名する。これによるとマレイン酸はZ型,フマル酸はE型である。
執筆者:竹内 敬人
錯体の幾何異性
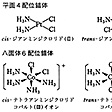
錯体中での配位子の立体配置の違いによって幾何異性が生ずる場合は,配位数4以上,とくに平面型4配位と八面体型6配位の錯体に多くみられる。平面型4配位では,たとえば[PtCl2(NH3)2]に次のような二つの異性体が存在する。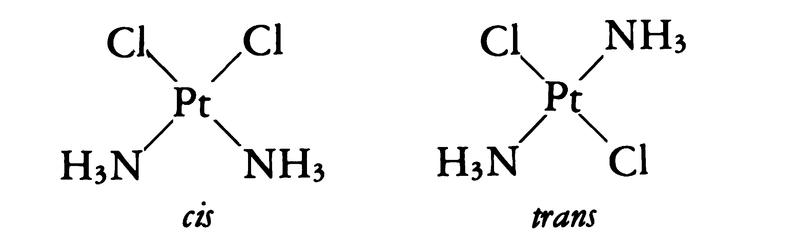
すなわち中心原子のPtに対し,四つの結合原子が同一平面内にあるとき,上記のような2種の配位子の組合せでは,必ず2通りの方法があるわけであり,実際にも2種類の化合物(物理的および化学的性質が違う)が得られる。これらはcis-[PtCl2(NH3)2],trans-[PtCl2(NH3)2]のように表して区別される。また配位子がすべて違う[MABCD]では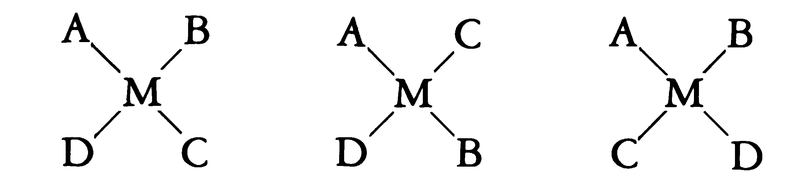
の3種が存在する。
八面体型6配位では,その構造を表すために,次のような配位座の番号づけをするのが普通である。すなわち八面体の一つの正三角形に垂直な方向から見た透視図をかき,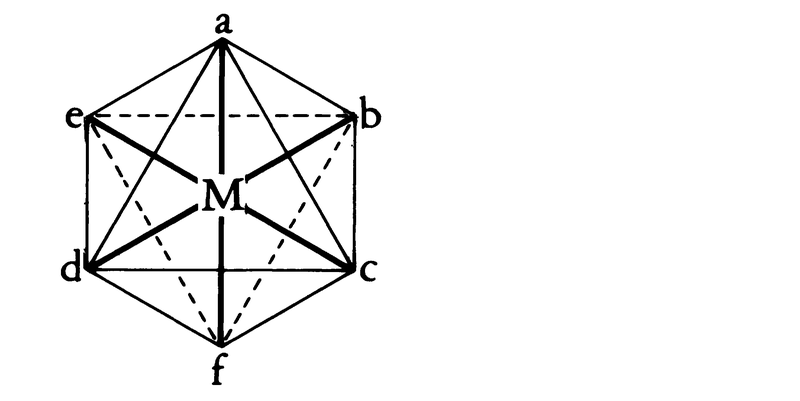
右まわりらせんで順序づけをする。このようにしてa位に配位子があると,次に配位子の入る位置は,b,c,d,e位の四つはいずれにしてもa位に対して隣りあっているシス位にあることになり,f位のみが反対側にあるトランス位にあることになる。これらはたとえば[PtCl4(NH3)2]や[CoCl2(en)2]⁺などでは次のようになる(en=NH2CH2CH2NH2)。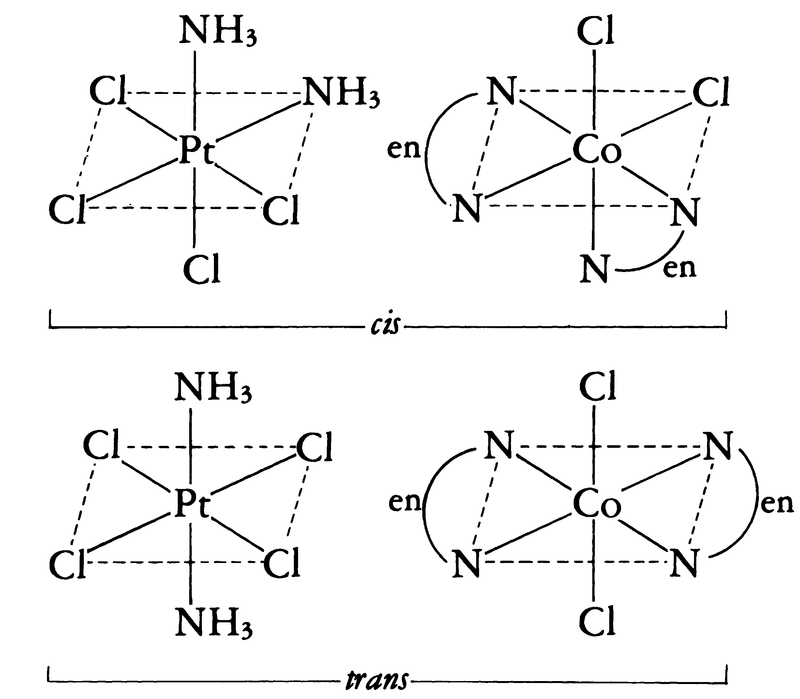
なお,このときcis-[CoCl2(en)2]⁺ではさらに光学異性体が存在する。配位子をさらに変えてMA3B3型とするときは,a,b,c型とa,b,f型の二つの異性体が存在することになる。たとえば[CoCl3(NH3)3]では次のようである。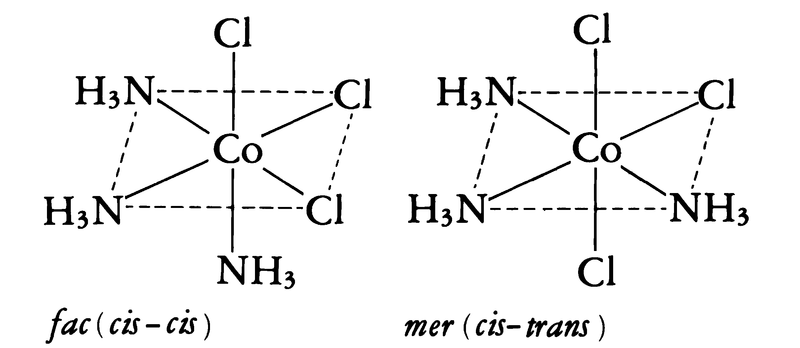
この関係は前者は,三つの配位子が八面体の一つの面上にあることから面を意味するfacialからfac,後者は子午線を意味するmeridianからmerをつけて区別する。八面体型6配位では,配位子の種類がふえると異性体の数はふえ,たとえば,[MABCDEF]のように,6種類の配位子がすべて異なる場合の立体配置は,全部で15種類あることになり,異性体もその数だけ存在する。
執筆者:中原 勝儼
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「幾何異性」の解説
幾何異性
キカイセイ
geometrical isomerism
立体異性の一種で,シス-トランス異性ともいう.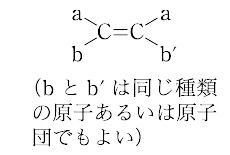 【Ⅰ】上記の化合物は平面分子であるが,同じ原子あるいは原子団aが,二重結合に対して同じ側に結合しているシス形と,反対側に結合しているトランス形の2種類の異性体が存在する.幾何異性の最初の例は,J.A. Wislicenus(ウィスリツェーヌス)によって1887年に発見されたフマル酸(融点287 ℃)とマレイン酸(融点130 ℃)である.幾何異性体は,一般に物理的・化学的性質が違う.
【Ⅰ】上記の化合物は平面分子であるが,同じ原子あるいは原子団aが,二重結合に対して同じ側に結合しているシス形と,反対側に結合しているトランス形の2種類の異性体が存在する.幾何異性の最初の例は,J.A. Wislicenus(ウィスリツェーヌス)によって1887年に発見されたフマル酸(融点287 ℃)とマレイン酸(融点130 ℃)である.幾何異性体は,一般に物理的・化学的性質が違う.
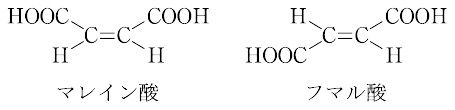
異なる原子あるいは原子団が二重結合に結合した場合でも,E-Z表示によれば一義的に区別できる([別用語参照]E,Z命名法).幾何異性はC=Cの二重結合だけでなく,N=NやC=Nなどの二重結合をもつ化合物にもみられる.たとえば,普通のアゾベンゼンはトランス形であるが,紫外線を照射すると,一部シス形にかわる.
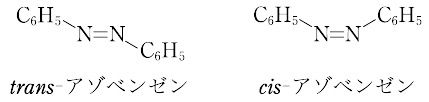
オキシムの立体異性体は,シス,トランスのかわりにシン(syn),アンチ(anti)を使うのが普通である.
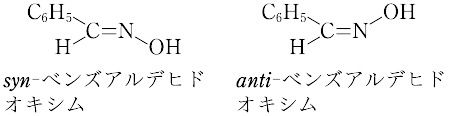
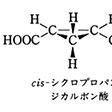
【Ⅱ】環式化合物で,環が平面ないし平面とみなされる場合,環の平面に対して同じ側にある置換基をシス,反対側にある置換基をトランスという.たとえば,1,2-ジクロロシクロプロパンには,次のような幾何異性体が存在する.
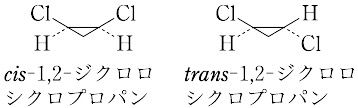
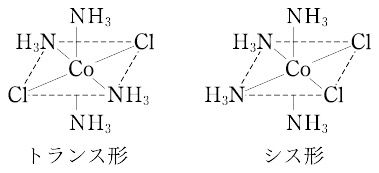
【Ⅲ】錯化合物において,中心原子(またはイオン)に配位する同種の配位子が,互いに近いものをシス,遠いものをトランスという.たとえば,[CoCl2(NH3)4]Clの組成をもつ錯塩のうち,プラセオ塩(緑色)はトランス形で,ビオレオ塩(紫色)はシス形である.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
日本大百科全書(ニッポニカ) 「幾何異性」の意味・わかりやすい解説
幾何異性
きかいせい
geometrical isomerism
分子やイオンの立体構造の違いによって生ずる異性の一種。有機化合物では、二重結合あるいは脂環構造をもつものに多くみられ、錯体では配位子位置の相互関係から生ずるものが多い。炭素‐炭素二重結合を挟んだシス‐トランス異性の例にはマレイン酸とフマル酸があるが、同様の幾何異性が窒素‐炭素あるいは窒素‐窒素二重結合に関するときにはシン‐アンチsyn-anti異性という。二重結合についてはE、Z方式という表記法もある。シクロプロパンジカルボン酸では、環を挟むシス‐トランス異性がある。
同じ配位子を2個もつ平面4配位錯体および八面体6配位錯体では、中心原子に対してのシス‐トランス異性がある。八面体6配位錯体で配位子の種類と個数の組合せが複雑になると、さらに多くの幾何異性が現れる。
[岩本振武]
百科事典マイペディア 「幾何異性」の意味・わかりやすい解説
幾何異性【きかいせい】
→関連項目異性|グッタペルカ
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「幾何異性」の意味・わかりやすい解説
幾何異性
きかいせい
geometrical isomerism
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...