精選版 日本国語大辞典 「ダニエル電池」の意味・読み・例文・類語
ダニエル‐でんち【ダニエル電池】
日本大百科全書(ニッポニカ) 「ダニエル電池」の意味・わかりやすい解説
ダニエル電池
だにえるでんち
Daniell cell
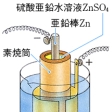
1836年にイギリスのダニエルによって考案された歴史的な電池で、電池の理論的説明には必須(ひっす)のものとなっている。多孔質の隔膜で仕切られた負極室には硫酸亜鉛ZnSO4水溶液と亜鉛電極を、また正極室には硫酸銅CuSO4水溶液と銅電極を入れた二液式の電池である。電池式では
Zn|ZnSO4‖CuSO4|Cu
と示すことができる。両電極を導線でつないで放電すると
(負極)
Zn―→Zn2++2e-
(正極)
Cu2++2e-―→Cu
(全体)
Zn+Cu2+―→Zn2++Cu
の反応がおこり、正極から負極へ電流が流れる。起電力は1.07~1.14ボルトで起電力変化は小さく、気体の発生もない。かつては電話交換機用電源として用いられたこともあったが、銅イオンが負極室へ拡散して自己放電をおこすため、液の交換を頻繁に行わなければならず、現在では実用性はなくなっている。
なお、逆方向に起電力より大きい電圧を印加(加えること)して電流を流し充電すると、上式の逆に反応が進み元に戻る。このような可逆性のある電池を可逆電池という。また、金属をM、その塩をMXとするとき、2種の金属と2種の塩を組み合わせた
M1|M1X1‖M2X2|M2
の形の電池を一般にダニエル形電池という。
[浅野 満]
『橋本尚著『電池の科学――生物電池から太陽電池まで』(1987・講談社)』▽『小久見善八編著『電気化学』(2000・オーム社)』▽『電気化学会編『電気化学便覧』(2000・丸善)』▽『電池便覧編集委員会編『電池便覧』(2001・丸善)』
改訂新版 世界大百科事典 「ダニエル電池」の意味・わかりやすい解説
ダニエル電池 (ダニエルでんち)
Daniell cell
隔膜によって仕切られた2室の一方に硫酸銅CuSO4水溶液と銅Cu板,他方に硫酸亜鉛ZnSO4水溶液と亜鉛Zn板を入れた電池で,1836年J.F.ダニエルの考案になる。起電反応は
Cu2⁺+Zn─→Cu+Zn2⁺
で,起電力は約1.1V。歴史的な電池で現在は用いられていない。
執筆者:笛木 和雄
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「ダニエル電池」の解説
ダニエル電池
ダニエルデンチ
Daniell cell
1836年J.F. Daniell(ダニエル)により発明された電池で,次のような構成よりなる.
Zn|ZnSO4|CuSO4|Cu
すなわち,素焼きのような多孔性物質で隔てられた2種類の溶液を含む2液一次電池の一種である.電池反応は,
Zn + CuSO4 → Cu + ZnSO4
であり,両電解液の濃度が等しいときの理論起電力は1.07 V である.この電池は自己放電による消耗が大きく,使用上も不便なので,現在では歴史的ないしは教育的な意味しかない.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「ダニエル電池」の意味・わかりやすい解説
ダニエル電池【ダニエルでんち】
→関連項目一次電池|ダニエル
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「ダニエル電池」の意味・わかりやすい解説
ダニエル電池
ダニエルでんち
Daniell cell
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
世界大百科事典(旧版)内のダニエル電池の言及
【ダニエル】より
…31年ロンドンのキングズ・カレッジ設立時に化学教授に就任する。36年,長時間安定した電圧・電流を与えるいわゆるダニエル電池を考案し,電気学やその実用面の発展を促した。気象学にも業績があり,露点湿度計を発明し,《気象学エッセー集》を出版した。…
【電気化学】より
… 電気化学の研究対象となる最も基本的な系は,異種の電気の導体(そのうち少なくとも一つは電解質溶液のようなイオン伝導体とする)が直列につながっていて,その末端相の化学的組成が等しいものであり,これをガルバーニ電池という。その代表的な例はダニエル電池で,この種の系の構成を模式的に次のように表すことが多い。 Cu(端子)|Zn(電極)|ZnSO4(溶液)| CuSO4(溶液)|Cu(電極)|Cu(端子)硫酸亜鉛ZnSO4溶液と硫酸銅CuSO4溶液の濃度が相等しく,かつ電池内に電流が流れていないときには,銅Cu電極は亜鉛Zn電極に対して約1.1Vの電位差を示す。…
※「ダニエル電池」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...