精選版 日本国語大辞典 「炎色反応」の意味・読み・例文・類語
えんしょく‐はんのう‥ハンオウ【炎色反応】
- 〘 名詞 〙 アルカリ金属などの塩類を炎の中に入れると、炎がその元素特有の色を現わす反応。揮発した金属原子が炎によって励起され、元素固有の可視光線を出すために起こる。〔稿本化学語彙(1900)〕
日本大百科全書(ニッポニカ) 「炎色反応」の意味・わかりやすい解説
炎色反応
えんしょくはんのう
flame reaction
アルカリ金属、アルカリ土類金属などの塩類をブンゼンバーナーの無色の炎中にて強熱すると、各金属元素特有の色を示す反応。発見者ドイツのブンゼンの名にちなんでブンゼン反応ともいう。この反応を利用して金属の定性分析を行うことを炎色試験といい、定性分析の補助法として重要である。この炎色の現象は、揮発性塩の解離で生じた励起金属原子が発する輝線スペクトルのうちで、特定の波長の光が強く発光することによる。波長と炎光強度の関係を測定したものを炎光スペクトルという。
普通、炎色反応を観察するには、ガラス棒の先端につけた白金線を塩酸に浸してから何度も焼いて清浄にし、試料の少量をつけて炎中に入れ、低温部からしだいに高温部に移す。炎色を直接目で見るほかに、携帯用の直視分光器を使えば便利であり、またナトリウムNaとカリウムKが共存する場合のように、コバルトガラスを用いてナトリウムの黄色を吸収して、カリウムの紫色を観察するという方法もよく用いられる。炎色反応は主として定性分析に用いられるが、この炎色は各元素に固有な波長の光の発光現象なので、これをさらに正確に知るためには、炎の色を分光器(プリズムあるいは回折格子分光器)によって確かめればよく、その強度から定量分析を行うことができる。この分析法をフレーム分光分析または炎光分光分析という。
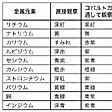
分光分析は1860年ドイツのキルヒホッフとブンゼンによって確立され、同年セシウムCsの発見、ついで1861年ルビジウムRbの発見につながったことは有名であり、その後1898年キュリー夫妻によるラジウムRa発見にあたり、分光スペクトルにより新元素であることを確認したことはとくに有名である。各金属元素の炎の色を直接目で見た場合とコバルトガラスを通して見た場合の色はのとおりである。
ナトリウムの基底状態の電子配置は1s22s22p63s1のようにナトリウムの原子核の周りに11個の電子がある。10個の電子はネオンNeと同じく閉殻電子配置をとり、最外殻の1個の3s電子は炎中で熱エネルギーを吸収していろいろな励起状態の原子になる。このうち3pに励起したナトリウム原子が放出する光がナトリウムD線に関係するので、ナトリウムの炎色反応が黄色に見えるのは、炎中に存在する励起ナトリウム原子の3p、4p、5p……のような軌道にある電子が3sに落ち込むときに両者のエネルギー差に相当する光を放出するが、そのうち3pから3sに落ちるときに発光する黄色の光がとくに強く観察されるためである。これがナトリウムD線で、分解能のよいプリズム分光器や回折格子分光器で観測すれば接近した二重線として観測される。4p、5p……から3sに落ち込む一連のスペクトルが近紫外部にかけて同時に観察されるはずであるが、色としては観測されない。このような原子の発光に基づく一連のスペクトルを原子スペクトルといい、鋭い線スペクトルを生じる。励起状態から、より低い励起状態や基底状態に落ちるときに放出するスペクトルは発光スペクトルで、輝線スペクトルともいう。これに対して低いエネルギー状態から高いエネルギー状態に電子が励起されるときは吸収スペクトルを与え、黒線スペクトルともいう。太陽の黒線スペクトルはこの例で、とくにフラウンホーファー線という。
ナトリウムD線が二重線を与える原因の究明から、電子がスピンをもつということが明らかになった。電子が自転するのである。すなわち、ナトリウムの基底状態の3s電子も励起状態の3p電子も軌道運動をすると同時にスピンもすると、アメリカの物理学者ハウトスミットとウーレンベックは考えた。すると軌道運動の角運動量ベクトルとスピン角運動の角運動量ベクトルが相互作用して内部角運動量ベクトル(全角運動量ベクトルともいう)が生じると、H・N・ラッセルとソーンダースFrederick Albert Saunders(1875―1963)は考えた。これをL‐S結合またはラッセル‐ソーンダース結合という。軌道角運動の量子数をL、スピン角運動の量子数をS、内部角運動の量子数をJと表すとJのとりうる値は
J=L+S,L+S-1,
L+S-2,……,|L-S|
である。ナトリウムのp電子はL=1であり、S=1/2である。したがって、
J=1+1/2,1+1/2-1,……
となるが最後は|1-1/2|で、結局ナトリウムのpはJ=3/2とJ=1/2の二つの状態をとる。Jは一つずつ減少するから3/2、1/2、-1/2となっていくはずであるが、負の値はとらないから、3/2と1/2だけになる。これを2P3/2と2P1/2のように表す。左肩の数字はスピン多重度で2S+1の値を示す。一方3s電子についてはL=0であり、S=1/2である。したがって、ナトリウムのS項はJ=1/2の状態のみである。これを2S1/2と表す。Lの選択率はΔL=0,±1(ただし、L=0のときはΔL=0の遷移は禁制である)であり、Jの選択率はΔJ=0,±1であり、Sの選択率はΔS=0である。スピンに関しては同じ多重度の遷移が可能である。したがって、2P3/2から2S1/2への遷移と2P1/2から2S1/2への遷移が可能となる。いずれも遷移の選択率を満足する許容遷移である。2P3/2と2P1/2はエネルギーが接近しているから、この二つのスペクトル線は接近した二重線として観測される。
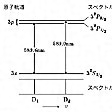
はナトリウムのグロトリアン図Grotrian diagramの一部で、原子軌道3sと3pの順位間でおこるナトリウムD線のようすを模式的に示した。3p原子軌道はエネルギーが縮退しているが、L‐S結合するとわずかに分裂してエネルギー差を生じる。スペクトルは589.6ナノメートル(1ナノメートルは10億分の1メートル)にD1、589.0ナノメートルにD2の二重線を生じる。両矢印で示したのは、エネルギーの低いほうから励起するときに吸収スペクトル線を生じ、逆にエネルギーの高いほうから低いほうに落ち込むときは発光スペクトル線を生じ、波長は同じであることを示している。横軸は振動数ν(ニュー)で、エネルギーに比例する量である。波長の長いほうがエネルギーは小さいので左側がD1で、右側がD2である。なお、ナトリウム原子のような電子配置の原子の場合は、1sと2s、2pの10電子はネオンと同じ閉殻電子配置で、その外側に荷電子が1個回っているというモデルで考えることができる。この場合は原子軌道の記号s、p、d、fをそのままスペクトル項の記号とすることができ、大文字で表す。すなわちS項、P項、D項、F項である。原子軌道の記号s、p、d、fはスペクトル項の記号S、P、D、Fに由来する。Fの後はG、H、Iのようにアルファベット順に表す。Sはsharp series(鋭系列)、Pはprincipal series(主系列)、Dはdiffuse series(鈍系列)、Fはfundamental series(基本系列)に由来する。ナトリウムの原子スペクトルの研究からP系列を主系列としたのはD線が強く観測されることから当然であったであろう。周期表でナトリウムの次の元素マグネシウムMgの基底状態の電子配置は1s22s22p63s2のようにマグネシウム原子核の周りに12個の電子がある。最外殻に3s電子が2個になると解釈が複雑になるが、現在では詳しく解明されている。
炎色反応は化合物の種類に関係なく、たとえばナトリウムでは黄色が観測される。塩化ナトリウムNaClであれば炎中で
NaCl―→Na+1/2Cl2
のように分解し、炭酸ナトリウムNa2CO3であれば
Na2CO3―→Na2O+CO2
の分解の後、さらに
Na2O―→2Na+O2
のように分解し、結局ナトリウム原子の炎色反応が観測される。
[成澤芳男]
『フリードリッヒ・フント著、山崎和夫訳『量子論の歴史』(1978・講談社)』▽『M・E・ウィークス、ヘンリー・M・レスター著、大沼正則監訳『元素発見の歴史3』(1990・朝倉書店)』▽『宮田光男編『化学が好きになる実験』(1990・裳華房)』▽『杉山剛英著『どきどき化学なるほど実験』(2000・裳華房)』
改訂新版 世界大百科事典 「炎色反応」の意味・わかりやすい解説
炎色反応 (えんしょくはんのう)
flame reaction
単体または化合物を炎の中に入れて熱すると,炎がそれらの元素に固有の色を呈する。この反応を炎色反応という。この呈色は,熱によって励起された原子が,不安定な励起状態から安定な基底状態に戻るときに発する輝線スペクトルによるものであり,アルカリ金属,アルカリ土類金属をはじめとする元素の定性分析の際の補助手段として利用される。ふつう,塩酸に浸し炎で焼いた清浄な白金線の先端に,塩酸で湿した試料を微量つけてブンゼンバーナーの酸化炎中に入れ,直接肉眼で,あるいは青色コバルトガラスを通して観察する。ブンゼンバーナーでは温度が低すぎて励起されないセシウムなどの場合には,より高温の酸水素炎などを利用する。おもな元素による炎色反応の色を表に示す。なお,分光器を使用すれば,それぞれの元素に固有な輝線スペクトルの波長が正確に測定でき,定性分析ばかりでなく,その強度から定量分析を行うことができる。
→炎光光度法
執筆者:原口 紘炁
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
最新 地学事典 「炎色反応」の解説
えんしょくはんのう
炎色反応
flame reaction
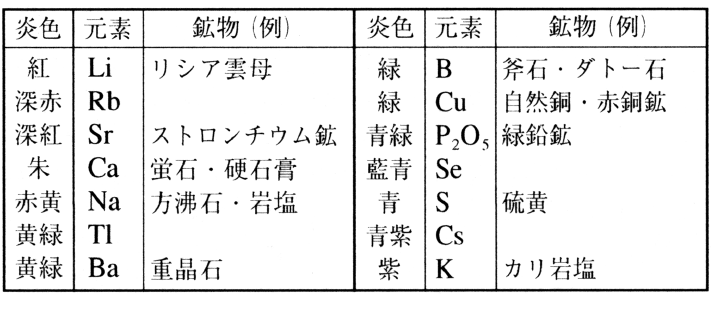
ある特定の元素または塩類を無色の炎の中に入れて熱すると,それぞれに特有の色を示す。これは金属の蒸気が熱せられて発する輝線スペクトルのうち,ある波長の光が特に強いために生ずる現象で,元素検出のための定性分析として利用される。塩酸をつけて強熱することを繰り返して清浄にした白金線をさらに塩酸に湿し,その先に鉱物粉末を少量つけて,炎の低温部から高温部に移して炎色を観察する。その際,直視分光器・フィルター用色ガラスを用いることもある。
執筆者:青木 義和
出典 平凡社「最新 地学事典」最新 地学事典について 情報
百科事典マイペディア 「炎色反応」の意味・わかりやすい解説
炎色反応【えんしょくはんのう】
→関連項目線スペクトル|定性分析|リン(燐)塩球試験
出典 株式会社平凡社百科事典マイペディアについて 情報
化学辞典 第2版 「炎色反応」の解説
炎色反応
エンショクハンノウ
flame reaction
アルカリ金属,あるいはアルカリ土類金属などの塩を炎のなかに入れると,揮発してできた金属原子が励起され,元素固有の可視光線を出す.これを炎色反応という.G.R. KirchhoffとR.W.E. Bunsen(ブンゼン)は,元素と波長を正確に結びつけた.この原理は炎光分析あるいはフレーム吸光光度法に利用され,とくにナトリウム(黄,589.3 nm),カリウム(紫,404.4 nm),リチウム(赤,670.8 nm),ルビジウム(赤,795.0,781.1 nm)などの定量分析に広く利用されている.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「炎色反応」の意味・わかりやすい解説
炎色反応
えんしょくはんのう
flame reaction
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...