翻訳|coenzyme
精選版 日本国語大辞典 「補酵素」の意味・読み・例文・類語
ほ‐こうそ‥カウソ【補酵素】
- 〘 名詞 〙 酵素作用は酵素蛋白と、非蛋白性の有機化合物の結合によって生ずるが、この後者の有機化合物をいう。たとえば、ビタミンは体内で種々の酵素の補酵素として生物学的活性を示すとされている。助酵素。〔人体の機能(1952)〕
日本大百科全書(ニッポニカ) 「補酵素」の意味・わかりやすい解説
補酵素
ほこうそ
coenzyme
酵素のタンパク質部分(アポ酵素という)と可逆的に結合して酵素作用の発現に寄与する補欠分子族(補欠分子団)をいう。助酵素、コエンチーム、コエンザイムともよばれる。普通はアポ酵素のみ、あるいは補酵素のみでは活性をもたないが、両者が結合すると複合体(ホロ酵素という)を形成して酵素作用を示すようになる。結合が弱く解離しやすい補酵素は、多くの類似の反応に共通な基質(補基質)とみなすことができる。
水溶性ビタミンの大部分は補酵素の成分である。水溶性ビタミンから誘導される補酵素としては、チアミン(ビタミンB1)→チアミンピロリン酸(TPP)、リボフラビン(ビタミンB2)→フラビンアデニンジヌクレオチド(FAD)とフラビンモノヌクレオチド(FMN)、ニコチン酸(ナイアシン)→ニコチンアミドアデニンジヌクレオチド(酸化型NAD・NAD+)、ピリドキシン・ピリドキサール・ピリドキサミン(ビタミンB6)→ピリドキサールリン酸(PLP)、パントテン酸→補酵素A、ビオチン→カルボキシラーゼに共有結合、葉酸→テトラヒドロ葉酸(FH4またはTHF)、コバラミン(ビタミンB12類)→コバミド補酵素がある。
補欠分子族のなかには補酵素とは区別されるものがある。たとえば、カタラーゼの補欠分子団はフェリプロトポルフィリンであるが、補酵素ではない。また、活性化のためには金属イオンを必要とする酵素もあり、これらの金属イオンは酵素または基質と結合して酵素の触媒作用を強める。このような金属イオンは活性化因子activatorではあるが、補酵素ではない。
補酵素は一般的には特異性があり、安定した小分子の非タンパク質性の有機化合物である。補酵素を必要とする反応には、酸化還元、基転移、異性体化、共有結合形成がある。分解反応では補酵素を必要としない。水素を転移する反応の補酵素には、NAD(ニコチンアミドアデニンジヌクレオチド)、NADP(ニコチンアミドアデニンジヌクレオチドリン酸)、FMN(フラビンモノヌクレオチド)、FAD(フラビンアデニンジヌクレオチド)、リポ酸、補酵素Q(ユビキノン)があり、水素以外の基を転移する反応の補酵素としては、リン糖質、補酵素A、チアミンピロリン酸、ピリドキサールリン酸、葉酸補酵素、ビオチン、コバミド補酵素、リポ酸がある。
補酵素を必要とする酵素反応の特徴としては、第一に基質におこる変化の裏返しの変化が補酵素におこることである。たとえば、酸化還元反応では基質が酸化されると補酵素が還元される。アミノ基転移反応の一つであるアラニンからピルビン酸への反応では、アミノ基はピリドキサールに転移されてピリドキサミンとなる。また、α(アルファ)-ケトグルタル酸からグルタミン酸への反応では、ピリドキサミンのアミノ基が転移されてピリドキサールとなる。
生理学的には、基質の反応が重要ではなく、補酵素の変化が重要なものがある。たとえば、筋肉の運動によって嫌気的にピルビン酸が乳酸となる反応で重要なのは、これらの基質ではなくて、NADH(還元型NAD)がNADとなる反応である。NADが生成されなくなると、解糖が行われなくなってATP(アデノシン三リン酸)の生成が止まる。すなわち、嫌気的条件では、ピルビン酸が還元されて乳酸となる反応でNADHが再酸化され、ATPの合成が行われる。
なお、補酵素の構造上の特徴としては、D-リボースアデノシンリン酸をもつものが多いことがある。
[有馬暉勝・有馬太郎・竹内多美代]
『稲田祐二・和田博編『タンパク質ハイブリッド第3巻 化学修飾最前線』(1990・共立出版)』▽『島原健三著『概説 生物化学』(1991・三共出版)』▽『西沢一俊・志村憲助編『新・入門酵素化学』改訂第2版(1995・南江堂)』▽『小宮山真・八代盛夫著、井上晴夫・北森武彦・高木克彦・平野真一編『生命化学1 天然酵素と人工酵素』(1996・丸善)』▽『飯田隆著、南原利夫監修『ライフサイエンス有機化学――立体化学・生体分子・物質代謝』(2000・共立出版)』▽『中島邦夫・柏俣重夫・樋廻博重著『新生化学入門』第5版(2002・南山堂)』▽『三輪一智・中恵一著『人体の構造と機能2 生化学』第11版(2005・医学書院)』
改訂新版 世界大百科事典 「補酵素」の意味・わかりやすい解説
補酵素 (ほこうそ)
coenzyme
助酵素,コエンザイムとも呼ばれる。酵素の活性発現のためには,タンパク質以外の分子が,可逆的にタンパク質成分に結合することが必要条件とされるものが少なくない。それらの分子を補欠分子族prosthetic group,または配合団と呼ぶが,金属原子,各種の無機アニオン,カチオンなどを除き,有機分子として作用するものを補酵素と呼ぶ。補酵素を解離させた残りのタンパク質部分をアポ酵素apoenzyme,アポ酵素に補酵素が結合したものをホロ酵素holoenzymeと呼ぶ。以下に代表的補酵素について述べるが,その多くはビタミンに属する。
(1)ニコチン酸の誘導体 NAD⁺(ニコチンアミドアデニンジヌクレオチド),NADP⁺(ニコチンアミドアデニンジヌクレオチドリン酸),および両者の還元型であるNADHとNADPHは生物界に広く分布し,乳酸脱水素酵素反応をはじめ,各種の酸化還元反応に関与する酵素の補酵素となる。NAD⁺の還元は次式のように立体特異的な反応として進行するが,この種のビタミンの欠乏はペラグラpellagraの原因となる。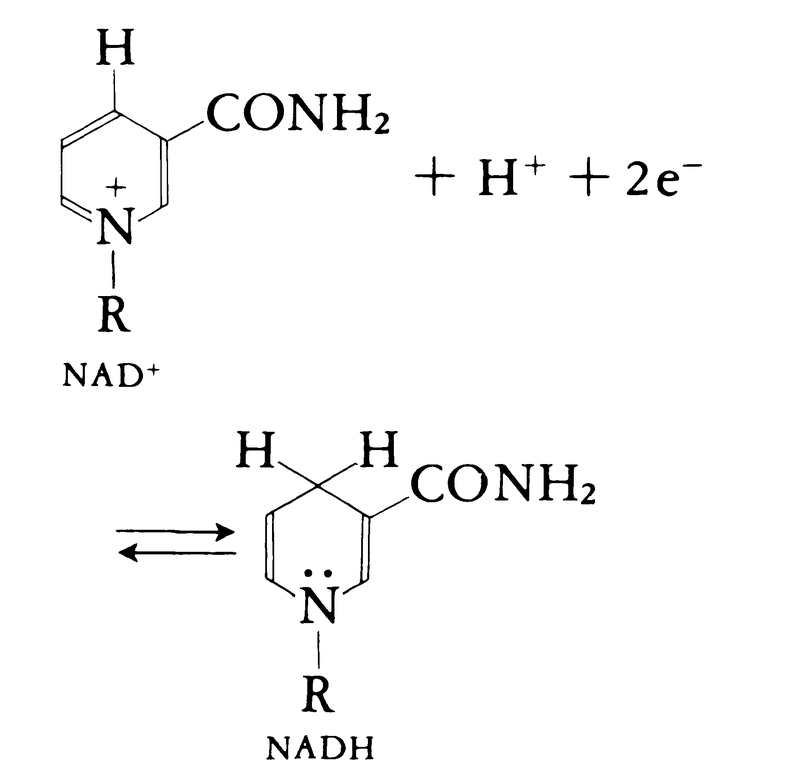
NAD⁺,NADP⁺の還元型すなわちNADH,NADPHは340nmに特異的な吸収極大を示すので,これを指標とする酵素活性の測定が広く利用されている。
(2)フラビンの誘導体 FMN(フラビンモノヌクレオチド),FAD(フラビンアデニンジヌクレオチド)もD-アミノ酸酸化酵素など各種の酸化還元酵素の補酵素としてよく知られているが,黄色いビタミンとして知られるビタミンB2,すなわちリボフラビンの誘導体に相当する。欠乏症としては口角炎,舌炎など,皮膚障害をひき起こす例が少なくない。
(3)チアミンピロリン酸thiamine pyrophosphate TPPと略される。ビタミンB1,すなわちチアミンのピロリン酸塩として解糖系代謝からクエン酸回路に入る接点でピルビン酸の酸化的脱炭酸反応に関与するなど,糖質代謝に重要な補酵素である。欠乏症は脚気,多発性神経炎が有名。
(4)コエンザイムA(補酵素Aともいい,CoAと略記) アデノシン-3′-リン酸,システアミン,パントテン酸の三つの部分が連結した化合物でアシル基の転移反応などに関与する。初めカプランN.O.KaplanとリップマンF.Lipmannが1947年に酵素的アセチル化反応に必要な耐熱性の活性酢酸として発見した物質。脂肪酸酸化,脂肪酸合成,ステロイド合成,ピルビン酸酸化,アミノ酸代謝,各種アセチル化反応に重要。分子内のSH基が生理活性の中心。
(5)ビオチンbiotin ビタミンHともいう。炭酸固定反応の補酵素として知られ,脂質と糖質の代謝に重要。アビジンと呼ばれるタンパク質が特異的に,しかも強くビオチンに結合し,ビオチン酵素を失活させる。ビオチンへの炭酸固定の部位については,かつて論争があったが,現在では下記の機作が受け入れられている。例えば,ピルビン酸カルボキシラーゼにおいては,ビオチンのカルボキシル基は酵素タンパク質のリシン残基のε-アミノ基に図1のようにアミド結合している。ピルビン酸のカルボキシル化は次の2段階で進行する。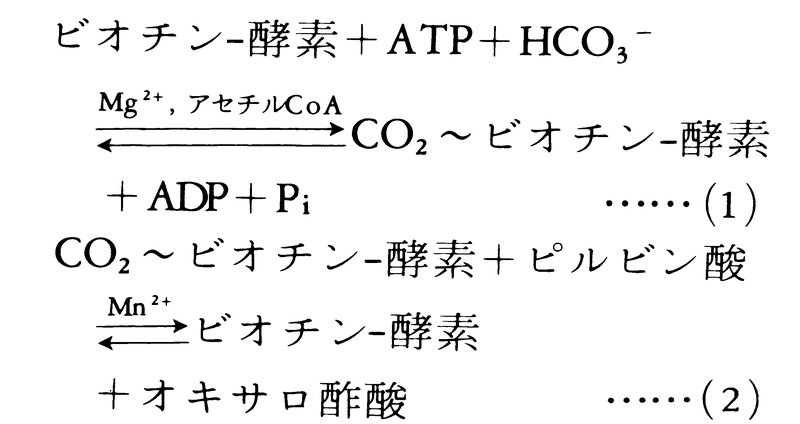
なお,カルボキシビオチン-酵素中間体において,カルボキシル基は次式のようにビオチン環の1位の窒素原子に結合する。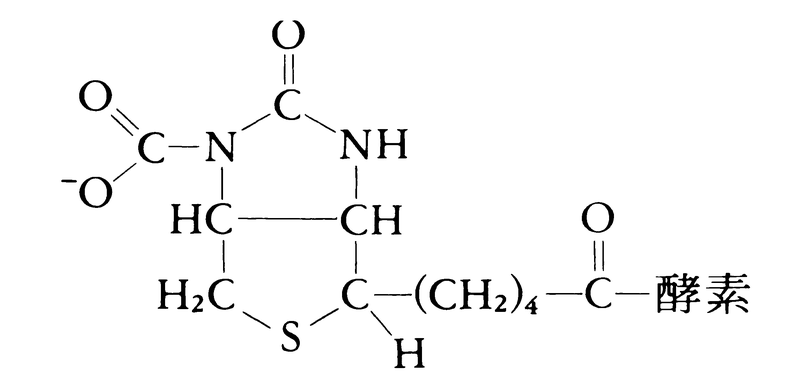
(6)ピリドキサルリン酸pyridoxal phosphate ビタミンB6のリン酸エステルとして,アスパルテートアミノ基転移酵素をはじめ,各種のアミノ酸代謝関連酵素の補酵素として重要。ピリジン環の4位のアルデヒド基がアミノ酸のアミノ基と図2のように,シッフ塩基を形成して,アミノ基転移,脱炭酸,異性化,脱アミノなどの各反応が進行する。ホロ酵素は分子内でリシン残基のε-アミノ基とシッフ塩基を形成しており,400~450nm付近に吸収極大を示す。
なおグリコーゲンホスホリラーゼに結合しているピリドキサルリン酸は,補酵素としての役割が上記とまったく異なり,リン酸基が基質としてのグリコーゲン分子の分解に関与すると理解されている。
(7)その他 テトラピロールに鉄が配位したポルフィリンの誘導体としてのヘムは各種酸化還元酵素の補酵素として,またユビキノンubiquinone,すなわち補酵素Q(CoQと略記)も電子伝達系で重要。テトラヒドロ葉酸はホルミル基などのC1ユニットの転移に,ビタミンB12としてのコバミド補酵素cobamide coenzymeはH,Cその他の分子内転移をめぐる脂質,核酸代謝に(欠乏症としては貧血が有名),ATPはリン酸基転移に,S-アデノシルメチオニンはメチル基転移にというぐあいに,多くの補酵素が生体反応で重要な役割をになっている。
→ビタミン
執筆者:徳重 正信
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
百科事典マイペディア 「補酵素」の意味・わかりやすい解説
補酵素【ほこうそ】
→関連項目オキシゲナーゼ|酵素|脂肪酸|トランスアミナーゼ|ヌクレオチド|フラビン補酵素
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「補酵素」の意味・わかりやすい解説
補酵素
ほこうそ
coenzyme
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
化学辞典 第2版 「補酵素」の解説
補酵素
ホコウソ
coenzyme
助酵素,コエンザイムともいう.酵素が複合タンパク質で,非タンパク質部分が酵素の機能発現に重要な役割を果たす場合,この低分子物質をいう.タンパク質と補酵素とは可逆的に解離,会合する場合が多く,透析操作などによってタンパク質部分より容易に分離される.補酵素との共同作用により,酵素はさらに多種多様な機能を発現する.次表に補酵素の種類と関与する反応を示す.

出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
栄養・生化学辞典 「補酵素」の解説
補酵素
世界大百科事典(旧版)内の補酵素の言及
【酵素】より
…タンパク質だけから成る酵素に対して,活性発現に必要なタンパク質以外の成分を結合した分子をホロ酵素holoenzyme,ホロ酵素のタンパク質部分をアポ酵素apoenzymeと呼ぶ。補欠因子族の中には,ビタミンB1,B2,B6などの誘導体やATPのような有機物質も含まれており,これらをとくに補酵素coenzymeと呼ぶが,このほか,K+,Na+,Cl-,Ca2+などの陽イオン,陰イオン,金属イオンを要求する酵素も少なくない。 各種アミノ酸が酵素的に脱水縮合してペプチドが形成され,遺伝情報に従って一定の長さのポリペプチド鎖が合成されると,その中の各種アミノ酸残基の側鎖の相互作用により,α‐らせん,β‐シート,ランダムコイルなどの二次構造が形成される。…
【酵素】より
…酵素の主成分であるタンパク質は,各生物固有のDNAの遺伝情報に基づいて,約20種類のL型α‐アミノ酸がNH2末端から順次ペプチド結合によって連結されることによって合成されたポリペプチド鎖が,構成アミノ酸残基の側鎖間相互作用によって三次元の立体構造を形成することになるが,酵素タンパク質は他の構造タンパク質,たとえば筋肉タンパク質や膜タンパク質と異なり,分子の一隅に活性中心を備えている。酵素の中にはまた,タンパク質以外に,金属イオン,特定の有機化合物としての補酵素,無機陽イオン・陰イオンなどの非タンパク質性分子やイオンを,その活性発現や構造保持に必須とするものも少なくない。
[人類と酵素の出会い]
酵素が上記のような物質であることは,今日誰でもよく知っている。…
※「補酵素」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
新暦の 4月後半から 5月の,梅雨前に日本列島が大きな移動性高気圧に覆われたときの晴天。発現期間は短い。もともとは旧暦 5月が梅雨にあたることから,梅雨の晴れ間の意味で,梅雨晴れ(つゆばれ)とも呼ばれ...


