精選版 日本国語大辞典 「王水」の意味・読み・例文・類語
おう‐すいワウ‥【王水】
改訂新版 世界大百科事典 「王水」の意味・わかりやすい解説
王水 (おうすい)
aqua regia
濃硝酸と濃塩酸を混合した溶液。ふつうは濃硝酸1容と濃塩酸3容を混合したものをいう。硝酸は強力な酸化剤であり,不働態をつくるアルミニウム,鉄,クロムなどは別としてほとんどの金属を侵すが,金,白金,ロジウム,イリジウムなどの貴金属は溶かすことができない。この硝酸だけでは反応しない貴金属もこの溶液には溶解することから,錬金術師によってaqua regia(〈水の王〉の意)と名づけられた。溶液中では次式に示す平衡が成り立っており,生ずる遊離塩素および塩化ニトロシルNOClが有効な触媒となって金属と反応する。
4H3O⁺+3Cl⁻+NO3⇄NOCl+Cl2+6H2O
また塩化物イオンCl⁻の金属陽イオンに対する複雑な作用も重要である。加熱溶解をする場合は酸が失われていくので,還流冷却器をつけて反応させるほうがよい。また試料と長く反応させる必要がある場合は,水で倍に薄めて使うほうが効率がよい。これを希王水と呼ぶ。一般に王水処理で溶解した溶液は薄めても酸化力が残っているから,硫酸あるいは塩酸を加えながら熱して硝酸を追い出しておいたほうが,次に還元性の試薬を用いる場合などに操作がしやすい。なお,王水は分解しやすいので使用の都度つくったほうがよい。硝酸3容と塩酸1容の混液を逆王水という。
執筆者:漆山 秋雄
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「王水」の意味・わかりやすい解説
王水
おうすい
aqua regia
濃硝酸と濃塩酸との混合物の通称。普通のどんな酸にも溶けない金や白金のような貴金属をも溶かすのでこの名がある。普通は濃硝酸1容と濃塩酸3容を混合したものであるが、試料を熱するなどの必要がある場合には初めから2倍に薄めて使うこともあり、これを希王水という。また組成を逆にした濃硝酸3容と濃塩酸1容の混合物を逆王水とよび、たとえば黄鉄鉱中の硫黄(いおう)を酸化溶解して硫酸イオンにする場合などに用いられる。
王水の酸化作用は次の反応の平衡が右へ行くことによって生ずる発生期の塩素と塩化ニトロシルの反応性によるものであるとされている。

一般に王水で処理して溶かすと金属イオンはその金属の最高原子価を示すのであって、たとえば、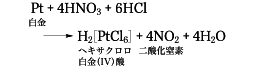
のようである。
[中原勝儼]
ブリタニカ国際大百科事典 小項目事典 「王水」の意味・わかりやすい解説
王水
おうすい
aqua regia
HNO3+3HCl→Cl2+NOCl+2H2O
王水は単独の硝酸,塩酸に溶けない金,白金などの貴金属を塩化物として溶解させる。また硫化物鉱石やテルル・セレン鉱物,鉛や銅の合金,種々の金属のヒ化物鉱石,亜鉛合金,ニッケル鉱,フェロタングステンなどの分析試料をよく溶解するので,化学分析における分解剤として重要である。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
化学辞典 第2版 「王水」の解説
王水
オウスイ
aqua regia
濃塩酸と濃硝酸とを体積比で3:1にまぜたもの.混合液中には,
HNO3 + 3HCl = Cl2 + NOCl + 2H2O
によってNOClと Cl2 を生じ,強い酸化剤となる.塩酸や硝酸のみでは溶けない金や白金も溶かす.塩酸と硝酸との体積比を1:3とした混合液は逆王水といわれ,黄鉄鉱中の硫黄分を硫酸に酸化する作用がある.王水はあまり安定でないので,使用時に調整する.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「王水」の意味・わかりやすい解説
王水【おうすい】
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「王水」の解説
王水
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

