精選版 日本国語大辞典 「製錬」の意味・読み・例文・類語
せい‐れん【製錬・製煉】
- 〘 名詞 〙 鉱石その他の原料から含有金属を抽出・精製し、金属材料の素材となる地金を作ること。冶金(やきん)。
- [初出の実例]「且鋳銕は〈略〉是製煉の間に之を石炭より得るなり」(出典:小学化学書(1874)〈文部省〉三)
日本大百科全書(ニッポニカ) 「製錬」の意味・わかりやすい解説
製錬
せいれん
金属元素を含んでいる岩石から目的金属を抽出し、金属塊や金属粉として生産する工程を製錬という。金属生産の目的で採掘した岩石(鉱石)には、目的金属を含む有価鉱物のほかに、脈石(みゃくせき)とよばれる無用鉱物も含まれている。そこで一般に製錬工程では、まず鉱石から脈石を除いて、目的金属の含有率ができるだけ高い鉱石部分(精鉱)を得るようにしている。この工程を選鉱という。精鉱を化学的に処理して目的金属を得る工程を抽出という。これが製錬工程の中心をなし、狭義の製錬はこの工程をさす。抽出した粗金属から不純物を除去する工程を金属精製という。
[原善四郎]
選鉱および鉱石処理
鉱物の色沢、比重、濡(ぬ)れ特性、磁性、誘導率などの性質が鉱物の種類によって異なることを利用して、各種の選鉱法がある。手選法、比重選鉱法、重液選鉱法、浮遊選鉱法、磁力選鉱法、静電選鉱法などである。鉱石中で有価鉱物と脈石は細かく入り混じっているから、両者がそれぞれ個別の粒子に分かれるまで鉱石を細分割しないと選鉱ができない。一般には、鉱石を各種の破砕、粉砕、磨砕機によってしだいに細分し、その各段階での鉱粒の粒度に応じた選鉱法で選鉱している。
選鉱で得た精鉱は、泥状ないし粉状である。次の抽出工程にかけやすくするため、付着水分除去のための乾燥、化合水分・気体分除去のための煆焼(かしょう)、化学成分を変化させる焙焼(ばいしょう)などの加熱処理を行う。粉鉱は団鉱法、ペレタイジング法、焼結法などの方法で塊化する。
[原善四郎]
精鉱からの金属抽出(狭義の製錬)
鉱物内の金属原子は普通、非金属原子と結合して酸化物、硫化物などの化合物を形成し、電気的には正の状態で存在している。その金属原子になんらかの方法で電子を与えて非金属原子との結合を解くとともに電気的に中性な金属状態にすること(広義の還元)が、鉱石からの金属抽出工程の基本をなしている。その際、金属原子との結合を解かれた非金属原子や鉱石中の脈石その他の随伴不用物質を目的金属から分離する操作も必要である。実際の金属製錬では、金属の種類、状態に応じて、次のような還元法が採用されている。(1)炭素質還元剤による還元法、(2)水素による還元法、(3)活性金属による還元法、(4)水溶液の電解還元および置換還元法、(5)溶融塩の電解還元法、などである。鉱石・金属が溶融するような高温で行う製錬を乾式製錬(乾式冶金(やきん))、常温付近で水溶液などの溶媒を用いて行う製錬を湿式製錬(湿式冶金)、電気を利用する製錬を電気製錬(電気冶金)という。
[原善四郎]
乾式製錬
乾式製錬には、以下(1)~(4)などの方法がある。
(1)炭素質還元剤を用いる溶融製錬 酸素との親和力があまり大きくない金属の酸化物は、高温で一酸化炭素や炭素と反応して金属に還元される。鉄、鉛、スズの製錬はこの原理によっている。鉄、スズは酸化鉱の赤鉄鉱Fe2O3、磁鉄鉱Fe3O4、褐鉄鉱Fe2O3・nH2O、錫石(すずいし)SnO2を、鉛は原鉱(方鉛鉱PbS)を焼結した酸化物を原料とし、コークスを燃料とした高炉(鉄)や溶鉱炉(鉛)、重油燃料の反射炉(鉛、スズ)や電気炉(スズ)で、コークスを還元剤として製錬する。脈石は添加溶剤とともに溶融スラグを形成して、還元された溶融粗金属から分離される。この場合の還元反応は一般的には次式で示される(Mが金属)。
MO+CO→M+CO2,
MO+C →M+CO
(2)マット濃縮による溶融製錬 銅、ニッケルの原鉱として重要な硫化鉱は、同伴金属を多量に含んでいるため、(1)の方法は適用できない。この場合は、まず同伴金属の硫化物の一部を酸化させて脈石とともにスラグとし、目的金属の硫化物は同伴金属の残存硫化物とともに溶融マット(鈹(かわ)、後述)を形成させてスラグから分離する。ついでマットを処理して粗金属を得る。これをマット溶融製錬法という。
実際には、黄銅鉱CuFeS2、硫鉄ニッケル鉱2FeS・NiSをそれぞれ、溶鉱炉、反射炉、電気炉、自溶炉などで溶融し、硫化鉄の一部は酸化しスラグとして排除し、目的金属は残存硫化鉄とともに溶融マットに濃縮してスラグから分離する。マット(銅マットCu2S・FeS1.08、ニッケルマットNi3S2・Cu2S・FeS)は転炉に移し、空気を吹き込んでまず硫化鉄を燃焼させ、生成する酸化鉄を添加ケイ酸とともにスラグとして排除する。
銅のマット製錬では、さらに空気吹き込みを続け、次式の反応で粗銅を得る。
Cu2S(融)+O2(気)
→2Cu(融)+SO2(気)
ニッケルのマット製錬では、転炉で硫化鉄を酸化し排除した段階の産物(濃鈹(のうひ))を、そのまま陽極に鋳込んで電解製錬するか、酸化焙焼・脱銅処理・再還元を行うかして粗ニッケルを得ている。
在来のマット生成炉(溶鉱炉、反射炉、電気炉)の熱源は、それぞれコークス、重油または天然ガス、電熱であったが、近年の自溶炉では、完全乾燥した精鉱粉を酸素富化空気ないし熱風とともに炉内に噴出して瞬間的に燃焼させることにより、硫化鉄の酸化発熱を十分に活用している。マット製錬法による製銅炉として、最近、マット生成から粗銅生成までの工程を連続的に行う連続製銅法が開発されている。
(3)揮発製錬法 蒸気圧の大きい金属の化合物は高温で分解あるいは還元によって金属蒸気となる。それを凝縮すれば金属が得られる。水銀、亜鉛、マグネシウムはこの原理で製錬される。水銀鉱石の辰砂(しんしゃ)HgSは空気中の加熱で硫黄(いおう)が酸化し、水銀蒸気が発生する。古くからこの原理で水銀が生産されていた。亜鉛鉱石の閃(せん)亜鉛鉱ZnSはまず焙焼して酸化亜鉛とする。ついでこれを木炭とともに素焼るつぼに装入・密封し、下方から加熱すると、亜鉛蒸気が発生し、るつぼ上部内面に金属亜鉛が凝縮する。中国では古くからこの方法で亜鉛を生産していた。現在は、溶鉱炉や電熱炉により同様の原理で蒸留亜鉛が生産されている。
(4)活性金属還元法 ウラン、チタンなどの酸素、炭素との親和力の大きい金属は炭素質による還元法では製錬できない。これらの金属は酸化物原鉱からいったんハロゲン化物をつくり、それをマグネシウムなどの活性金属で還元するという方法で製錬される。チタンの場合は、まず酸化チタン鉱に炭素質を加え、高温で塩素を作用させて生成する四塩化チタン(TiCl4、沸点136℃)の蒸気を脈石から分離し、凝縮させる。ついでアルゴンを満たした反応容器内の溶融マグネシウム層上に四塩化チタンを供給すると、次式により海綿状の金属チタンが生成する。
TiCl4(気) + 2Mg(融)
→Ti(固)+2MgCl2(融)
[原善四郎]
湿式製錬
湿式製錬では、鉱石中の目的金属を適当な溶媒(一般には水溶液、金・銀鉱のアマルガム製錬法では水銀)で溶かし出し(浸出という)、浸出液中の金属イオンを電解還元や置換還元法で金属に還元する。あるいは浸出液から目的金属の純化合物を晶出、沈殿させ、ふたたびなんらかの還元処理で金属を得る。浸出には、鉱石の種類により、水、酸、アルカリなど各種の溶媒が、常温・常圧から加温・加圧まで各種の操作条件で使用される。浸出操作後、浸出液と不溶解残滓(ざんし)の分離、浸出液から不純物の分離(浄化)、浸出液中の金属イオンの濃縮、浸出液からの目的金属ないし目的金属化合物の採取などの操作が必要である。湿式製錬のいくつかの例を次に示す。
(1)金・銀の湿式製錬 主要な金鉱石であるケイ酸質脈状鉱石(輝銀鉱Ag2Sも含む)は磨砕して泥化し、シアン化ソーダ希薄水溶液で金・銀を浸出する。浸出液に亜鉛末を加え、置換反応で金・銀を析出・沈殿させ、沈殿物を溶融して金・銀合金の粗金属を得る。
(2)銅、亜鉛、カドミウムの湿式製錬 銅酸化鉱、亜鉛硫化鉱の焙焼鉱は、硫酸でそれぞれ金属を浸出し、浸出液(硫酸塩水溶液)から銅、亜鉛をそれぞれ電解採取する。亜鉛原鉱中に随伴するカドミウムは、浄液工程で亜鉛浸出液に亜鉛粉末を加えることにより金属カドミウムとして置換・析出するので、これを分離・捕集し、亜鉛の湿式製錬法と同様の方法により精製する。
(3)ニッケルの湿式製錬 硫化鉱からはアンモニアと加圧空気で、酸化鉱からは硫酸で、それぞれ加温・加圧下でニッケルを浸出する方法が実用されている。浸出液に加温・加圧条件下で水素を吹き込み、その還元作用で金属ニッケル粉を採取している。
(4)アルミニウムの湿式製錬 代表的なアルミニウム鉱石であるボーキサイトには、加温・加圧下でカ性ソーダ水溶液を作用させ、アルミニウムをアルミン酸ナトリウムとして浸出する。浸出液は不溶解残滓(赤泥)を分離したのち、加水分解して高純度アルミナとする。このアルミナを溶融塩電解(後述)して金属アルミニウムを生産する。
(5)ウランの湿式製錬 ウランの主要鉱石である瀝青(れきせい)ウラン鉱U3O8は硫酸によってウランを浸出する。浸出液はイオン交換法や有機溶媒抽出法によってウランを濃縮したのち、アルカリを加えて重ウラン酸塩として沈殿させる(その乾燥物がイエローケーキ)。イエローケーキはふたたび酸溶解有機溶媒抽出法によって精製し、純酸化ウランやフッ化ウランに変える。金属ウランはフッ化ウランを金属マグネシウムで還元して生産する。
[原善四郎]
電気製錬
電気は電熱として乾式製錬の熱源に利用されるが、電解還元法は重要な金属製錬法である。金属表面で電解浴との電子の授受反応が生ずる平衡単極電位は、金属によって異なる。一定条件下の標準単極電位によって金属につけた順位を電位列とよぶ。溶解しやすく析出しにくい金属(正イオンになりやすい金属)は標準単極電位が低く、卑な金属とよばれる。電位列で水素よりも著しく卑な金属(ナトリウム、マグネシウム、アルミニウム)の金属塩水溶液を電解すると、陰極で水素イオンから水素への還元が生じて金属の還元析出は生じない。これらの金属の電解は溶融塩電解によらざるをえない。ただし、実際に電流が流れている状態での陰極における水素析出電位は、標準単極電位よりも著しく低くなり、電位列で水素以下マンガンまでの金属の陰極析出電位よりも低くなるため、これらの金属も水溶液電解が可能である。
不溶性陽極を用いて電解浴から陰極に金属を析出・採取する方法を電解採取といい、湿式製錬における金属浸出液からの金属採取に利用される。銅、亜鉛の湿式製錬がその例で、この場合、陽極には鉛合金を用いる。電解採取の廃液(硫酸)は、鉱石からの金属浸出に繰り返し使用する。
溶解塩電解の代表例はアルミナを原料とするアルミニウムの電解である。アルミナを溶解させた溶融氷晶石Na3AlF6を電解浴とし、黒鉛を電極とする。
[原善四郎]
粗金属からの金属精錬
粗金属を実用に十分な純度にまで精製する操作を精錬という。精製法は、電解精製と乾式精製とに大別される。
[阿座上竹四]
電解精製
粗金属を陽極とし、純金属を陰極として適当な電解質溶液中で電解すると、陽極から目的金属が溶け出し、陰極面上に析出する。不純物のうち、目的金属より電気化学的に貴な元素は陽極から溶け出さずに残留し、目的金属より卑な元素はいっしょに溶け出すものの陰極には析出せず、電解液中に残って、いずれも分離される。銅、鉛、金、銀などはこの方法で精製されている。溶出と析出は逆反応であるため、電力消費は理論的にはゼロであるが、種々の電気抵抗や副反応のため少量の電力を消費する。
[阿座上竹四]
乾式精製
目的金属と不純物の間の物理的・化学的性質の差を利用した多くの方法が実用されている。
(1)酸素・硫黄・塩素などによる精製 たとえば転炉中で銑鉄に酸素を吹き込んでシリコンや炭素を酸化し、鋼に精製するように、不純物がより化合しやすいガスや元素を加えて反応除去する方法で、もっとも広く行われる。
(2)蒸留による精製 不純物との沸点の差を用いる精製法で、石油の分留と同じ原理による。純度98%の粗亜鉛はこの方法で99.99%の最純亜鉛に精製される。
(3)第三金属の添加による精製 金・銀を含む鉛に亜鉛を加えると、金・銀は亜鉛と化合物をつくって表面に浮き上がる。鉛中の銅を分離するのにアルミニウムを加えるのも同じ原理によるものである。
(4)溶解度差を利用する精製 亜鉛中の鉛は、溶融亜鉛の温度を下げると鉛を多く含む別相をつくって沈降するので、これを分離することができる。これは二つの相の間の溶解度差を利用する方法で、超高純度の電子材料をつくるのに用いるゾーン精製法もこの一種である。
(5)熱解離を利用する精製 粗アルミニウムに三塩化アルミニウムガスを高温で作用させると、一塩化アルミニウムガスを生ずる。これを低温のコンデンサーに導くとふたたび三塩化アルミニウムガスに戻り、純アルミニウムを分離析出する。この種の反応を不均化disproportionation反応とよぶ。
[阿座上竹四]
改訂新版 世界大百科事典 「製錬」の意味・わかりやすい解説
製錬 (せいれん)
extractive metallurgy
鉱石その他の原料から金属を採取,精製して地金(じがね)(金属材料の素材)を作ることをいう。地金以外に合金,純粋な化合物として採取することもある。製錬技術の目的は原料中の有価成分を他の共存物質から分離,濃縮することにあり,原料の組成,産出形態,製品地金の純度,製品形態に応じてさまざまな技術が適用される。
製錬原料
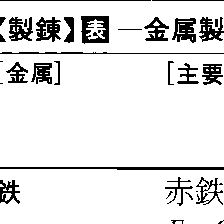
金属は有機材料と異なり,合成ができないので,もともと金属元素を含む資源から採取される。天然に産出する鉱産資源のなかで目的金属を経済的に抽出,採取できるものが鉱石と呼ばれて製錬原料のおもなものとなる。鉱山から採取された状態の鉱石は粗鉱と呼ばれ,目的金属の鉱物のほかに他の有用金属の鉱物や無価値の鉱物を随伴している。自然に産出する鉱物の化学結合の形を変化させないで目的金属分を分離濃縮することを選鉱という。選鉱したのちに製錬の直接対象となる鉱石を精鉱と呼んでいる。鉱石中に含まれる鉱物および原鉱石の品位(金属含有量の重量%)の代表的な値を表に示す。鉄,アルミニウム,チタンなどは酸化物の形で天然に産出し,特別の選鉱手段を経ないで製錬される。クロムは重い鉱物であるクロム鉄鉱として産出するので比重選鉱で選別される。銅,亜鉛,モリブデンなどは原鉱品位は低いが,浮遊選鉱で品位向上が図られる。ウランは直接湿式製錬によって酸浸出し,溶媒抽出法またはイオン交換樹脂法によって精製ののち純酸化物U3O8(イェローケーキ)として回収される。製錬原料として独自の鉱石ではなく,他の金属の製錬廃滓が用いられ,副産物として回収されるものも多い。日本では金,銀はおもに銅製錬,鉛製錬の副産物として生産される。また工場内で発生する屑や市中から回収される廃棄物中の金属分なども原料として利用されている。
製錬の原理
金属の融体,酸化物の混合融体(スラグ),硫化物の混合融体(マット),ヒ化物の混合融体(スパイス),気相蒸気のように化学結合の様式の異なる相は互いに混じり合わない。また,それぞれの相で金属成分の溶解度に差がある。互いに混じり合わない二つの相の間でのそれぞれの金属に特有の分配の差を利用して分離するのが基本原理である。この分配は酸化還元の強さ,混合融体の成分,温度などによって大きく変化する。
製錬方式
(1)直接製錬と間接製錬 精鉱から金属を取り出す際に,焙焼(ばいしよう)によって原料中の金属の化合物の形を変えたり,マットのような中間産物にして,いったん金属分を濃縮するような方式を間接製錬という。これに対し精鉱から1段階のプロセスで金属を得る方法を直接製錬と呼んでいる。直接製錬は工程数が少ないので,製錬プロセスの省エネルギー化,省力化の可能性を秘めており,現行製錬法の技術革新のために広く研究の対象となっているが,プロセス制御の困難,製品歩留り(原料中に含まれた金属分のうち製品として採取できた量の割合)の低下,製品純度の低下などの欠点の克服が通常難しい問題となる。工業生産される金属では間接製錬が普通で,一次製錬(粗製錬,目的金属の濃縮)と二次製錬(精製,純金属の製造)などの2段階以上のプロセスで組み立てる。
(2)乾式製錬と湿式製錬 水溶液を利用した製錬法を湿式製錬,水溶液を用いないで,高温化学反応を利用した製錬方式を乾式製錬と呼ぶ。
(3)還元製錬 鉱石を還元して目的金属を得る方法。銅,水銀など特殊なものを除いて大部分の金属は化合物を還元して金属を得る。このため製錬と還元とがほぼ同義の言葉として用いられることもあるが,これは区別しておくほうがよい。還元製錬で最も多く用いられるのは,炭素(コークス)を還元剤とする還元法で,炭素と酸化物が直接反応する場合を直接還元,一酸化炭素COが還元剤となる場合を間接還元という。間接還元で生じた二酸化炭素CO2は,炭素と反応して再び一酸化炭素に戻り還元力が回復する。化学量論上の還元剤は炭素であるが,還元作用は一酸化炭素の仲介で起こるという意味で間接還元という。溶鉱炉を使う還元製錬では直接還元と間接還元はどちらも寄与するが,間接還元の可能性のない金属酸化物の製錬に溶鉱炉は用いない。
(4)酸化製錬 原料鉱物中の不純物を酸化除去する場合,たとえば黄銅鉱CuFeS2中の鉄と硫黄を酸化して除くと銅が金属の形で残るという場合と,いったん還元によって金属を製造したあとで,共存混入している不純物を選択的に酸化除去する場合(二次製錬)を酸化製錬という。
(5)揮発製錬 金属を蒸気の形でいったん気相に分離したのち凝縮させる方法。水銀,亜鉛(乾式製錬),マグネシウム(ピジョン法--フェロシリコンによる還元揮発)などに用いられる。粗亜鉛中の鉛とカドミウムの分離には蒸留精製も行われる。
(6)真空製錬 減圧下での揮発製錬を真空製錬と呼ぶことがある。金属中のガス成分や不純物を気相に分離除去する方法も含まれる。
(7)電熱製錬 炭素を熱源としては使わずに単なる化学的還元剤(酸化物中の酸素の受取り役)としてだけ利用し,反応に必要なエネルギーは電熱により供給する方式の製錬。直接還元によるフェロアロイの電気炉による製造や亜鉛の電熱蒸留がこの例である。
(8)電解製錬 溶融塩もしくは水溶液という電解質溶液を利用して,イオンとして溶解している金属を電気化学的に還元する方法。金属塩の形で精製した原料を電解質溶液に溶解して金属に還元する電解採取と,一方の電極で粗金属を溶解させ,一方の電極で純金属を製造する電解精製とがある。電解精製では電解質溶液は単なる反応媒体で,不純物の分離の働きをする。溶融塩電解採取では,アルミニウム,ナトリウム,カルシウム,マグネシウムなどが製造される。水溶液電解採取では,亜鉛,クロム,マンガン,ニッケル,コバルトなどが製造される。水溶液電解精製は金,銀,銅,鉛,スズなどの製錬に利用される。
(9)塩化製錬 中間産物として塩化物を経由する方法で,間接製錬の一種。チタンの製錬では,原料の二酸化チタンTiO2を炭素と塩素を用いて四塩化チタンTiCl4にしたのち,マグネシウムあるいはナトリウムによって還元する。特殊なものに塩化焙焼があり,製鉄原料の脱銅などに利用されている。塩化物以外のハロゲン化物としてはウランの製錬でフッ化物が使われている。これは,四フッ化ウランUF4が吸湿性が少ないことと,六フッ化ウランUF6の蒸気がウランの同位体分離濃縮(天然ウラン中に0.72%含まれる核分裂物質235Uを主成分238Uと分離する)にとって好都合な物質(UF6の沸点が低く,フッ素は天然には100%19Fである)であることとによる。
→冶金
執筆者:増子 昇
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
百科事典マイペディア 「製錬」の意味・わかりやすい解説
製錬【せいれん】
→関連項目鉱業|鉱山|鉱石|粗鉱|品位|冶金
出典 株式会社平凡社百科事典マイペディアについて 情報
最新 地学事典 「製錬」の解説
せいれん
製錬
smelting ,refining
鉱石から目的金属を抽出する操作。鉱石・精鉱等を原料とし,炉を用いて酸化還元反応で粗金属・高純度金属を得る乾式製錬(smelting),原料を溶解し電解採取,または乾式製錬で得られた粗金属を電解精製する湿式製錬(refining)がある。乾式製錬のうち,高純度化を目的とする工程を精錬(refining)と呼ぶこともある。
執筆者:稲垣 勝彦
出典 平凡社「最新 地学事典」最新 地学事典について 情報
ブリタニカ国際大百科事典 小項目事典 「製錬」の意味・わかりやすい解説
製錬
せいれん
「金属の製錬」のページをご覧ください。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...