触媒(読み)ショクバイ(その他表記)catalyst
精選版 日本国語大辞典 「触媒」の意味・読み・例文・類語
しょく‐ばい【触媒】
改訂新版 世界大百科事典 「触媒」の意味・わかりやすい解説
触媒 (しょくばい)
catalyst
catalyser
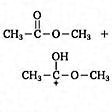
熱力学的には進行可能であるけれども,遅いある特定の化学変化の反応速度を,少量の添加によって,著しく増大させることのできる物質。反応の前後でそれ自体に変化はなく,また反応の平衡に影響を与えないと考えてよい。たとえば白金黒を入れた容器で水素と酸素を混ぜ合わせると,激しく反応して水が生成する。また,酢酸メチルの水溶液に少量の塩酸(水素イオン)を加えると,加水分解反応が容易に進み酢酸とメチルアルコールになる。反応速度は白金黒と水素イオンの存在しない場合に比べそれぞれ著しく増大しており,反応終了後の白金黒と水素イオンの状態はもとのままである。触媒が白金黒のような固体物質で,反応する物質が水素と酸素のような気体である場合,不均一触媒反応という。塩酸と酢酸メチル水溶液のように同じ溶液相になるときは,均一触媒反応と呼ばれる。塩酸の添加量が少なければ,酢酸メチル加水分解反応と酢酸-メチルアルコールエステル化反応の平衡関係はほとんど影響を受けない。
一般に触媒は反応を促進させるが,なかには遅らせるものもあり,とくに前者を正触媒,後者を負触媒ということがある。また,触媒成分に少量の違う物質を添加し,活性をさらに増大させる助触媒(促進剤ともいう)としては,アンモニア合成用の鉄触媒におけるアルミナやカリウムの例が挙げられる。逆に,少量の添加物質のために活性が著しく低下する,水素化触媒反応における硫黄化合物のような例も数多く知られ,触媒毒と呼ばれる。なお,水素化触媒の活性成分である白金は,一般に表面積の大きいアルミナや活性炭に担持して用いられる。この場合のアルミナや活性炭は担体と呼ばれ,細孔の存在がとくに重要と考えられている。
触媒の作用機構
白金黒の表面に吸着した水素や酸素は,分子のままでなく原子(HとO)に解離しており,容易に表面上で水分子を生成し脱離していくと考えられている。鉄触媒上で,水素と窒素からアンモニアを生成する反応においても,まずそれぞれの分子が解離して吸着し,逐次NH,NH2,NH3が生成し,アンモニア分子の脱離にいたるとされている。このような反応経路をとる場合,最も遅い反応素過程の速度によって全反応の速度が律せられる(律速段階)。
液相均一触媒反応における水素イオンと同様の役割を,固体であって酸性を示す物質の表面が果たすことがあり,固体酸触媒と呼ばれる。酸化ケイ素と酸化アルミニウムの混合ゲルにあたるシリカ-アルミナや,両者が特徴ある結晶構造をとるため反応分子を固体内部にとり込むことのできるゼオライトは,その代表例である。カルボニウムイオン中間体の生成が反応進行上の鍵となる。
一方,ヨウ化水素を助触媒とするロジウム錯体には,酢酸溶液中メチルアルコールと一酸化炭素を反応させ酢酸を合成する触媒作用がある。溶液中に平衡的に生じるヨウ化メチルがロジウム錯体に解離付加(酸化的付加という)し,別に配位した一酸化炭素がメチル配位子と反応(配位子挿入という)してアセチル配位子になり,それがヨウ化物イオンとともに脱離(還元的脱離という)し,加水分解を受けてヨウ化水素を再生するとともに酢酸を生成するという,触媒反応サイクルを構成している。触媒反応の機構は多くの場合複雑で,よくわかっていない場合が少なくない。
ベルセリウスの命名
スウェーデンの化学者J.J.ベルセリウスが1836年,そのような働きをする物質に注目し,ギリシア語のkatalysis(原義はもつれ,結び目などを解く,ゆるめること)から命名した。すでに古くから糖を原料とするアルコール発酵やアルコールの酢酸発酵が行われ,18世紀前半にはリネン漂白のための鉛室式硫酸製造が始まっていたが,さらに酸によるデンプンの糖化が見いだされ(1781),イギリスのH.デービーにより加熱白金線による発火点以下での水素,一酸化炭素,エチレン,アルコール,エーテルなどの燃焼に関する公開実験がロンドンのローヤル・インスティチューションで行われ(1817),また塩素酸カリウムからの酸素発生反応における二酸化マンガンの促進効果,エチルアルコールからエーテルを得る脱水反応における硫酸添加効果など,注目に値するこの種の現象が多く見いだされるようになった。当時化学界の大御所であったベルセリウスは,通常の化学親和力によらないそれらの現象に興味を抱き,化学反応をひき起こす新しい概念として,この考えを提起したのであった。〈反応空間中にあって,しかも反応の前後で化学的に不変な物質により進行する場合,これを触媒反応と呼ぶ〉というのが,命名にあたっての彼の定義である。しかし,やや神秘的な〈触媒力〉の作用と考えたため,J.vonリービヒやL.パスツールはじめ,多くの化学者の批判を受けることとなった。
オストワルトの定義
19世紀の後半は物理化学の黎明期であった。ショ糖の転化速度を旋光度の変化から追跡し,速度がショ糖濃度に比例することを示した研究(1850)や,エチルアルコールと酢酸との酢酸エチルエステル生成平衡の研究(1862),あるいは化学平衡に熱力学を応用したJ.H.ファント・ホフやJ.W.ギブズの貢献によって,触媒の働きでは平衡値以上に反応を進行させえないという認識が,しだいに一般的になった。1900年,F.W.オストワルトは触媒を次のように定義した。〈触媒は化学反応において,化学平衡を変えることなく,ある方向の反応速度を速めたり遅くする作用を示し,触媒自身は反応の前後で見かけ上なんの変化も示さない。この場合,反応速度を速めるものを正触媒,逆に遅くするものを負触媒という〉。この定義は現在も受けつがれている。しかし,いくつかのコメントが新しい観点から付け加えられてきた。鍵となる用語とともに列挙すると,触媒作用の重要性は反応の速さばかりでなく反応の経路をも変えるところにある(選択性),反応の前後で触媒自身がまったく変化しないわけではない(触媒寿命),触媒の特質は反応過程にくり返し関与し再生されつつ,反応進行を速めるところにある(触媒反応サイクル)。
オストワルトはまた,白金存在下でアンモニアを空気酸化する硝酸製造法を発明した。同じころP.サバティエは,還元ニッケルが不飽和炭化水素の水素化活性をもつことを見いだし,硬化油製造工業の道を開いた。また,窒素酸化物を触媒とし二酸化硫黄を酸化する鉛室式硫酸製造法は,白金触媒法に代わった。
アンモニア合成と触媒
触媒の働きが世界に衝撃的な影響を及ぼしたのは,20世紀初頭のアンモニア合成であった。とくに前世紀末,食糧不足問題が強く叫ばれ,窒素肥料の供給不足を空中窒素の固定により解決しようと,多くの化学者が研究に取り組んでいた。石灰窒素(シアン化カルシウムと炭素の混合物)法が工業化され(1905),チリ硝石(天然硝酸ナトリウム)の枯渇に備えるなどの動きがあったころである。F.ハーバーは1909年ついに,空気中の窒素を原料に,触媒を用いてアンモニアの連続合成実験に成功した。彼はアンモニア合成反応が平衡上高圧であるほど有利になることをよく認識していた。また,生成するアンモニア濃度が低くても,低温高圧下で液化しやすい性質を利用すれば,生成するアンモニアを液体で連続的に取り出し残りの気体を循環させることによって,反応を有利に進めうる点にも気づいていた。そして十分活性の高い金属オスミウム粉末をようやく手にすることができたのであった。このときすでにハーバーはBASF(バスフ)社と協同研究体制に入っていた。工業化の研究は同社が担当し,高圧反応装置はK.ボッシュ,触媒はミタシュP.A.Mittaschが開発することとなった。高活性のアンモニア合成触媒--鉄-アルミナ-酸化カリウム系--が見いだされ,日産10tの生産が始まったのは13年のことであった。この組成は,現行の実用触媒と基本的に同じである。しかも,同社は高圧技術と触媒研究の蓄積のなかから,酸化亜鉛-酸化クロム触媒を用いてメタノール合成工業も生み出した。
触媒が化学工業プロセスの中枢となる例はつぎつぎに現れた。メチルアルコール合成法と同じく水素と一酸化炭素を原料としながら,液体燃料製造を主眼とするフィッシャー=トロプシュ反応のコバルトまたは鉄触媒,硫酸製造触媒としての白金を代替し,無水フタル酸や無水マレイン酸を得る選択酸化触媒としての五酸化バナジウム,ニッケルとアルミニウムの合金を水酸化ナトリウムで処理し,アルミニウムを溶出させて微粉末のニッケルを得,温和な条件で医薬原料や食品などの製造に使われるラネー・ニッケル触媒,オレフィンから液体重合体を得る固体リン酸触媒,オレフィン,一酸化炭素,水素から高級アルコールなどをつくるオキソ法コバルト触媒などがその例である。
石油精製・石油化学と触媒
第2次大戦後は石油を主軸に大展開があった。まず,石油精製プロセスが,常圧蒸留,減圧蒸留などの単なる物理操作から,触媒反応を縦横に駆使した化学プロセスに拡大された。とくに,触媒を気流中で流動できる微粒子の形で用い,軽油を接触分解する反応器と,触媒上に析出する炭素質を空気で燃焼除去する再生器の間を触媒が循環することによって,大規模連続生産を行う流動床式触媒反応装置の開発は,化学工学的に注目される成果でもあった。触媒自体についても,第2次大戦中に航空ガソリンやトルエンの製造のため,石油のナフサ留分をアルミナ担持酸化モリブデン触媒で反応させていたものが,プラットフォーミング法と呼ばれるアルミナ担持白金触媒に代わり(1949),さらにレニフォーミング法と呼ばれるアルミナ担持白金-レニウムバイメタリック触媒へと改良が進んだ(1967)。レニウムの添加により白金の高分散状態が安定に維持され,また炭素質の析出が少ないので水素分圧を低めることができ,芳香族生成に有利のうえ,水素化分解を抑える結果,改質油の収率が増えるといわれている。
重質油を原料とする接触分解反応の触媒は最初は酸性白土が用いられたが,無定形の合成シリカ-アルミナに代わった。アルミニウムイオンに由来する固体酸触媒が原料中に含まれるオレフィンをカルボニウムイオンに変え,オクタン価の高いガソリンを生成する。触媒はその後ゼオライトの出現(1960)で一変した。ゼオライトは定まった形の細孔が規則正しく配列しているという特徴があり,イオン交換により触媒機能を向上させることが可能なうえ,形状選択性(反応する分子と反応しない分子を選ぶ性質と,生成する分子の形を選ぶ性質がある)があるので,大きな期待がかけられている。接触分解用には希土類でイオン交換したゼオライトが使用される。重油中の硫黄分を少なくする水素化脱硫反応あるいは石油精製化学プロセスとしての水素化精製反応には,アルミナ担持のモリブデン-コバルト系触媒が使われる。硫化モリブデン自体に水素化触媒活性のあることが重要である。石油化学製品はその多くが触媒反応の所産である。エチレンから酸化エチレンをつくる銀触媒,プロピレンをアンモニアとともに酸化してアクリロニトリルを得るソハイオ法や,種々の選択酸化反応に使われるモリブデン-ビスマス-アンチモン-鉄などの複合酸化物触媒,液相でp-キシレンから臭化物を助触媒にテレフタル酸を合成する酢酸コバルト触媒など,枚挙にいとまがない。
ところで,第2次大戦後の最も画期的な触媒開発と考えられるのは,K.チーグラーとナッタGuilio Natta(1903-79)による,立体規則的オレフィン重合反応であろう。これにより立体規則性ポリプロピレンがつくられ,広い用途に使われるようになった(〈チーグラー触媒〉の項参照)。三塩化チタンと有機アルミニウム化合物からなるこの触媒の配位重合活性は,有機金属錯体に関する広い関心を呼び起こし,種々の錯体触媒が生み出された。パラジウム塩水溶液によるエチレンの酸化でアセトアルデヒドを合成するワッカー法は,石油化学プロセスの一翼を担うこととなった(1960工業化)。ヨウ化物イオンを配位子とするロジウム錯体触媒によって,メチルアルコールと一酸化炭素から酢酸を得る反応もその流れに沿うものであり(1970工業化),化学工業原料が石油系からC1化合物に移行する状況を反映している(〈C1化学〉の項参照)。
触媒の新しい役割
環境問題を契機に,触媒は化学工業の領域を越えてその威力を発揮するようになった。煙突から出る硫黄と窒素の酸化物,あるいは自動車排ガスを処理するうえで,触媒の果たす役割は大きい。固定発生源から排出される窒素酸化物はアンモニアと反応させ,窒素と水に変えるが,このとき酸化チタン担持酸化バナジウム触媒などが使われる。移動発生源に対しては,供給酸素量を調節しつつ一酸化炭素と炭化水素を窒素酸化物と空気中の酸素でちょうど酸化しきるように白金-パラジウム-ロジウムを含む触媒で処理している。
エネルギー問題との関連では,石炭の液化・ガス化,燃焼効率を高める酸化触媒,化学蓄熱・熱パイプ・熱ポンプに利用する触媒,燃料電池電極,太陽エネルギー利用を指向する光触媒などが注目を集めている。一方,白金懐炉をはじめ,調理器の脱臭装置,ガス漏れセンサーのように,触媒を利用したさまざまのくふうが身のまわりにも見いだされる。
なお生物体内の化学反応をつかさどる酵素も触媒の一種であるが,基質特異性や反応条件などの面で一般の触媒とは著しい相違がある。詳しくは〈酵素〉の項を参照されたい。
執筆者:斉藤 泰和
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「触媒」の意味・わかりやすい解説
触媒
しょくばい
catalyst
catalyser
ある物質が少量存在することにより化学反応の速度は加速されるが、その物質自体は反応後もそのままに保たれるものをいう。たとえば、高温で窒素と水素とが反応してアンモニアができる場合に、鉄の粉末を置いておくと反応の速度がずっと速くなる。しかし鉄自体は変化を受けずに残る。また酢酸メチルの水溶液に塩酸などの酸を加えると、その水素イオンH+により、酢酸とメタノール(メチルアルコール)への加水分解が促進される。しかし、H+そのものは変化せずに加えた量だけ残る。これらの場合、鉄やH+は触媒であり、このような働きを触媒作用、触媒によって引き起こされる反応を触媒反応という。しかし、場合によっては触媒は完全には保存されず、失われることもあるが、この量が反応したものの量に比べてずっと小さいときには、やはり触媒として取り扱う。
[戸田源治郎]
触媒研究の歴史
触媒作用の研究は、1836年スウェーデンの化学者であるベルツェリウスがその作用に注目し、1901年にドイツのF・W・オストワルトが触媒の定義を与えたときからいままでに、多くの研究者によって続けられてきた。触媒の語は、ギリシア語で「結び目などを解く」を意味するkatalysisから、ベルツェリウスによって命名された。
20世紀の初めには工業用として実用化できる活性なアンモニア合成用触媒をみいだすために、試行錯誤によりながら約2万種もの触媒を次々につくって活性を試験し、現在の鉄‐酸化カリウム‐酸化アルミニウム系の触媒に到達したといわれている。現在では、いままでに積み重ねられてきた経験を基に、最適な触媒を探し出しているが、まだある程度の試行錯誤は必要である(しかし、またこれをもとに複合機能をもった触媒も開発されてきた)。また触媒作用の本性を明らかにするために、いままでに得られた実験の結果をまとめ、それから経験則を引き出し、これをもとにして触媒作用についての仮説をたてるということが行われてきている。この場合の経験則としては、触媒活性と電子状態との関係(金属、酸化物および金属錯体の触媒について)、反応に関与する物質の化学吸着能の大小に対する各種金属の序列、触媒活性と触媒表面の幾何学的構造との関係などが知られている。
[戸田源治郎]
正触媒と負触媒
普通の触媒は、その反応の速度を速めるが、なかには逆に反応速度を減少させるものがある。前者を正触媒、後者を負触媒という。
[戸田源治郎]
均一触媒反応
反応の機構として、たとえば、前に述べた酢酸メチルの加水分解では、反応物も触媒も同じ一つの溶液相中にあるから均一触媒反応という。のように反応にH+が加わり、最後にはH+が再生されると考えられている。このほか、水酸化物イオンOH-が触媒として働く反応もあり、これらをまとめて酸塩基触媒反応という。
[戸田源治郎]
不均一触媒反応
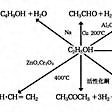
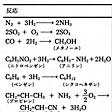
反応物が気体または液体、触媒が固体の場合で、実際に化学工業、各種装置、あるいは研究室で使われる触媒反応の大部分はこれである。アンモニア合成反応の場合、反応する窒素と水素は気体、触媒の鉄は固体であるから、異なった相の間の触媒反応なので、このような系でおこる触媒反応を不均一触媒反応という。反応の種類としては、酸化、水素化、異性化、重合、クラッキングなどがある。またそれに使われる触媒も、金属、金属酸化物、金属の各種の塩、錯体など多岐にわたる。その一例をに示す。同じ反応物でも使用する触媒、さらに反応条件により異なった生成物を与える。すなわち触媒は選択性をもつ。エタノールの例をに示す。また、いろいろな酵素は、それぞれ1種類の反応のみを促進するのできわめて選択性の高い触媒ということができる。
不均一触媒反応は、触媒と反応物とが接する場所、すなわち触媒の表面上で進行する。したがって触媒の有効さ、活性は、触媒の表面積の大きさと単位表面積当りの活性(比活性)に依存する。触媒の表面積を増すためには、触媒を細かく砕くか、多孔質のものにするか、あるいは各種の担体(支持物)の上に微粒子としてのせるかなど、いろいろな方法がとられている。
[戸田源治郎]
不均一触媒作用の機構
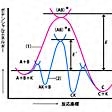
触媒の働きは、熱力学的に不可能な反応を進ませるのではなく、可能な反応の速度を増加させるだけである。その加速の過程をに示す。例として、A+B―→Cの反応の場合、(1)触媒のないときと、(2)触媒のあるときの反応進行に伴う系のエネルギー変化を示す。(1)では左側のA+Bの系に外からなんらかの方法(加熱など)でE(活性化エネルギーという)だけのエネルギーが供給されると、初めてエネルギーの極大(活性化状態)を超えて右側のCに変化することができる。この反応の速さは、全体のA+Bのうち、この極大を乗り越えて進むA+Bの割合(これはe-E/RTに比例する)によって決まる。(2)ではA(またはB)が触媒Kと結合してAK(またはBK)ができ、これにさらにB(またはA)が反応してABKの活性化状態(活性錯合体)(AB)*Kを生成し、ついで生成物Cができ、触媒Kが再生する。この過程でのエネルギー極大(E′)は、Eに比べてはるかに小さいから、反応の速さは非常に大きくなる。このように触媒は、活性化エネルギーを低下させる役割をする。
また、触媒は反応の速さを、正方向にも、また逆方向にも同じ倍率だけ増加させる。
[戸田源治郎]
助触媒と触媒毒
触媒の比活性は、触媒として働く金属や金属酸化物などに固有のものではあるが、またこれにほかの金属や金属酸化物(それら自体は活性をもたない)を添加すると、活性が大幅に改善されることがある。この添加物を助触媒または促進剤という。アンモニア合成鉄触媒には、助触媒として酸化カリウムや酸化アルミニウムが使われる。触媒作用は反応系中に、ある種の微量不純物が存在すると、活性が低下するかまたは失われる。このようなものを触媒毒、この現象を被毒という。いったん被毒した触媒は、この毒を反応系から取り去ることでその活性が回復する場合(一時被毒)と、回復しない場合(永久被毒)とがある。
[戸田源治郎]
不均一触媒反応の具体例
の反応例のうちプロピレンからアクリロニトリルをつくる反応以下は、第二次世界大戦後、大発展した石油精製(脱硫を含む)、石油化学工業に関するものである。
[戸田源治郎]
石油精製と触媒
原油は蒸留(常圧下または減圧下)によって軽質留分から重質留分へと各留分に分別される。そのうちガソリン留分はそれほど多くないので、重質留分を接触分解反応により軽質留分に変える。これには固体酸触媒が有効で、希土類でイオン交換したゼオライトが用いられる。また、高オクタン価の炭化水素をつくるためには、軽質ナフサ留分をPt-X/Al2O3-Cl-(XはGe、Sn、Pb、Re、Ir)触媒により異性化させる。燃料油の重油中には、硫黄(いおう)を含む化合物が存在し、これを除去するためにアルミナ担持モリブデン、コバルト系触媒を使った水素化脱硫が行われる。この技術が確立されたことにより硫黄酸化物による大気汚染が非常に減少した。
[戸田源治郎]
石油化学工業と触媒
合成繊維、プラスチック、合成ゴムなどの合成高分子からつくられた製品は、われわれの身近に数多い。それらのほとんどは石油化学製品で、石油ナフサ留分の高温熱分解、接触分解で生成したエチレン、プロピレン、ブタジエン、分解油などを原料としている。その製造段階には、いずれも触媒が使われているが、そのなかでもっとも画期的な触媒は、ドイツのK・ツィーグラーが発見した立体規則的オレフィン重合用のものである。
[戸田源治郎]
拡大する触媒の重要性
前節に述べたのは、触媒の化学工業に果たす役割の一例であるが、近年ますますその領域を広げている。その背景には環境問題があり、たとえば大気汚染などがそうである。大気汚染には硫黄酸化物のほかに自動車の排ガス中などに含まれる窒素酸化物が関与するが、これを除去するためにコージェライト担体上に活性アルミナ‐白金‐パラジウム(またはロジウム)を含む触媒が開発された。また工場などから排出される窒素酸化物は、酸化チタン担持酸化バナジウム触媒などを用いてアンモニアと反応させて窒素と水に変えている。これらの研究・開発で蓄積された知識は、他の分野にも応用され、脱臭、各種センサーなどにも利用されている。
このほかにも、太陽熱の高効率利用を目ざした光触媒や、石炭のガス化、液化などに用いる酸化触媒の開発など、エネルギー問題にも触媒は深く関係している。
[戸田源治郎]
『斯波忠夫他著『触媒化学概論』(1968・共立出版)』▽『触媒工業協会編『触媒の話』改訂版(2000・化学工業日報社)』▽『小野嘉夫・御園生誠・諸岡良彦編『触媒の事典』(2000・朝倉書店)』▽『化学工学会監修、西村陽一・高橋武重著『工業触媒――技術革新を生む触媒』(2002・培風館)』▽『上松敬禧・中村潤児他著『触媒化学』(2004・朝倉書店)』▽『「触媒活用大事典」編集委員会編『触媒活用大事典』(2004・工業調査会)』▽『日本化学会編『実験化学講座25 触媒化学、電気化学』第5版(2006・丸善)』
化学辞典 第2版 「触媒」の解説
触媒
ショクバイ
catalyst
熱力学的には進行できるが,現実には反応がきわめて遅い系に加えることにより,反応過程をかえることで,反応速度を増し,あるいは可能な反応のうち特定の反応のみを促進する作用をもつ物質を触媒といい,その作用を触媒作用という.触媒には,反応溶液中に溶解して作用する均一系触媒と,固体触媒のように,液体または気体の反応物とは相が異なる不均一系触媒とがある.不均一系触媒反応では,触媒作用を接触作用とよぶことがある.触媒反応は多くの素反応で構成され,逐次的に反応が進行するなかで触媒自体も化学変化をするが,反応が完結したときにはじめの状態に戻るので,繰り返し反応に使用することができる.このため,触媒の使用量は反応系全体の量に比べてきわめて少なく,また反応系についての化学量論的な反応式のなかに含まれないため,反応の前後での存在量はかわらず,反応系の平衡関係には影響しない.したがって,触媒の作用により,正反応および逆反応がともに促進される.触媒のほかの重要な機能としては,反応促進が選択的であることで,たとえばアルコールはアルミナ触媒により脱水されてオレフィンを生じるが,遷移金属触媒では脱水素されてアルデヒドを生じる.この機能を選択性といい,もっとも特異的に現れているのが酵素である.工業的にはこのほかに,触媒がその機能を維持できる時間,すなわち寿命も大切な要因となる.現在,工業的に行われているほとんどの化学反応で,触媒が用いられている.触媒として利用されている物質は,典型元素から遷移金属元素の単体およびその化合物と広範囲にわたり,各反応にそれぞれ適した触媒が開発されている.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
百科事典マイペディア 「触媒」の意味・わかりやすい解説
触媒【しょくばい】
→関連項目オストワルト|純鉄|反応速度
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「触媒」の意味・わかりやすい解説
触媒
しょくばい
catalyst; catalyser
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
栄養・生化学辞典 「触媒」の解説
触媒
世界大百科事典(旧版)内の触媒の言及
【化学反応】より
…有用な物質を生産し,有害な物質を無害化するために,非常に多くの化学反応が利用されている。 反応速度を大きくしまた特定の反応を選択的に進めるために触媒が利用される。触媒は平衡位置を変えることはないが,反応速度を大きく変化させるので,特定の物質を選択的に効率よく生産するために有効であり,現在特定の反応に選択的に働く触媒の設計もある程度可能となっている。…
※「触媒」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
初夏のころの、わずかに感じる暑さ。《季 夏》「はんけちのたしなみきよき―かな/万太郎」...