日本大百科全書(ニッポニカ) 「乳がん」の意味・わかりやすい解説
乳がん
にゅうがん
breast cancer
定義
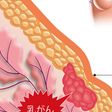
乳房内の乳腺(せん)に発生するがん(悪性腫瘍(しゅよう))。「乳管がん」と「小葉がん」に大別される。乳腺には腺葉という組織の集まりがあり、腺葉は乳管と多数の小葉で構成されている(母乳は小葉で産生され、乳管を通って乳頭まで運ばれる)。乳がんのうち約90%が乳管由来の細胞から発生する「乳管がん」、約5%が小葉由来の「小葉がん」で、まれに乳頭周囲のパジェット細胞とよばれる上皮細胞から発生する「パジェット病」などがある。病理診断に基づく組織型でも分類され、がん細胞が乳管や小葉の中にとどまっている状態を「非浸潤がん」、周りの組織(間質)に広がったものを「浸潤がん」とよぶ。浸潤がんではしこりが触知され、非浸潤がんに比べ転移や再発のリスクが高い。乳がんと診断される患者の80%以上は浸潤がんである。浸潤がんはさらに、その大半を占める一般型(乳頭腺管がん、充実腺管がん、硬がん)と特殊型(粘液がん、髄様がん、浸潤性小葉がんなど)に分けられる。
乳がんがもっとも多く発生する乳房部位は外側上部(50%)である。次いで内側上部(20%)、外側下部(10%)、内側下部(5%)、乳輪部(5%)の順となっている。発症には女性ホルモンのエストロゲンが深く関わっているため、「女性のがん」というイメージが強いが、男性もわずかながら罹患(りかん)する(罹患率は女性乳がんの1%程度)。乳腺には乳がんとの鑑別がむずかしい良性疾患が生じることもあり、乳腺症や乳管内乳頭腫、線維腺腫などがある。
[渡邊清高 2019年9月17日]
疫学・病因(危険因子)
統計
日本において乳がんで死亡する女性は2004年(平成16)に年間1万例を超え(1万0524例)、以後も増加を続け2017年に乳がんで死亡した女性は1万4285例で、女性のがん死亡全体(15万2936例)の9.3%を占めている。部位別にみると、大腸(2万3347例)、肺(2万1118例)、膵臓(すいぞう)(1万6823例)、胃(1万5481例)に次いで第5位の死亡数となっている。年齢階級別の死亡率は40歳以降大きく上昇し、50歳代後半でピークに達する。
2014年に乳がんに罹患した女性は7万6257例(全国合計値)で、女性のがん罹患全体(36万5881例)の20.8%を占めている。部位別にみると、女性では乳がんの罹患数がもっとも多く、以下は大腸がん(5万7735例)、胃がん(3万9493例)、肺がん(3万5739例)、子宮がん(2万4944例)と続く。乳がんの罹患数は、2007年には5万6289例、2009年には6万1232例、2011年には7万2472例と年々増加している。年齢階級別の罹患率は30歳以降大きく上昇し、40歳代後半から50歳代前半にピークがある。
経年的な推移をみるうえで、人口の高齢化の影響を除き、一定の年齢構成に調整した数値を比較する年齢調整死亡率は、近年は横ばい、年齢調整罹患率は増加傾向を示している。両指標ともに日本は欧米諸国より低値であるが、その差は縮まる傾向にある。
また、欧米では閉経後の乳がん発症が多いのに対し、日本においては30歳代から増加し始める、比較的若い年齢から発症するがんとなっている(データ出典:国立がん研究センターがん対策情報センター)。
[渡邊清高 2019年9月17日]
要因
女性ホルモンのエストロゲンが乳がんの発症に深く関わっている。体内のエストロゲンレベルやエストロゲンへの暴露期間がリスク要因とされ、初経年齢が早い、閉経年齢が遅い、出産歴がない、授乳歴がないことなどが発生の危険性を高める。また閉経後の肥満、飲酒習慣、良性乳腺疾患の既往歴などもリスクとされる。経口避妊薬や閉経後の女性ホルモン補充療法など、体外からのホルモン追加でリスクが高まる可能性も指摘されている。
2017年の世界がん研究基金(WCRF)と米国がん研究協会(AICR)による報告では、乳がんとの関連が確実な食物・栄養・身体要因として、閉経前乳がんでは「成人期の身長の高さ」、閉経後乳がんでは「飲酒習慣」「肥満」「成人期の体重増加」「成人期の身長の高さ」、可能性がある要因に、閉経前乳がんでは「飲酒習慣」「重い出生時体重」、一方、乳がんリスク低下の可能性がある要因として、閉経前乳がんでは「活発な運動」「減量」「授乳」、閉経後乳がんでは「運動」「若年期(18~30歳)の減量」「授乳経験」があげられている。また遺伝性乳がんの存在も知られており、乳がん患者全体の5~10%を占める。BRCA1遺伝子もしくはBRCA2遺伝子の変異が原因で、これらは同側乳房の乳がん再発、反対側乳房の乳がんや卵巣がんのリスクにもなる。
[渡邊清高 2019年9月17日]
分類
病理組織学的分類
日本乳癌学会の「乳癌取扱い規約」による組織学的分類(組織型分類)では、乳がんは「非浸潤がん」(14.0%)、「浸潤がん」(85.5%)、「パジェット病」(0.4%)の3型に大別される。非浸潤がんは「非浸潤性乳管がん」(13.8%)と「非浸潤性小葉がん」(0.2%)に、浸潤がんは「浸潤性乳管がん」(79.2%)と「特殊型」(8.6%)に分けられる。さらに浸潤性乳管がんは「乳頭腺管がん」(24.8%)、「充実腺管がん」(13.8%)、「硬がん(32.3%)」の3型、特殊型は「粘液がん」(2.9%)、「髄様がん」(0.4%)、「浸潤性小葉がん」(3.5%)など12種類に細分化されている。
[渡邊清高 2019年9月17日]
浸潤・転移様式
乳がんには、がん細胞が乳管の中を広がる「乳管内進展」と、乳管の壁である基底膜を破り、乳管の外の間質に広がる「浸潤」の、二つのおもな進展パターンがある。がん細胞が間質だけにとどまらず、他の部位で病巣を形成した状態が「転移」であるが、乳がんは他の固形がんと比較して、限局している状態であっても転移が起こりやすいがんと特徴づけられる。乳房近くの腋窩(えきか)リンパ節や皮膚、骨(椎体(ついたい)や肋骨(ろっこつ)、骨盤など)、肺、肝臓、脳などがおもな転移部位で、がん細胞が血液やリンパの流れにのって移行しそこで増殖する。骨や肺、肝臓、脳など、乳房から離れた臓器に発生する転移を「遠隔転移」とよぶ。
再発については、乳房温存手術後、乳房内で起こる再発(乳房内再発)と、乳房切除術後、近傍の胸壁やリンパ節、周囲の皮膚に微小転移して発生する再発(局所再発)がある。
[渡邊清高 2019年9月17日]
症状・症候
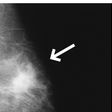
初期には無症状のことが多く、乳がん検診(マンモグラフィ検査)で指摘される例も少なくない。自覚症状としては、乳房や腋窩(わきの下)のしこり、乳首からの血性分泌物、乳首のびらん(ただれ)、乳房の皮膚のひきつれ、乳房の変形や左右差、乳頭の陥没などがみられることがある。転移した場合は部位によってさまざまな症状が現れる。乳房周辺のリンパ節に転移するとリンパの流れが滞って腕がむくんだり、神経が圧迫されて腕がしびれたり、骨転移では腰や背中、肩の疼痛(とうつう)、肺転移では咳(せき)や息苦しさを生じたりする。骨転移では骨折が起こることもある。脳転移によって頭痛、吐き気・嘔吐(おうと)、麻痺(まひ)、けいれんなどが起こることもある。肝臓への転移では症状は現れにくいことが多い。
乳房のしこりは明確ではないが、皮膚が赤く、痛みや熱を伴う乳がんを「炎症性乳がん」とよぶ。ただし痛みやむくみなどは良性疾患の乳腺症や線維腺腫、細菌感染が原因の乳腺炎や蜂窩織炎(ほうかしきえん)などでも起こり、乳がんに特異的な症状ではない。
[渡邊清高 2019年9月17日]
検査・診断
検査・診断
(1)乳がん検診
対策型検診として実施されている乳がん検診は40歳以上の女性が対象で、2年に1回の受検が推奨されている。おもな検診内容は問診と乳房X線検査(マンモグラフィ検査)である。視触診はとくには推奨されていないが、実施する場合はマンモグラフィ検査と併用される。マンモグラフィ検査は40歳以上の女性の乳がん死亡リスクを低下させることが科学的に証明されており、乳がん検診の国際基準になっている。実際にアメリカやイギリスでは、マンモグラフィ検査の受検率の上昇に伴い、罹患率は上昇しているにもかかわらず死亡率は低下し続けている。日本ではがん検診受診率が先進諸国と比較し低いことが課題である(44.9%、2013年データ)。一方で近年では検査を受けることの不利益(偽陽性〈がんではないのに陽性と判定されること〉や過剰診断〈生命予後に関係のないがんが発見され治療されること〉)についても指摘されている。また、乳腺密度が高い40歳代では検診精度が低下することも知られている。
従来、検診項目に含まれることが多かった超音波検査については、マンモグラフィ検査と併用した場合、マンモグラフィ検査単独に比べて40歳代の女性の乳がん発見率が高いことがわかっている。一方、超音波検査の実施により、治療不要の良性変化が過度に抽出される欠点もあり、乳がん死亡率を低下させるエビデンスは十分に示されていない。そのほかにもMRI検査やPET検査などが実施されることもあるが、いずれも対策型検診としての乳がん検診としては推奨されていない。
(2)原発巣の存在診断
マンモグラフィ検査などで乳がんが疑われた場合、病巣の一部を採取し、がん細胞の存在を顕微鏡で確認する病理検査・病理診断が行われる。がん細胞が確認されれば、その種類や性質などを精査する。病理検査には「細胞診」と「組織診」があり、前者は細胞、後者は組織を採取する。細胞診には乳頭からの分泌液を検査する分泌液細胞診と、病巣に細い針を刺し、吸引した細胞を検査する穿刺(せんし)吸引細胞診がある。細胞診は身体への負担が比較的少ないものの、偽陽性や偽陰性(がんなのにがんではないと判定されること)となる可能性がやや高い傾向がある。
組織診は病理診断を確定するための検査で、「生検」とよばれる。生検では局所麻酔下で病巣組織を採取する。注射針より太い針を使用する針生検、さらに太い針を用いて十分量の組織を採取する吸引式組織生検(マンモトーム生検)、皮膚を切開して病巣の組織を採取する外科的生検がある。生検は腫瘍に関するより詳しい情報が得られ、確実な診断につながることから、近年では細胞診よりも生検が優先して行われることが多い。生検によって得られる具体的な情報は、がんの場合には浸潤の有無、腫瘍の大きさ、組織型、悪性度(グレードgrade)、増殖能(Ki67陽性細胞の割合)、ホルモン受容体の有無、HER2(ハーツー)タンパクの過剰発現あるいはHER2遺伝子増幅の有無などである。さらに、超音波検査やCT、MRIなどによる画像診断により、リンパ節転移の有無と個数、血管侵襲(病変周囲の血管やリンパ管にがん細胞がみられるか)、遠隔転移の有無などの評価が行われる。これらの情報と患者の年齢、卵巣機能(月経状況)などから治療法が検討されていく。
がんの悪性度は細胞の形状から判断され、グレード1~3に分けられる。上位グレードほど悪性度は高く、転移・再発のリスクが高い。
がん細胞の増殖能はKi67というタンパクが指標とされ、Ki67陽性細胞の割合(Ki67値)が高ければ増殖能が高く、悪性度も高いと判断される。
HER2タンパクは細胞表面に存在して細胞増殖を調節しており、HER2タンパクが過剰発現した状態、あるいはHER2タンパクをコードする(もととなる)遺伝子が増幅した状態では転移・再発のリスクが高い。一方で、HER2タンパクは、特異的に結合する分子標的治療薬の標的になる。
ホルモン受容体の存在は内分泌療法(ホルモン療法)の効果を左右する。ホルモン受容体陽性ではエストロゲンがホルモン受容体に結合してがん細胞を増殖させるため、エストロゲンの結合をブロックするホルモン療法が有効であることが推測できる。
ホルモン療法をはじめとする薬物療法の選択では、これまでもホルモン受容体やHER2タンパクなどを指標に検討されてきたが、近年ではがん細胞の性質(生物学的因子)に基づいたサブタイプ分類が定着してきている。(a)ホルモン受容体(エストロゲン受容体、プロゲステロン受容体)の有無、(b)HER2タンパクの有無、(c)Ki67値により乳がんを五つに分類するもので、このサブタイプによって治療方針を決定するという考え方である(後述)。
(3)その他の検査
乳がんと診断された後、治療前に実施する画像診断では、腫瘍の大きさ、反対側乳房内病巣の有無、腋窩リンパ節転移の有無と程度、遠隔転移の有無などが調べられる。これらはマンモグラフィ検査や超音波検査では完全に把握することが困難なため、造影剤を用いたCT検査やMRI検査、PET検査が実施される。これらの画像診断で腋窩リンパ節転移が認められれば、外科療法(手術)時に、乳房内の病巣とともに腋窩リンパ節の郭清(かくせい)(切除)が原則として行われる。画像診断で転移なし、あるいは転移の有無が判然としない場合にはセンチネルリンパ節生検が実施される。センチネルリンパ節とは、乳房内からがん細胞が最初に到着するリンパ節と定義され、このセンチネルリンパ節を同定して採取し、転移の有無を顕微鏡で確認する。センチネルリンパ節にがん細胞が認められなければ他のリンパ節にも転移がないと判断され、反対に転移があると判断されれば乳房の病巣とともに腋窩リンパ節の郭清が行われる。センチネルリンパ節生検を行うことによって、手術後のリンパ浮腫、腋窩や上腕の感覚異常などの、腋窩リンパ節郭清によって起こりうる後遺症を回避できる可能性がある。
その他の検査として、骨転移の有無や位置を確認するために骨シンチグラフィ検査が行われることもある。また血液検査においてCEAやCA15-3などの腫瘍マーカーが上昇する可能性があるが、いずれも乳がんに特異的なマーカーでなく、おもに治療後の経過観察や再発の有無の確認、薬物療法の治療効果の評価などに用いられる。
[渡邊清高 2019年9月17日]
病期分類
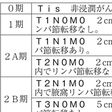
乳がんの病期(ステージstage)は、腫瘍の大きさ、リンパ節転移の有無、骨や肺、肝臓や脳などへの遠隔転移の有無により分類され、治療方針の決定や予後の推測などの指標となる。日本においては「乳癌取扱い規約」(日本乳癌学会編)の進行度分類や、国際対がん連合(UICC)のTNM分類に基づいて病期分類が行われている。いずれも原発巣の大きさや状態を示すT因子(皮膚浸潤と胸壁浸潤の状況および腫瘍の最大径を評価)、リンパ節転移の有無を示すN因子(触診や画像所見をもとに評価)、遠隔転移の有無を示すM因子(画像所見などをもとに評価)の3因子から分類する。「乳癌取扱い規約」の進行度分類では、ステージ0(非浸潤がん)~Ⅳ(他臓器転移あり)まで8段階〔0、Ⅰ、Ⅱ(ⅡA、ⅡB)、Ⅲ(ⅢA、ⅢB、ⅢC)、Ⅳ〕に分けられている。UICCのTNM分類では手術後の検査結果によりステージⅠをⅠA期とⅠB期に分けているが、それ以外は進行度分類と同一である。
[渡邊清高 2019年9月17日]
治療
治療法の選択
乳がんの治療では、外科療法(乳房温存手術〈乳房部分切除術〉、乳房切除術〈乳房全摘術〉)、放射線療法、薬物療法(ホルモン療法、化学療法〈抗がん剤治療〉、分子標的治療〈抗HER2療法〉)が単独または複数組み合わせて行われる。基本治療は根治を目ざした外科療法であり、初期治療では他臓器への転移がみられない場合を中心に外科療法が検討される。転移・再発乳がんの治療では、延命や生活の質(クオリティ・オブ・ライフ、QOL)の維持に主眼が置かれ、薬物療法が治療の中心となる。
「乳癌診療ガイドライン」(日本乳癌学会編)には、病期に応じた標準的な治療の方向性が提示されており、治療法の選択に際しての目安となっている。
[渡邊清高 2019年9月17日]
外科療法(手術)
手術可能と判断される乳がんの場合、乳房内のがんの大きさや進展範囲、患者の希望、身体状況などを考慮して術式が選択される。また必要に応じて乳房周辺の領域リンパ節郭清(切除)が行われる。
(1)乳房温存手術(乳房部分切除術)
乳房を全摘出せず、乳頭と乳輪を残した上で、腫瘍を周囲の正常乳腺を含めて部分切除する術式である。日本では現在もっとも実施割合の高い術式となっている(約60%)。乳房温存手術の目的は、乳房内再発率を高めることのないよう病巣を確実に切除しつつ、整容的に患者が満足できる乳房を残すことである。ステージ0~Ⅱに対する標準的な外科療法に位置づけられる。かつては乳房の4分の1程度を切除する扇状部分切除術が多く行われていたが、近年では術前の画像検査で腫瘍範囲を詳細に測定し、より狭い範囲を円形に切除する円状部分切除術が増加している。術後に放射線療法を実施し、乳房内再発を予防する。
(2)乳房切除術(乳房全摘術)
乳房全体を切除する術式で、がんが乳房の広範囲に広がっている場合などに選択される。胸筋を残すため、術後に腋窩が陥没したり、皮膚に肋骨が浮き出たりすることは少なく、従来行われてきたハルステッド法(胸筋+腋窩~鎖骨下リンパ節も切除する術式)や拡大乳房切除術(ハルステッド法+鎖骨上リンパ節と胸骨傍リンパ節の切除も加えた術式)などに比べると整容性にも配慮されるようになっているが、治療成績は乳房温存手術に放射線治療を併用した場合と同等との報告があり、近年は実施割合が低下している(約30%)。
一方で、乳房皮膚、乳頭、乳輪を残し、皮下の乳腺を全切除する乳頭温存乳房切除術が整容性の面からも普及してきている。
(3)腋窩リンパ節郭清
乳房内のがん細胞が最初に転移するリンパ節のほとんどは腋窩リンパ節(わきの下の脂肪組織の中に埋め込まれるように存在しているリンパ節)であり、腋窩リンパ節を周囲の脂肪組織も含めて一塊(ひとかたまり)に切除することを腋窩リンパ節郭清という。転移の有無や転移個数を調べることに加え、再発を防ぐことを目的に行われる。
(4)乳房再建術
手術によって失われた乳房を形成外科の技術によって再建する手術である。自家組織を用いる方法と人工乳房(インプラント)を用いる方法があり、乳房切除術と同時に行う一次再建と切除術後期間をあけて行う二次再建に分けられる。自家組織による再建ではおもに腹部や背中の組織を移植し、乳房の形状を再現する。人工乳房による再建では皮膚を伸ばすエキスパンダーを胸の筋肉下に挿入し、その内部に生理食塩水を注入して乳房の形に膨らませ、エキスパンダーをシリコン製の人工乳房に入れ替える。手術を担当するのはおもに形成外科医となる。
治療によって変化した外見を補い、術後のQOLの維持や乳房を失うことで生じる心理的ショックを和らげることを目的に行われるもので、実施は患者の希望に基づくが、乳房切除を行うすべての女性において検討されるべきものである。
(5)術後合併症
乳がんの手術範囲は乳房周囲の限定された部位であるため、内臓機能などの全身への影響は小さく、術後比較的早期に通常の生活に戻ることができる。一方、手術した側の腕や肩の運動障害(動かしたりあげたりがしにくくなる)、痛み、むくみ、倦怠(けんたい)感、感覚障害(しびれなど)が生じることがある。このため、術後には肩や腕の運動リハビリテーションが行われる。また腋窩リンパ節を切除した場合には、リンパ浮腫のために腕にむくみが生じることがある。リンパ浮腫は、術後間もないときから起こることもあれば、数年後に起こってくることもある。
その他、片側の乳房切除により左右の身体のバランスが崩れ、歩行時などに不安定感を覚えることがある。乳がん術後用の補正用品や補正下着(乳房パットなど)の使用は、術後の胸部を保護しつつ身体の左右バランスや外見の整容性を保つのに役だつ。
[渡邊清高 2019年9月17日]
放射線療法
高エネルギーのX線や電子線などの放射線を体外から照射し、がん細胞の遺伝子を損傷させることで増殖の活発ながんを抑制する。手術同様、局所療法に位置づけられる。放射線は正常細胞も通過するが、がん細胞に比べてダメージを受けにくく回復しやすいため、がん組織を効率よく攻撃できる。乳房温存手術後に、温存した乳房やリンパ節などからの再発を抑制する目的で予防的に実施されたり、あるいは再発後、がん細胞の増殖や骨転移に伴う痛み、脳転移による神経症状などを軽減する目的で実施される。近年では外来での治療が主流となっている。
最近では陽子線や重粒子線という特殊な放射線を使った治療が種々のがんに対して行われるようになってきたが、乳がんでは治療標的とする病変が体表に近く、X線や電子線で安全かつ効率よく治療できるため、陽子線や重粒子線による治療は健康保険の適用にはなっていない。
放射線治療による副作用として、放射線照射部位の皮膚炎(赤み、熱感など)が治療中~治療後1、2週間にみられることがあるほか、皮膚の乾燥、倦怠感、食欲不振などが生じることもある。また、治療終了後、数か月を経て起こりうる晩期副作用として、肺炎、咳や微熱の持続などがある。
[渡邊清高 2019年9月17日]
薬物療法
従来、腫瘍の大きさやリンパ節転移の有無など解剖学的な所見に基づいて薬物療法が選択されてきたが、前述の通り、近年ではエストロゲン受容体、プロゲステロン受容体、HER2タンパク、Ki67の各生物学的因子に基づいた薬剤の使い分けが提唱されている。これらの因子に基づく分類は「サブタイプ分類」とよばれ、(1)ルミナルA型、(2)ルミナルB型(HER2陰性)、(3)ルミナルB型(HER2陽性)、(4)HER2型、(5)トリプルネガティブの5型に分けられる。
おのおのの臨床病理学的特徴として、(1)ルミナルA型はエストロゲン受容体およびプロゲステロン受容体陽性、HER2タンパク陰性、Ki67低値、(2)ルミナルB型(HER2陰性)は、エストロゲン受容体が陽性または陰性、プロゲステロン受容体が弱陽性または陰性、HER2タンパク陰性、Ki67高値、(3)ルミナルB型(HER2陽性)は、エストロゲン受容体陽性、プロテステロン受容体が陽性または陰性、HER2タンパク陽性、Ki67低~高値、(4)HER2型はHER2タンパクのみ陽性、(5)トリプルネガティブはエストロゲン受容体、プロゲステロン受容体、HER2タンパクがすべて陰性(ネガティブ)の状態である。
選択される薬物療法の基本は、ルミナルA型がホルモン療法、ルミナルB型(HER2陰性)がホルモン療法に加え、場合により化学療法、ルミナルB型(HER2陽性)が化学療法+抗HER2療法+ホルモン療法、HER2型が化学療法+抗HER2療法、トリプルネガティブが化学療法とされている。
(1)ホルモン療法
乳がんでは、がん細胞の増殖に女性ホルモンを必要とするタイプが全体の7~8割を占める。このタイプには女性ホルモンの働きを阻害する「ホルモン療法」の効果が期待される。対象となるのはエストロゲン受容体かプロゲステロン受容体のいずれかが認められるホルモン受容体陽性の乳がんである。使用されるのは抗エストロゲン薬(タモキシフェン、トレミフェン、フルベストラントなど)、アロマターゼ阻害薬(アナストロゾール、エキセメスタンなど)、LH-RHアゴニスト(黄体ホルモン放出ホルモン抑制薬。ゴセレリン、リュープロレリンなど)などで、閉経前患者では卵巣からのエストロゲン分泌を抑制するLH-RHアゴニストや、女性ホルモンのエストロゲン受容体への結合をブロックする抗エストロゲン薬、閉経後患者では微量に放出される男性ホルモンからのエストロゲン合成に関わるアロマターゼという酵素を阻害するアロマターゼ阻害薬、あるいは抗エストロゲン薬が用いられる。
手術可能なホルモン受容体陽性乳がんでは、腫瘍を縮小させて手術を行うことで、切除範囲を小さくして術後の合併症や組織欠損を小さくすることを企図して、術前ホルモン療法が行われることがある。一方、手術後に微小な残存病変の根絶や再発リスクの低下を目的としてホルモン療法を行う場合には、薬剤の種類や再発のリスクなどにもよるが5~10年間程度治療が続けられる。
ホルモン療法の副作用は殺細胞性の抗がん剤による治療に比して少ないものの、更年期障害様の症状(ほてり、のぼせ、顔面紅潮、発汗、動悸(どうき)など)、体重増加、骨粗鬆症(こつそしょうしょう)が現れる場合があり、必要に応じて症状を緩和させる薬剤などを併用しながら治療を継続していく。
(2)化学療法(抗がん剤治療)
がん細胞は正常細胞と異なり、際限なく増殖し続ける性質がある。化学療法は殺細胞性の抗がん剤を用い、細胞増殖を制御している遺伝子の複製や転写機構に作用したり、がん細胞の分裂を阻害したりすることで異常な増殖を抑制する。
根治目的で手術療法に併用して化学療法が行われる場合、術前に実施される化学療法(術前補助化学療法)と術後に実施される化学療法(術後補助化学療法)があり、前者は、腫瘍が大きい、術後の合併症や組織欠損が大きいなどのために手術困難な場合に、手術の根治性を高めることを目的に3か月~半年ほどかけて術前化学療法を行うことで、あらかじめ腫瘍を縮小させて手術を行うものである。後者は、手術による治療効果を高め、術後の転移・再発を防ぐため、潜在している微小転移を滅することを目的に行われる。術後補助化学療法では、作用が異なる複数の抗がん剤を併用し、効果的にがん細胞を攻撃する。
また、手術が困難な進行がんや再発がんに対しても化学療法が検討される。手術不能・再発・進行乳がんの場合の殺細胞性抗がん剤の使用においては、効果と不利益(副作用や後遺症のリスク、コストなど)のバランスが重視される。殺細胞性抗がん剤による治療は、肺・肝臓・脳など生命予後に影響を及ぼす病変がある場合に、腫瘍の縮小や症状の軽減効果を期待して検討される。一方、転移を有する場合であっても生命予後への影響が少ないと考えられる場合には、がんの特性(ホルモン受容体の有無、HER2の発現、悪性度など)、患者の状態(全身状態、閉経の前後、臓器機能)、患者の希望(生活への影響、整容、治療方法やコストなど)などさまざまな側面からの検討が行われ、なるべく負担の少ない治療法が検討される。
乳がんに使用されるおもな抗がん剤には、アントラサイクリン系薬剤(ドキソルビシン、エピルビシンなど)、タキサン系薬剤(ドセタキセル、パクリタキセルなど)、代謝拮抗(きっこう)薬(フルオロウラシル、カペシタビン、ゲムシタビンなど)、ビンカアルカロイド、エリブリンなどがある。がんの進行状態や患者の状態、治療反応性、過去の治療歴など複数の要素を考慮して治療薬が選択され、薬剤により経口または経静脈的に投与される。
殺細胞性の抗がん剤は正常細胞にも影響を及ぼすため、使用にあたっては副作用が生じる。毛髪、口腔(こうこう)や消化管などの粘膜、血球をつくる骨髄などの新陳代謝が盛んな部位はとくに影響を受けやすく、脱毛、口内炎、下痢、白血球(好中球)や血小板の減少などが発生する。全身倦怠感、吐き気、手足のしびれ、筋肉痛、関節痛、皮膚や爪の変化、肝機能異常などがみられることもある。これらの副作用に対しては、予防や対策を講じながら、治療を円滑に進められるよう配慮される。好中球減少に対するG-CSF(顆粒球(かりゅうきゅう)コロニー刺激因子)製剤や、貧血に対する輸血の実施、吐き気・嘔吐のリスクが高い薬剤を使用するときの制吐剤の予防的な使用など、副作用に対する予防や治療・ケア(支持療法という)が、治療と同様に重視されている。
(3)分子標的治療(抗HER2療法)
分子標的治療は、がん細胞の増殖に関わる分子を標的とし、その働きをピンポイントで阻害する治療法である。乳がんではHER2タンパクががん細胞の増殖に強く関わっているため、この働きを選択的に阻害する抗HER2療法が行われる。使用される分子標的治療薬には、トラスツズマブ(商品名:ハーセプチン)、ペルツズマブ(商品名:パージェタ)、トラスツズマブエムタンシン(商品名:カドサイラ)、ラパチニブ(商品名:タイケルブ)などがある。乳がん患者の15~20%を占めるHER2陽性患者が対象になる。
抗HER2療法は一般に、化学療法に比して副作用は少ないが、心機能低下や呼吸機能障害、インフュージョンリアクション(発熱、悪寒、頭痛、発疹、嘔吐などの一過性の急性輸注反応)、手足症候群(手足の赤み・腫(は)れ・ひび割れ・痛みなど)など、特有の副作用が生じることがある。
分子標的治療薬の仲間には、がん細胞に栄養や酸素を供給する血管の新生を阻害するベバシズマブ(商品名:アバスチン)や、がん細胞の増殖に関わるmTOR(エムトール)タンパクの働きを阻害するエベロリムス(商品名:アフィニトール)、細胞分裂の制御機構を治療標的としたCDK4/6阻害薬であるパルボシクリブ(商品名:イブランス)やアベマシクリブ(商品名:ベージニオ)などもあり、乳がんの治療に用いられている。
なお、若年発症の乳がん、乳がんや卵巣がんなどの家族歴を有する乳がん患者においては、BRCA1、BRCA2遺伝子変異の検査が考慮される。遺伝性乳がんの治療薬として、BRCA1/2陽性の場合には、PARP阻害薬であるオラパリブ(商品名:リムパーザ)が適応となる。BRCA1/2遺伝子変異はDNAの損傷応答経路に異常をきたすことによって、乳がん・卵巣がんなどの若年発症をもたらす。オラパリブはがん細胞に特異的に作用し、BRCA変異をもつがん細胞に細胞死を誘導することで抗腫瘍効果を発揮する。一方で、BRCA1/2変異は生殖細胞系列変異であり、血縁者の発症リスクや、家族性卵巣がん・乳がん症候群(HBOC)の同定につながる可能性がある。ゲノム情報に基づく医療・予防の実施、患者・血縁者への検査前・検査後の遺伝カウンセリングの実施など、ゲノム医療提供体制の整備が進められている。
[渡邊清高 2019年9月17日]
経過・予後
集学的治療の進歩を背景に、乳がんの予後は他臓器のがんに比して比較的良好である。全国がんセンター協議会(全がん協)が公表している加盟32施設院内がん登録から算出された乳がんの5年相対生存率(2007~2009年診断症例)は、ステージⅠが100%、ステージⅡが96.0%、ステージⅢが80.8%、ステージⅣが37.1%と報告されている。一方で、治療後長期にわたって再発リスクがあるがんであり、たとえば根治的手術を行ったあとのホルモン療法について、再発のリスクや副作用のバランスを考慮した上で、10年間継続されることがある。
分子標的治療薬の登場や効果的な治療レジメン(薬剤の組合せ)の開発、治療の副作用を軽減する支持療法の進歩などが、治療成績の向上、再発の抑制、症状緩和などに寄与している。
[渡邊清高 2019年9月17日]
その他
高濃度乳房
乳房内の乳腺濃度が高く、その分布が不均一である状態を「高濃度乳房」といい、日本人に多いことが知られている。乳がん検診(マンモグラフィ検査)の特性上、高濃度乳房では乳がんの病巣が発見されにくい傾向がある。そこで期待されているのが高濃度乳房に対する超音波検査の活用である。がん対策のための戦略研究「超音波検査による乳がん検診の有効性を検証する比較試験」(J-START(ジェイスタート)試験)が実施され、感度およびがん発見率が向上する結果が得られている。一方で死亡率減少効果は明らかではなく、超音波検査を検診に導入することの利益と不利益について、さらなる検討が進められている。
[渡邊清高 2019年9月17日]
糖尿病と乳がんの関連
糖尿病患者では一部のがんのリスクが高くなることが明らかにされている。乳がんはその一つで、インスリン抵抗性に伴う高インスリン血症や高血糖などが要因と考えられている。糖尿病と乳がんの関連については多くの臨床研究が行われ、糖尿病患者では非糖尿病患者に比べ、約1.2~1.3倍のリスク増であることが海外報告で示されている。
[渡邊清高 2019年9月17日]
『日本乳癌学会編『患者さんのための乳がん診療ガイドライン 2016年版』(2016・金原出版)』▽『日本乳癌学会編『乳癌取扱い規約』第18版(2018・金原出版)』▽『日本乳癌学会編『乳癌診療ガイドライン 2018年版』(2018・金原出版)』▽『〔WEB〕国立がん研究センターがん情報サービス『一般の方向けサイト(乳がん)』』▽『〔WEB〕国立がん研究センターがん情報サービス『がん登録・統計』』