精選版 日本国語大辞典 「希土類元素」の意味・読み・例文・類語
きどるい‐げんそ【希土類元素・稀土類元素】
日本大百科全書(ニッポニカ) 「希土類元素」の意味・わかりやすい解説
希土類元素
きどるいげんそ
rare-earth element
周期表第3族のスカンジウム、イットリウム、および原子番号57~71のランタノイドの15元素をあわせた17元素の総称。スカンジウムとイットリウムを除いた15元素をランタノイドとよび、あるいはランタニドとよぶことがあるが、この名称は適当ではない。ときにはこれに、第二希土類元素といわれるアクチノイド(原子番号89~103の元素の総称)をも含めていうこともある。ランタンからサマリウムまでの6元素をセリウム族元素、ユウロピウムからルテチウムまでとイットリウム、スカンジウムをあわせた11元素をイットリウム族元素という。
[中原勝儼]
存在
これらの元素の化合物は、初めは比較的希(まれ)にしか産しない鉱物から得た混合酸化物(土(ど)earthとよんでいた)から分離されたので、これを希土類元素(レア・アース)とよび、すべて希元素に属するとしたが、実際の地殻中の存在量はそれほど少なくないことがわかっており、希元素に分類するのはあたらない。たとえば希土類元素のうち地殻中の元素存在度が最大のものはセリウムであるが、これはスズ、鉛、亜鉛などよりも大きいし、最小のツリウムでもビスマスと同じ程度で、銀よりは大きい。ただし、プロメチウムだけは放射性元素で安定同位体は存在せず、天然には存在しない。また、一般に原子番号奇数のものは両隣のものに比べて存在量が少ない。
[中原勝儼]
性質
セリウム族は水酸化物の塩基性が強く、モナズ石、褐簾石(かつれんせき)などの主成分となる。イットリウム族は水酸化物の塩基性が弱く、ゼノタイムやガドリン石などの主成分となって存在する。希土類元素の大部分を占めるランタノイドは内遷移元素(核外電子の電子配列が内部軌道であるf軌道で、原子番号増大とともに増加していることにより内遷移あるいは内部遷移とよばれる)で、化学的性質はよく似ており、またイットリウムのイオン半径その他も似ているため、これらの希土類元素は地球上でつねに共存し、鉱物から取り出しても混合物であることが多い。これらのことから各元素を相互に分離するのには困難なことが多く、溶媒抽出法、イオン交換法などを利用して行われている。
単体は一般に銀白色ないし灰白色の金属。空気中では徐々に酸化される。酸および熱水には溶けるが、アルカリには溶けない。化学的性質はよく似ており、普通すべて酸化数+Ⅲの化合物をつくるが、セリウム、テルビウム、プラセオジムでは+Ⅳ、イッテルビウム、ユウロピウム、サマリウムでは+Ⅱの化合物もある。アルカリ金属、アルカリ土類金属に次いで陽性が強く、そのため水酸化物は強い塩基である。酸化物、水酸化物の塩基性は原子番号を増すとともに弱くなっている。一般に塩化物、臭化物、ヨウ化物、硝酸塩、過塩素酸塩、臭素酸塩は水に可溶、フッ化物、炭酸塩、リン酸塩、シュウ酸塩は不溶で、硫酸塩は可溶性から難溶性のものまである。複硝酸塩、複硫酸塩、キレート化合物なども多く知られている。Sc3+、Y3+、La3+、Ce4+、Lu3+、Yb2+などは反磁性であるが、その他は一般に常磁性である。イットリウムなどを含む銅酸化物での高温超伝導体が多く知られており、この分野での発展は著しい。
単体および化合物は、合金、触媒、原子炉材料などに用いられ、そのほか、磁性、誘電性などの特異性によって種々の用途がある。
[中原勝儼]
産業
希土類元素(レア・アース)は世界各国で採掘されるものの、単体元素として取り出すのがむずかしく、希少価値が高い。充電式電池、高性能永久磁石、発光ダイオード、光学ガラス、研磨剤、排ガス触媒、レーザーなどの原料として不可欠で、スマートフォン、液晶テレビ、エコカー、光磁気ディスクなど幅広い先端技術製品に使われている。微量を添加するだけで電子部品などの性能が向上するため「産業のビタミン」とよばれることもある。
希土類元素の埋蔵量をみると、2020年時点で中国(37%)、ベトナム(18%)、ブラジル(18%)、ロシア(10%)、インド(6%)、オーストラリア(3%)など世界に分布するが、採掘人件費の上昇や、残土に有害物質が含まれることもあって、アメリカなどが一時生産を停止し、2000年代初頭には中国が世界生産の9割強を占めていた。しかし資源ナショナリズムの台頭もあって、中国依存から脱却すべきだとして、アメリカ、オーストラリアなどが生産を再開。2020年時点で、中国が世界生産量の6割を占め、アメリカ、ミャンマー、オーストラリアなどが世界の1割程度をそれぞれ生産している。2010年(平成22)、尖閣(せんかく)諸島沖での中国漁船船長逮捕事件が日中間の外交問題に発展した際には、中国は希土類元素の対日輸出を一時停止する措置をとった。このため日本政府も中国以外の安定調達先を探しており、ベトナムやカザフスタンからの調達のほか、希土類元素の代替品開発の動きが出ている。
[矢野 武 2021年9月17日]
化学辞典 第2版 「希土類元素」の解説
希土類元素
キドルイゲンソ
rare earth elements
【Ⅰ】希土類元素:周期表3族のSc,Y,およびランタノイド(La~Lu)15元素の合計17元素のこと.ただし,アクチニドも含めることもある.土とは,苦土MgO,ばん土Al2O3など,ある種の金属酸化物のこと.希は,最初に発見されたのが珍しい鉱物中であったためであるが,現在では希ではない.天然には,地殻中に化合物(炭酸塩,リン酸塩など)として広く存在し,その存在度は,一番多いCeはCuよりやや多い程度,一番少ないTmやLuでもI程度(Clの半分,Agの7倍程度)である.なお,ハーキンズの規則により,原子番号が偶数の元素は,両隣りの奇数番号の元素より存在確率は大きいことが認められる.おもな鉱石は,モナズ石(リン酸塩でCe族が多い),バストネス石(炭酸塩で,Ce族が多い),ゼノタイム(リン酸塩で,Y族が多い)である.これらの鉱石はいずれも全希土類を含んでいる.希土類元素は相互の性質が類似していて,通常の化学操作では単離が困難であったが,現在,分離はイオン交換法や連続溶媒抽出法などにより行われている.各元素の単体金属は,各元素の塩化物やフッ化物の溶融電解,またはアルカリ金属による還元などで得られる.とくに高純度なものの製造には,高度の真空中での溶融,蒸留,昇華などの手法も用いられる.いずれも元素単体は銀白色の金属で,塩基性が強い.塩基性はイオン半径の減少とともに減少する.空気中では常温でも徐々に酸化され,酸や熱水には水素を発生して溶ける.室温でアルカリ水溶液には溶けない.S,Se,Te,As,B,C,Hなどの単体とは,反応条件を選べば,いずれも直接に反応する.ランタノイドでは,ランタノイド収縮のため,YはHo~Erに性質が似る.Scは外殻電子配置の類似からやはり性質がランタノイド(ことに重希土)に似る.ランタノイドの種々の配位化合物では,中心となる金属イオンの大きさが,同じ配位子による錯体の配位数や配位型に影響するが,Y,Scもランタノイドの相当する大きさの元素と同型の錯体をつくる傾向がある.
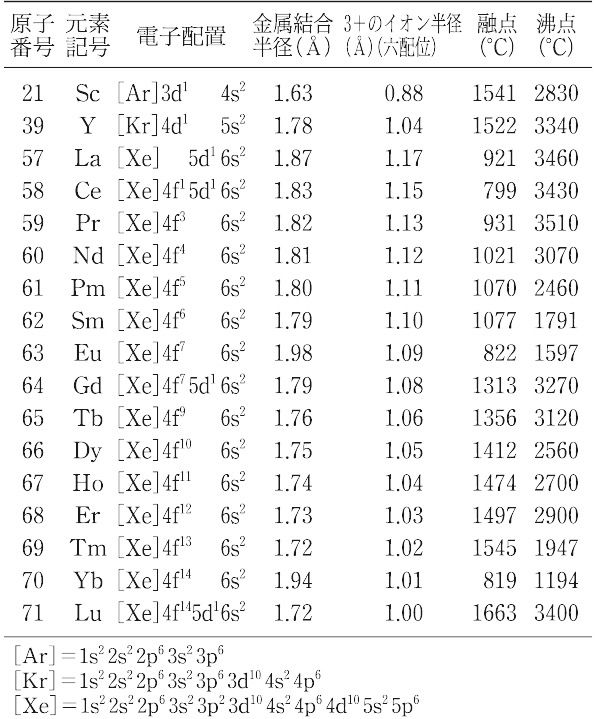
【Ⅱ】化合物:希土類元素は,一般に3+の原子価をとる.例外として,Ceは4+,Sm,Eu,Ybは2+となりうる.磁性は,Sc3+,Y3+,La3+,Ce4+,Lu3+,Yb2+ は反磁性,それ以外は常磁性である.希土類の3+価イオンは安定で,イオンの大きさもアルカリ金属やアルカリ土類金属のイオンと類似しているため,ペロブスカイト型構造のような複合酸化物を容易に形成し,それらのなかには格子欠陥に伴う特異性を示すものがある.また,4f軌道が不完全に充填されていることによる磁気的,光学的な特異性を示し,それらを利用した用途が多い.塩のうち,Cl-,Br-,I-,NO3-,ClO4-などの塩は水に可溶,F-,CO32-,PO43-,(COO)22- などの塩は水に不溶.SO42-の塩もあまり溶けないが,溶解度はLa→Euでは順次減少し,それ以後は順次増加する.希土類の塩の製造の途中,シュウ酸塩が水に難溶なことを利用して,希土類をほかの金属塩などから沈殿分離し,次にこれを加熱分解して酸化物とした後に,各種の酸に溶解してそれぞれの塩をつくることがある.希土類の塩のうちで,次のものは4f電子の影響で着色しているが,それ以外は無色である.

希土類元素はクエン酸,EDTAをはじめ,多くの配位子と錯体をつくる.錯体の配位数は,Scでは6をとることが多いが,Yおよびランタノイドでは7以上が普通である(7,8,9が多いが,それ以上のこともある).【Ⅲ】用途:(1)合金:発火合金(Ce-Fe,La-Mg),永久磁石用合金(SmCo3,Nd-Fe(+Co)-B系合金など),水素吸蔵合金(LaNi5,CeNi5),光磁気ディスクの記録層用合金膜(Gd,Tb,Dy-Fe,Co系合金)などがある.(2)酸化物:CeO2または軽希土のミッシュメタル酸化物は,ガラスなどの研磨に用いられる.混合酸化物には高温超伝導体(たとえば,銅酸化物系のYBa2Cu3O7-δ)がある.また,希土類の混合酸化物は,燃料電池の電解質や電極物質にも用いられる.(3)原子力関連:Gdは元素中で中性子捕獲能力が最大である(Eu,Dyがこれにつぐ)から,原子炉の緊急制御用に用いられる.また,Dy(+Gd)-Pb合金は放射線しゃへい用材に,Yは原子炉の減速材に用いられる.(4)セラミックスなど:(a)特殊ガラス;La添加ガラスは高屈折,低分散でレンズ用,Nd添加ガラスはまぶしさを避ける眼鏡,窓ガラスなどに用いられる.また,色ガラス用に添加される(Ce→黄,Pr→黄緑,Nd→赤紫~青,Er→桃など).(b)工業材;焼結ジルコニア(Y2O3-ZrO2)は硬度大で,刃物,工具などに加工して利用される.また,ゼオライト置換型などの触媒は石油クラッキングに利用される.(c)ガーネット型電子材料;YIG(Y3Fe5O12),YAG(Y3Al5O12),GGG(Gd3Ga5O12)など各種のものがつくられている.YIGやGGGは,磁気バブルメモリー材に,YAGは,Ndを数% ドープしたものが,波長1.06 μm の大出力レーザー光源用に用いられる.また,レーザー核融合用や,手術用レーザーにも利用される.さらに,これらは,コンデンサー,バリスター,誘電体素子などの電子材料にも用いられる.また,YAGやGGGは,硬く屈折率も大きいので人造宝石としても用いられる.(d)光ファイバー;Erなどをドープしたガラス,とくにフッ化物ガラスが利用され,研究されている.(e)センサー;LaF3の単結晶膜を利用する F- イオンセンサーなどが利用されている.(f)蛍光体;テレビのブラウン管用の蛍光体として,赤色用のY2O2S(+Eu数%)をはじめ,いろいろのものがある.着色蛍光灯用の蛍光体には,赤色用以外にLa,Ce,Tb→緑,Eu2+→青などを加えたものが利用される.医療用には,CTのX線測定感度向上のため,X線シンチレーター用に,(Y,Gd)2O2S(+数% のEu,Pr)を用いる.直接X線撮影用フィルムに増感剤として,La2O2S(+少量のTb)を塗布する.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
改訂新版 世界大百科事典 「希土類元素」の意味・わかりやすい解説
希土類元素 (きどるいげんそ)
rare earth elements
原子番号57番のランタンLaから71番のルテチウムLuまでの15元素(ランタノイドという)に,さらにランタンと同族(第ⅢA族)である21番のスカンジウムScと39番のイットリウムYを加えた17元素の総称。すべて金属元素で,61番のプロメチウムPmのみは人工放射性元素であり,天然には見いだされない。希土類の〈土〉とは,融点が高く,還元されにくい金属酸化物をさす古語であるが,これらの元素ははじめスウェーデン産のまれな鉱物から酸化物の混合物として取り出され(ガドリンJ.Gadolin,1794),その後20世紀初頭までに多数の化学者の研究によって現在知られている諸元素に分離されたのでこの名がある。ただし61番元素はウランの核分裂の研究に関連して1947年にはじめて発見されたので,全元素の発見と確認には150年余の歳月を要したことになる。希土類元素の大部分を占めるランタノイドは化学的性質が互いにきわめてよく似ており,3価の陽イオンとなって化合物をつくるが,その半径はランタニド収縮と呼ばれる現象のためにLa3⁺(1.06Å)からLu3⁺(0.85Å)まで著しく収縮する。一方,イットリウムはもともとランタンと同族の元素であるうえ,そのイオンY3⁺(0.88Å)はLa3⁺よりは小さいが,Lu3⁺やその手前の二,三の元素のイオンよりはやや大きく,ちょうどランタノイドの一員のような性質のイオンの化合物をつくる。スカンジウムだけはイオン半径(Sc3⁺,0.68Å)がとくに小さく,他の元素とはやや性質が異なる。
このように大多数の元素が化学的によく似ているので,希土類元素は鉱物中につねに一団となって見いだされる。工業原料として最も有名な鉱物はインドやブラジルに多いモナザイト(モナズ石)で,これを強酸または強アルカリで分解して得られる溶液の成分をイオン交換樹脂を用いて分離し,それぞれの元素の塩を取り出し,溶融電解法で金属単体を得る。金属は銀白色で,うすい酸のほか熱湯とも反応して水素を発生し,空気中で酸化・変色し,150~180℃で着火する。熱すれば塩素,水素,窒素などとも反応する。アルカリには溶けない。総じてアルミニウムなどのふつうの3価金属よりもずっと陽性であり,かつ比重が大きい。種々の特別な用途があり,ライターの石(セリウム約65%,鉄約35%を含む合金)は発火点が130℃くらいなので,強くこすると発火する性質を利用したものである。またミッシュメタル(希土類元素どうしの混合合金)は鉄鋼工業において製品の品質を改善するためにしばしば添加され,酸化ネオジムを3~10%含む淡青色のガラスは黄色い光をよく吸収するので,まぶしさを避ける眼鏡に用いられる。フッ化物の混合物はアーク灯用のカーボンにまぜて輝度を増すために,酸化物の混合物はガラスの研磨に,また高純度のランタンおよびセリウムの酸化物は光学レンズ用に用いられる。このほか,原子力工業用の制御材(ガドリニウム,ユウロピウム),耐食材(イットリウム),テレビジョンのブラウン管の蛍光体,電磁気材料など,数多い用途が近年に開発されている。
執筆者:曽根 興三
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
最新 地学事典 「希土類元素」の解説
きどるいげんそ
希土類元素
rare earth element
ランタニドに加え,YとScを合わせた元素群。REEと略記。Scを含めない場合もある。また軽希土類元素(LREE:La・Ce・Pr・Nd・Pm・Sm・Eu)と重希土類元素(HREE:Gd・Tb・Dy・Ho・Er・Tm・Yb・Lu)に分けたり,Sm~Dyを中希土類元素と呼ぶこともある。化学的性質の類似性から,相伴って産することが多い。地球化学的解析手法に,試料中のREE存在量をコンドライト中の存在度との比で表し,原子番号順に並べるMasuda-Coryell plotがある。原子番号が増加するにつれ,電子は最外殻軌道でなく内部の4f軌道に充塡されるため,イオン半径は系統的に減少し,希土類元素存在度パターンは滑らかな変化を示す。希土類元素はさまざまな工業素材に添加される重要な資源であり,大陸地域のカーボナタイト/アルカリ岩鉱床と大陸周辺部の砂鉱床が主要な鉱床となっている。日本では福島県石川地方や岐阜県苗木地方に多くの希元素鉱物の産出が報告されているが,資源となるだけの量は産しない。フッ化セリウム石(ハロゲン塩)・フェルグソナイト(酸化物)・バストネ石・シンキス石・パリサイト(以上炭酸塩)・モナズ石・ゼノタイム(以上リン酸塩)・ガドリン石・褐れん石(以上珪酸塩)等に濃集。鉱床はカーボナタイト鉱床(バストネ石)・漂砂鉱床(モナズ石・ゼノタイム)・風化残留鉱床(花崗岩風化殻中のイオン吸着型)・マグマ性リン鉱床(りん灰石に固溶)など。発火合金・石油精製用触媒・光学ガラス材・研磨材のほか希土類蛍光体・強磁性材・磁気バブルメモリ材・中性子吸収材などに中希土の需要が増大。世界年産量はREO換算で6万t(1992),主産国は中国(35.6%)・米国(34.5%)・旧ソ連(13.3%)・オーストラリア(6.4%)・インド(6.4%)。
執筆者:平野 英雄・田中 剛
参照項目:ランタニド
出典 平凡社「最新 地学事典」最新 地学事典について 情報
百科事典マイペディア 「希土類元素」の意味・わかりやすい解説
希土類元素【きどるいげんそ】
→関連項目常磁性|信越化学工業[株]|セリウム|ランタニド元素|レアアース
出典 株式会社平凡社百科事典マイペディアについて 情報
ブリタニカ国際大百科事典 小項目事典 「希土類元素」の意味・わかりやすい解説
希土類元素
きどるいげんそ
rare earth element
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
岩石学辞典 「希土類元素」の解説
希土類元素
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...