精選版 日本国語大辞典 「炭酸カルシウム」の意味・読み・例文・類語
たんさん‐カルシウム【炭酸カルシウム】
日本大百科全書(ニッポニカ) 「炭酸カルシウム」の意味・わかりやすい解説
炭酸カルシウム
たんさんかるしうむ
calcium carbonate
炭酸のカルシウム塩。工業部門では炭カルともいう。天然には方解石、大理石、石灰石、あられ石、白亜などの鉱石として産出する。工業的には、石灰岩を乾式粉砕し、ふるい分けまたは風簸(ふうひ)(空気中での自然沈降速度の違いを利用する粉体分別操作)によって微粉を集め製品とする(重質炭カル)。石灰乳に二酸化炭素を吹き込んで生じた沈殿を乾燥、粉砕することによっても製造される(沈降炭酸カルシウムまたは軽質炭カル)。貝類を湿式粉砕したものも利用される(胡粉(ごふん))。一般に白色固体または無色の結晶。結晶には二つの変態がある。熱すると次の反応式に従って解離する。これは吸熱反応である。
CaCO3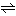 CaO+CO2-42.0kcal
CaO+CO2-42.0kcal
898℃で解離圧は1気圧に達する。この反応は二酸化炭素と酸化カルシウムの工業的製造に用いられる。酸と反応して二酸化炭素を発生する。純粋な水にはほとんど溶けないが、二酸化炭素を含んだ水には炭酸水素カルシウムとなって溶ける。
CaCO3+CO2+H2O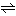 Ca(HCO3)2
Ca(HCO3)2
二酸化炭素を含んだ天然水が石灰岩を溶解した結果生じた空洞が鍾乳洞(しょうにゅうどう)である。その中で温度の上昇や分圧の低下によって二酸化炭素の溶存量が減少すると平衡は左に偏り、炭酸カルシウムが沈積する。このようにして生成したのが鍾乳石や石筍(せきじゅん)である。
石灰石はポルトランドセメント、酸化カルシウムなどの原料、大理石は建築材料として用いられる。重質炭カルは顔料、紙やゴムの充填(じゅうてん)剤に用いられ、沈降炭酸カルシウムは顔料、塗料、製紙、歯みがき粉に、胡粉も白色顔料や水性塗料に用いられる。
[鳥居泰男]
農業への利用
土壌の酸性を中和することを目的に使用される。純度の高いものは薬品用、工業用に適するので、比較的不純物の多いものが農業用として用いられている。通常アルカリ分53~60%を含み、粒度の粗いものほど土壌酸性矯正速度が遅い。炭酸カルシウムは生石灰(せいせっかい)、消石灰よりも塩基性は弱いが、大気中での安定性がもっとも大きく、貯蔵中に変質することがない。カーボンブラックで黒く着色したものは融雪を促進する効果があるため、北海道などの寒冷地で早春に用いられる。なお酸化マグネシウム(苦土)を含むものは苦土炭カルといい、マグネシウムが欠乏している酸性土壌に効果がある。
[小山雄生]
改訂新版 世界大百科事典 「炭酸カルシウム」の意味・わかりやすい解説
炭酸カルシウム (たんさんカルシウム)
calcium carbonate
化学式CaCO3。天然には,方解石,氷州石,アラゴナイト(アラレ石),石灰岩,大理石,チョーク(白亜)などとして多量に産出する。また,貝殻の主成分は炭酸カルシウムであり,これを微粉砕したものは胡粉(ごふん)と呼ばれ,白色顔料となる。実験室では,カルシウム塩の水溶液に炭酸アルカリ水溶液を加えると,白色の沈殿(沈降炭酸カルシウム)として得られる。Ca2⁺イオンと平面正三角形のCO32⁻イオンから成る結晶であるが,それらの空間的配列の違いによって方解石型(比重2.71),アラレ石型(比重2.93)の2種の結晶形のものができる。たとえば上の沈殿反応を煮沸下で行えば後者が,また沈殿と溶液を共存させて長く放置すれば前者がそれぞれ生ずる。約900℃に熱すれば次式のように解離する。
CaCO3⇄CaO+CO2
この反応は酸化カルシウム(生石灰)CaOや二酸化炭素の工業的製造に利用される。水には溶けにくく,100gの水に対する溶解度は方解石型1.3mg(18℃),アラレ石型1.5mg(18℃)にすぎない。しかし二酸化炭素を含む水には炭酸水素カルシウムCa(HCO3)2となって溶ける。鍾乳洞は,石灰岩がこの反応を受けてできたもの。
CaCO3+CO2+H2O─→Ca(HCO3)2
酸を作用させると二酸化炭素を発生して溶けるので,実験室で二酸化炭素を発生させるために利用される。
CaCO3+2HCl─→CaCl2+CO2+H2O
沈降炭酸カルシウムは,ゴム,プラスチック用充てん剤,製紙用てん料,歯磨剤,医薬(制酸剤)などに用いられる。
執筆者:曽根 興三
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「炭酸カルシウム」の解説
炭酸カルシウム
タンサンカルシウム
calcium carbonate
CaCO3(100.09).天然には方解石,石灰石,大理石,あられ石,白亜として産出し,工業的にはこれらを粉砕して利用する.化学的製法で得られるものは沈降炭酸カルシウムとよばれ,カルシウムの可溶性塩の水溶液にアルカリの炭酸塩を加えると沈殿として得られる.結晶構造は次の2種類が存在する.あられ石型構造は斜方晶系.密度2.93 g cm-3.方解石型構造は六方晶系.密度2.71 g cm-3.融点1339 ℃(10.38 MPa).いずれも水には難溶であるが,二酸化炭素を含む水には炭酸水素カルシウムを生じて溶ける.強熱すると二酸化炭素と酸化カルシウムとに解離する.酸を作用させると二酸化炭素を放出してカルシウム塩を生じる(二酸化炭素の実験室的製法).セメントの主原料,建材,石灰乳,白色顔料,塗料,歯磨き粉,食塩の凝固防止剤,ゴムタイヤの製造,医薬品(制酸剤)などに用いられる.[CAS 471-34-1]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「炭酸カルシウム」の意味・わかりやすい解説
炭酸カルシウム
たんさんカルシウム
calcium carbonate
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
百科事典マイペディア 「炭酸カルシウム」の意味・わかりやすい解説
炭酸カルシウム【たんさんカルシウム】
→関連項目酸化カルシウム|石灰肥料|体質顔料
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「炭酸カルシウム」の解説
炭酸カルシウム
世界大百科事典(旧版)内の炭酸カルシウムの言及
【制酸薬】より
…
[局所性制酸薬]
塩酸中和後も消化管から吸収されにくい化合物で,粘膜の被覆作用もある。酸化マグネシウム,炭酸カルシウム,水酸化アルミニウムゲル,胃粘膜ムチン,イオン交換樹脂など。二次性酸分泌亢進は起こしにくく,制酸薬として好ましい条件を備えたものが多い。…
【石灰肥料】より
… 各種石灰肥料の原料となる石灰岩やドロマイトは日本で豊富に産出する。主要な石灰肥料には生石灰,消石灰,炭酸カルシウム,苦土石灰や他の産業の副生物として生産される副産石灰がある。生石灰は石灰岩をコークスとともに900~1000℃で焙焼(ばいしよう)して製造するが,その主成分は酸化カルシウムCaOで,アルカリ分は80%以上含有される。…
【炭酸塩補償深度】より
…炭酸カルシウムCaCO3は海洋の表層水では過飽和であるが,深くなるほど急激に飽和度を減じ,2500m以深では不飽和になる。CaCO3の溶解度は,水圧が増すほど,水温が低くなるほど,また炭酸ガスの分圧が増すほど増加するからである。…
※「炭酸カルシウム」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

