精選版 日本国語大辞典 「金属間化合物」の意味・読み・例文・類語
きんぞくかん‐かごうぶつ‥クヮガフブツ【金属間化合物】
改訂新版 世界大百科事典 「金属間化合物」の意味・わかりやすい解説
金属間化合物 (きんぞくかんかごうぶつ)
intermetallic compound
金属元素と金属元素との間に形成される化合物で,金属的な性質を示す固体結晶である。化合物といっても気体分子化合物とはまったく異なり,合金の構成要素(相)の一つとして金属材料の組織の中に出現する固相であるので,中間相intermediate phaseという呼び方もある。単純な原子価の考え方が適用できない結晶も数多く含まれる。
結晶を特徴づけるのは規則正しい格子点の配列である。格子点はいくつかの等価の位置に分けられる。たとえばAB2という結晶はA位置1に対しB位置が2である構造を意味する。AB2を可能にする結晶形は数多くあるが,その一つのC14型結晶でA位置をマグネシウムMg原子,B位置を亜鉛Zn原子が占有すると,MgZn2という一つの典型的な金属間化合物となる。結晶をつくる格子点の比は正確に1対2であるが,現実の結晶では格子点は正しくない原子(たとえばMgの占めるべき位置にZnもしくは他の不純物元素の原子)によって占有されたり,何の原子も存在しない(空格子点)状態が起こりうるので,MgZn2相といってもMgとZnのモル比が正確に1対2となるわけではない。すなわち中間相(金属間化合物)にも固溶範囲が存在する。
金属元素と非金属元素の区別は明確でなく,中間的な元素も数多く存在する。このため無機物の固体結晶のうちどこまでを金属間化合物と呼べばよいかについては必ずしも明らかでなく,結合様式,結晶構造などもきわめて多種多様である。一般に,原子価効果化合物,原子半径効果化合物,電子化合物,の三つに大別される。
(1)原子価効果化合物normal valency compound 電気化学的化合物electrochemical compoundとも呼ばれ,通常の原子価の法則を満足しているもので,比較的単純な結晶形をとり,固溶範囲は狭い。半導体材料のAlN,InP,GaAsなどのIII-V化合物,ZnS,CdTeなどのII-VI化合物はこの分類の例である(II,III,V,VIは周期表の族)。
(2)原子半径効果化合物size factor compound ラーベスLaves相,シグマσ相,侵入型化合物interstitial compoundなどが含まれる。成分原子の半径比が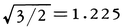 の近くの値(1.05~1.68)をとるときにはA格子位置が16個の隣接B位置,B格子位置が12個の隣接A位置をもつAB2型結晶をとると成分原子は最もよく充てんする構造となる。このような構造の化合物は数多く知られ,一括してラーベス相と呼ばれる。MgZn2,FeB2,TiBe2などの例がある。Fe-Cr合金は高温ではほとんど全組成範囲にわたって固溶体(体心立方格子)をつくるが,低温ではFeの43~50原子%を中心として硬くてもろいσ相を生ずる。この化合物の結晶構造は30格子点で単位胞が形成される複雑なものであり,Mn,V,Co,Mo,NiなどとFeの合金にも出現する。この相の出現は耐熱合金などの強度低下の原因となる。体心立方格子金属に対して原子半径が金属の半径の0.59倍以下と小さい原子の場合には,特定の格子間位置を占拠した侵入型化合物を形成する。遷移金属の水素化物,窒化物,炭化物などに例がみられる。Cの半径はFeの半径の約0.63倍であり単純な侵入型の位置には入れないので,複雑な構造をとるFe3Cというセメンタイト相をつくる。炭化物のなかにはCr23C6,Mn23C6,といった複雑なものも存在する。
の近くの値(1.05~1.68)をとるときにはA格子位置が16個の隣接B位置,B格子位置が12個の隣接A位置をもつAB2型結晶をとると成分原子は最もよく充てんする構造となる。このような構造の化合物は数多く知られ,一括してラーベス相と呼ばれる。MgZn2,FeB2,TiBe2などの例がある。Fe-Cr合金は高温ではほとんど全組成範囲にわたって固溶体(体心立方格子)をつくるが,低温ではFeの43~50原子%を中心として硬くてもろいσ相を生ずる。この化合物の結晶構造は30格子点で単位胞が形成される複雑なものであり,Mn,V,Co,Mo,NiなどとFeの合金にも出現する。この相の出現は耐熱合金などの強度低下の原因となる。体心立方格子金属に対して原子半径が金属の半径の0.59倍以下と小さい原子の場合には,特定の格子間位置を占拠した侵入型化合物を形成する。遷移金属の水素化物,窒化物,炭化物などに例がみられる。Cの半径はFeの半径の約0.63倍であり単純な侵入型の位置には入れないので,複雑な構造をとるFe3Cというセメンタイト相をつくる。炭化物のなかにはCr23C6,Mn23C6,といった複雑なものも存在する。
(3)電子化合物electron compound。1926年ころにヒューム・ロザリーW.Hume-Rotheryらによって認められた中間相で,合金の価電子数(Fe,Co,Niでは0,Cu,Ag,Auでは1,Mg,Zn,Beでは2,Alでは3,Sn,Siでは4と数える)の和と原子数の比が3/2,21/13,7/4のような一定の比をとるところで出現する(ヒューム=ロザリーの規則)化合物である。3/2型としてはCuZn,Cu3Al,Cu5Si,21/13型としてはCu5Zn8,Fe5Zn21,7/4型としてはCuZn3,Ag5Al3などが知られている。電子化合物は固溶範囲が広く,規則構造だけでなく不規則構造をとるものも出現する。
金属間化合物の用途はきわめて広く,超電導材料(Nb3Sn,V3Ga),永久磁石(SmCo5,MnBi),水素吸蔵金属(FeTi,LaNi5),形状記憶合金(NiTi。〈形状記憶効果〉の項参照),化合物半導体(GaAs,CdS)などがあげられる。なかには,強度が高温ほど増加するという性質をもつものもあり(Ni3Al),これは耐熱合金(超合金superalloy)に応用されている。一般に金属間化合物はもろく成形加工が困難なため,実用にあたっては鋳造,粉末成形,高温加工法などが技術的に開発されている。しかし単結晶にすると延性を示すものもある。
執筆者:増子 昇+山本 良一
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
化学辞典 第2版 「金属間化合物」の解説
金属間化合物
キンゾクカンカゴウブツ
intermetallic compound
2種類以上の金属元素のみから形成される化合物.【Ⅰ】電子化合物:ヒューム-ロザリーの規則が適用されるもの.たとえば,e/a(eは価電子の合計,aは原子数の合計)が3/2のβ相化合物(CuZn,Ag3Alなど),21/13のγ相化合物(Cu5Zn8),7/4のε相化合物(CuZn3,AgMg3など)である.周期表11族と多価の12~14族の元素間の化合物に例がみられる.【Ⅱ】配位多面体化合物:最密原子配列をもち,各原子は互いに12~16面体型配位構造となっている.たとえば,σ相化合物(FeCr,FeVなど,周期表5,6族-7~10族元素間の原子数比1:1の合金型化合物),ラーヴェス相化合物(MgZn2,MgNi2など,組成式がAB2で,原子半径比が,A:Bが約1.2:1のもの)などがある.【Ⅲ】電気化学的化合物:電気陰性度の差が大きい陽性と陰性の金属または半金属間で,原子価が満足されるもの.Mg2Pb,GaAs,CdSなどが該当する.【Ⅳ】金属と結合する成分元素がI,C,Si,Ge,As,Seなどのものや,金属結合格子間に軽原子H,C,N,Oなどが入った侵入型化合物も含めることがある.これらのなかには,通常の合金にはみられない特性をもつものがある.たとえば,Ⅲ-Ⅴ半導体(GaAs),超伝導材料(Nb3Sn),水素吸蔵合金(LaNi5),永久磁石材料(SmCo3),耐熱合金(Ni3Al)などである.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
日本大百科全書(ニッポニカ) 「金属間化合物」の意味・わかりやすい解説
金属間化合物
きんぞくかんかごうぶつ
intermetallic compound
金属元素と他の金属元素あるいは非金属元素とが簡単な整数比の原子組成をもつ相を形成し、その結晶構造にも規則性があるとき、これを金属間化合物という。合金の一種ともみえるが、連続的に組成が変化しうる一般の合金とは異なり、化学量論的定比組成を示すのが特徴である。原子間の化学結合は金属結合性であり、組成式中の各原子がもつ価電子(s電子とp電子)数の総和と原子数との比が同じになるものは同じ構造をとる、というヒューム‐ロザリーの規則が成立する例が知られている。たとえばCuZn、AgCd、Cu3Al、Cu5Snはいずれもこの比が3対2となり、塩化セシウム型、あるいはそれと本質的に等価な結晶構造をとる。
13族元素と15族元素との1対1の化合物は半導体になることが知られているが、AlAs、AlSb、GaP、GaAs、InP、InAsなどはいずれもダイヤモンドと同じ原子配列をとる閃亜鉛鉱型構造(せんあえんこうがたこうぞう)をもっている。
[岩本振武]
ブリタニカ国際大百科事典 小項目事典 「金属間化合物」の意味・わかりやすい解説
金属間化合物
きんぞくかんかごうぶつ
intermetallic compound
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
百科事典マイペディア 「金属間化合物」の意味・わかりやすい解説
金属間化合物【きんぞくかんかごうぶつ】
→関連項目合金|固溶体|メカニカル・アロイング
出典 株式会社平凡社百科事典マイペディアについて 情報
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...

